دژنراسیون ماکولا وابسته به سن (AMD) یکی از علل اصلی نابینایی است. در سد خونی بیرونی شبکیه چشم (oBRB) که توسط اپیتلیوم رنگدانه شبکیه (RPE)، غشای بروخ و کوریوکاپیلاریس تشکیل شده است، شروع می شود. مکانیسمهای شروع و پیشرفت AMD به دلیل فقدان مدلهای مرتبط فیزیولوژیکی oBRB انسانی هنوز باید بهتر درک شوند.
تیم تحقیقاتی موسسه ملی چشم (NEI) که بخشی از موسسه ملی بهداشت است، از بیمار استفاده کرد سلول های بنیادی و پرینت زیستی سه بعدی برای تولید بافت چشمی که درک مکانیسم بیماریهای کورکننده را ارتقا میدهد. دانشمندان ترکیبی از سلول ها را چاپ کردند که سد بیرونی خونی شبکیه را تشکیل می دهند.
اپیتلیوم رنگدانه شبکیه (RPE)، جدا شده از کوریوکاپیلاریس غنی از رگ های خونی توسط غشای بروچ، سد بیرونی خونی شبکیه را می سازد. کوریوکاپیلاریس و RPE مواد مغذی و ضایعات را تحت کنترل غشای بروخ مبادله می کنند. Drusen که تجمع لیپوپروتئینی است در خارج از غشای بروخ در AMD ایجاد می شود و مانع عملکرد آن می شود. تخریب RPE در طول زمان باعث زوال گیرنده نور و از دست دادن بینایی می شود.
دانشمندان سه نوع سلول مشیمیه نابالغ را در یک هیدروژل ترکیب کردند: پری سیت ها، سلول های اندوتلیال و فیبروبلاست ها. سپس ژل را روی داربست زیست تخریب پذیر چاپ کردند. در عرض چند روز، سلول ها شروع به بلوغ و تبدیل به یک شبکه مویرگی متراکم کردند.
در روز نهم، دانشمندان سلولهای اپیتلیال رنگدانه شبکیه را در طرف دیگر داربست کاشتند. بافت چاپ شده در روز 42 به بلوغ کامل رسید. تجزیه و تحلیل بافت و آزمایش ژنتیکی و عملکردی نشان داد که بافت چاپ شده شبیه به سد خونی-شبکیه بیرونی بومی به نظر می رسد و رفتار می کند.
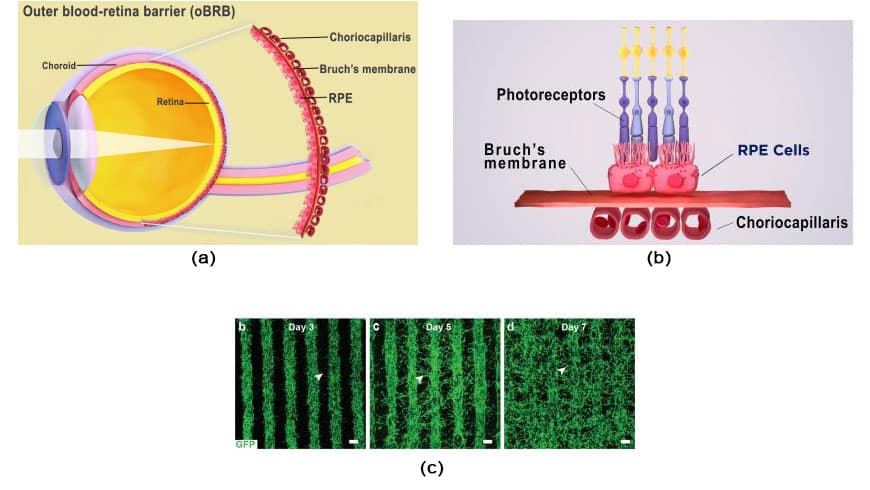
ب سد خونی- شبکیه خارجی چشم شامل اپیتلیوم رنگدانه شبکیه، غشای بروخ و کوریوکاپیلاریس است. اعتبار تصویر: موسسه ملی چشم.
ج. رشد رگ های خونی در ردیف های چاپ شده مخلوط سلول اندوتلیال-پریسیت-فیبروبلاست. در روز هفتم، رگهای خونی فضای بین ردیفها را پر میکنند و شبکهای از مویرگها را تشکیل میدهند. اعتبار تصویر: کاپیل بهارتی.
هنگامی که در معرض استرس قرار می گرفت، بافت چاپ شده ویژگی های AMD در مراحل اولیه را نشان می داد، مانند رسوبات دروسن در زیر RPE، و به مرحله پایانی مرحله خشک AMD، جایی که تجزیه بافت مشاهده می شد، پیشرفت کرد. سطوح پایین اکسیژن باعث ایجاد ظاهری مرطوب مانند AMD با پرولیفراسیون عروق مشیمیه که به ناحیه زیر RPE منتقل شد. هنگامی که برای درمان AMD استفاده می شود، داروهای ضد VEGF تشکیل و مهاجرت رگ های خونی را کند می کند و در عین حال شکل بافت را نیز بهبود می بخشد.
کاپیل بهارتی، دکترا، که سرپرست بخش NEI در تحقیقات ترجمه ای سلول های بنیادی و چشمی است، گفت: با چاپ سلولها، ما تبادل نشانههای سلولی لازم برای آناتومی طبیعی سد خونی-شبکیه بیرونی را تسهیل میکنیم. به عنوان مثال، حضور سلول های RPE باعث القا می شود بیان ژن تغییرات در فیبروبلاستها که به شکلگیری غشای بروخ کمک میکنند - چیزی که سالها پیش پیشنهاد شد، اما تا قبل از مدل ما ثابت نشده بود.
دانشمندان به دو موضوع تکنولوژیکی پرداختند: ایجاد یک داربست زیست تخریب پذیر مناسب و دستیابی به یک الگوی چاپ ثابت. آنها یک هیدروژل حساس به دما ساختند که در حالی که ژل سرد بود، ردیف های متمایز ایجاد می کرد اما با گرم شدن ژل حل می شد. سیستم دقیق تری برای ارزیابی معماری بافت با سازگاری ردیف خوب امکان پذیر شد. علاوه بر این، آنها نسبت فیبروبلاست ها، سلول های اندوتلیال و پری سیت ها را در ترکیب سلولی بهینه کردند.
یکی از نویسندگان مارک فرر، دکترا، مدیر آزمایشگاه چاپ زیستی بافت سه بعدی در مرکز ملی پیشرفت علوم ترجمه NIH، و تیم او برای ساختن بیولوژیکی بافتهای مانع خونی-شبکیه بیرونی "در چاه" تخصص ارائه کردند. همراه با اندازه گیری های تحلیلی برای فعال کردن غربالگری دارو.
[محتوای جاسازی شده]
Ferrer "تلاش های مشترک ما منجر به مدل های بافت شبکیه بسیار مرتبط بیماری های دژنراتیو چشم شده است." گفت:. چنین مدل های بافتی کاربردهای بالقوه زیادی در کاربردهای ترجمه ای از جمله توسعه درمانی دارند.
مرجع مجله:
- مین جائه سونگ، راس کوین و همکاران. سد بیرونی شبکیه سه بعدی چاپ شده زیستی، فنوتیپ مشیمیه وابسته به RPE را در دژنراسیون ماکولا پیشرفته آشکار می کند. روش های طبیعت، 2022؛ DOI: 10.1038/s41592-022-01701-1