پروتئینهای غیر معمولی که در مغز ایجاد گره میکنند و نورونها را از بین میبرند، منجر به اختلالات نورودژنراتیو میشوند.
نوروبیولوژیست ها در EPFL اکنون برخی از مکانیسمهای کلیدی تشکیل این درهمتنیدگیها را شناسایی کردهاند. آنها همچنین آسیب پذیری سلولی را در مراحل اولیه تخریب عصبی مشاهده کردند.
به گفته دانشمندان، متوقف کردن یا کاهش سرعت اولین قطع ارتباط نورون ها می تواند مراحل بعدی را با شروع انحطاط نورون ها کند کند.
در این مطالعه، دانشمندان مدلهای شروع بزرگسالی را برای سمیت تاو انسانی (hTau) در مگس سرکه (مگس میوه) مهندسی کردند. این امکان اندازه گیری کمی وابسته به سن از دست دادن سیناپس سیستم عصبی مرکزی و انحطاط آکسون و همچنین اثرات آن بر طول عمر را فراهم کرد تا ارزیابی عوامل مؤثر در تخریب عصبی وابسته به تاو را تسهیل کند. تاو پروتئینی است که در بیماری آلزایمر و سایر اختلالاتی که منجر به جنون.
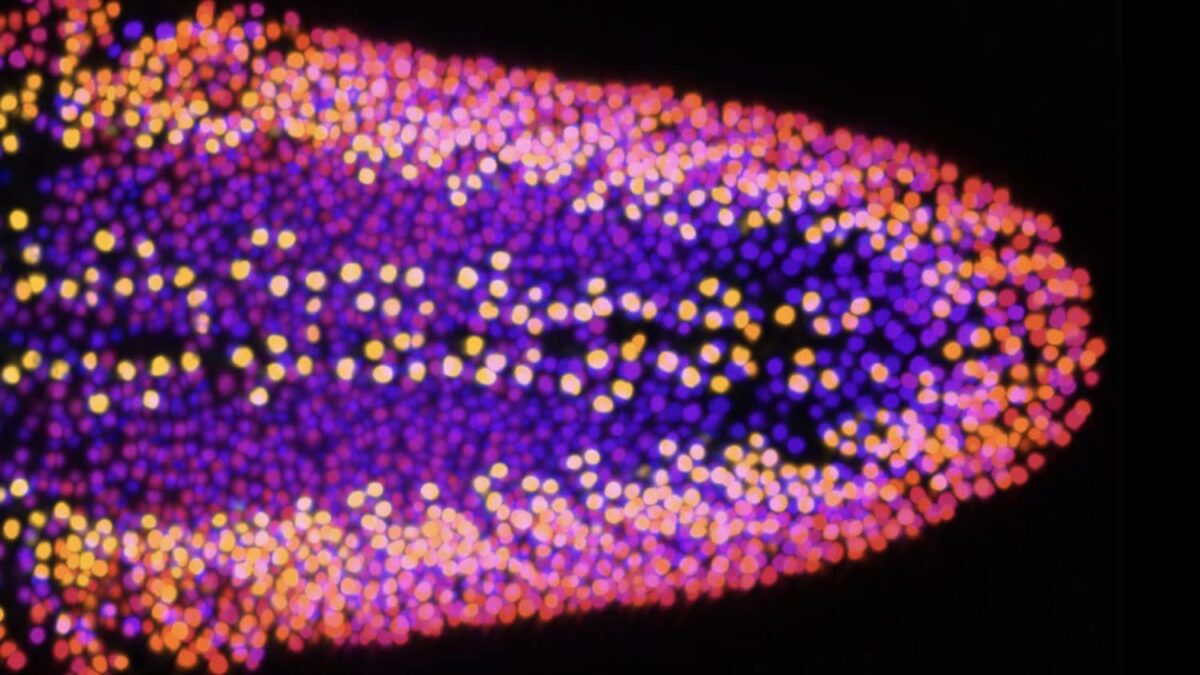
دانشمندان دریافتند که مگس هایی که تاو انسان را بیان می کنند، عمر کوتاه تری نسبت به مگس های کنترل داشتند. آنها بعداً به تأثیر تاو انسان بر روی بدن دست یافتند مغز با استفاده از یک سری فناوری های ژنتیکی، میکروسکوپی و محاسباتی که امکان تصویربرداری دقیق از افراد را فراهم می کند نورون ها.
این اولین باری است که دانشمندان می توانند به تحلیل عصبی در سطح تک نورونی در بافت مغز یک بزرگسال نگاه کنند.
در مقایسه با گروه کنترل، مگسهایی که تاو انسانی را بیان میکردند، از دست دادن قابل توجهی سیناپسها یا اتصالات بین نورونها را نشان دادند. در این حیوانات، نورون ها آکسون نیز منقبض و عقب نشینی کرد.
برایان مک کیب، نویسنده ارشد این مطالعه، مدیر آزمایشگاه ژنتیک عصبی و بیماری و پروفسور دانشکده علوم زیستی EPFL، گفت: زمانی که آکسون جمع شد، نورونها دیگر بخشی از یک مدار عملکردی نبودند. ما باید در این مراحل اولیه مداخله کنیم، زیرا وقتی نورونها میمیرند، نبرد از قبل شکست خورده است.»
تحقیقات بیشتر نشان داد که تخریب عصبی با از دست دادن رترومر، یک مجموعه پروتئینی که می تواند در افراد مبتلا به جهش پیدا کند، تسریع می شود. فلج مرتعش. رترومر به عنوان سیستم بازیافت عمل می کند و پروتئین ها را از تجزیه شدن نجات می دهد و آنها را به سطح سلول باز می گرداند. مسدود کردن فعالیت کمپلکس رترومر منجر به افزایش سطح یک شکل کوتاه شده تاو می شود که سمیت عصبی را تشدید می کند.
دانشمندان خاطرنشان کردند، هنگامی که فعالیت رترومر کاهش می یابد، پروتئین های تاو برای مدت طولانی تری در داخل سلول باقی می مانند، جایی که توسط آنزیم های تخصصی به نام کاسپازها «بریده می شوند». در واقع، مهار تولید شکل کوتاه شده تاو می تواند از بین رفتن سیناپس ها و آکسون ها را متوقف کند.
مک کیب گفت:, «یافتهها نشان میدهند که کاهش فعالیت رترومر، قاچاق تاو را کند میکند. این «ترافیک» به کاسپازها اجازه میدهد تاو را به شکل کوتاهتری برش دهند که میتواند به نورونها آسیب برساند. شناسایی داروهایی که قاچاق تاو را تقویت می کنند ممکن است به کاهش سمیت عصبی کمک کند.
اگر شکل کوتاه شده تاو یک نشانگر تشخیصی برای مغزهای مبتلا به آلزایمر و بیماری پارکینسون باشد، سطح این پروتئین غیر معمول می تواند در غربالگری دارو به عنوان نماینده ای برای اثربخشی دارو استفاده شود.
دانشمندان به درک اولیه ترین مراحل در تخریب عصبی ادامه می دهند.
مرجع مجله:
- اسدزاده، ج.، روچتی، ای.، جیائو، دبلیو و همکاران. کمبود رترومر در مدلهای تائوپاتی، برش و سمیت تاو را افزایش میدهد. Nat Commun 13، 5049 (2022). DOI: 10.1038/s41467-022-32683-5