کنترل از راه دور واکنش های شیمیایی در محیط های بیولوژیکی می تواند طیف متنوعی از کاربردهای پزشکی را امکان پذیر کند. برای مثال، توانایی رهاسازی داروهای شیمی درمانی روی هدف در بدن، می تواند به دور زدن عوارض جانبی مضر مرتبط با این ترکیبات سمی کمک کند. با این هدف، محققان موسسه فناوری کالیفرنیا (کالتچ) یک سیستم دارورسانی کاملاً جدید ایجاد کرده اند که از اولتراسوند برای آزادسازی ترکیبات تشخیصی یا درمانی دقیقاً در زمان و مکان مورد نیاز استفاده می کند.
پلت فرم، توسعه یافته در آزمایشگاه های ماکسول راب و میخائیل شاپیرو، بر روی مولکول های حساس به نیرو بنا شده است که به عنوان مکانوفور شناخته می شوند که در اثر نیروی فیزیکی دچار تغییرات شیمیایی می شوند و مولکول های محموله کوچکتری را آزاد می کنند. محرک مکانیکی را می توان از طریق فراصوت متمرکز (FUS) که به عمق بافت های بیولوژیکی نفوذ می کند و با دقت زیر میلی متری اعمال می شود، ارائه می شود. با این حال، مطالعات قبلی در مورد این روش، به شدت صوتی بالایی نیاز داشت که باعث گرم شدن می شود و می تواند به بافت مجاور آسیب برساند.
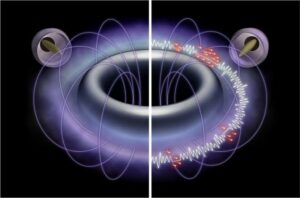
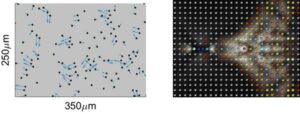
برای فعال کردن استفاده از شدت فراصوت کمتر و ایمنتر، محققان به وزیکولهای گازی (GVs) روی آوردند، نانوساختارهای پروتئینی پر از هوا که میتوانند به عنوان مواد کنتراست اولتراسوند استفاده شوند. آنها فرض کردند که GV ها می توانند به عنوان مبدل های صوتی-مکانیکی برای متمرکز کردن انرژی اولتراسوند عمل کنند: هنگامی که در معرض FUS قرار می گیرند، GV ها تحت کاویتاسیون قرار می گیرند و انرژی حاصله باعث فعال شدن مکانوفور می شود.
نویسنده اول توضیح می دهد: «اعمال نیرو از طریق اولتراسوند معمولاً به شرایط بسیار شدیدی بستگی دارد که باعث انفجار حباب های کوچک گاز محلول می شود. مولی مک فادن در بیانیه مطبوعاتی فروپاشی آنها منبع نیروی مکانیکی است که مکانوفور را فعال می کند. وزیکول ها حساسیت بیشتری به سونوگرافی دارند. با استفاده از آنها، متوجه شدیم که میتوان با سونوگرافی بسیار ضعیفتر، همان فعالسازی مکانیفور را به دست آورد.
گزارش یافته های خود در مجموعه مقالات آکادمی ملی علوممحققان نشان میدهند که این رویکرد میتواند از راه دور باعث آزادسازی مولکولهای محموله از پلیمرهای عاملدار مکانیکی با استفاده از FUS زیست سازگار شود.
توسعه دارورسانی
مک فادن و همکارانش ابتدا پارامترهای سونوگرافی ایمن را برای کاربردهای فیزیولوژیکی شناسایی کردند. آزمایشها با FUS 330 کیلوهرتز، حد بالایی زیست سازگار با حداکثر فشار منفی 1.47 مگاپاسکال با چرخه کاری 4.5٪ (3000 سیکل در هر پالس) را نشان داد که منجر به شدت صوتی 3.6 W / cm شد.2. در یک فانتوم ژل تقلید بافت، این پارامترها منجر به حداکثر افزایش دما تنها 3.6 درجه سانتیگراد شد.
محققان سپس بررسی کردند که آیا FUS می تواند پلیمرهای حاوی مکانیفور را با استفاده از این پارامترهای زیست سازگار فعال کند یا خیر. آنها پلیمر PMSEA حاوی یک مکانیفور زنجیره محور را که با یک مولکول کوچک فلوروژنیک بارگذاری شده بود مورد مطالعه قرار دادند. قرار دادن محلول رقیق این پلیمر در معرض FUS زیست سازگار در حضور GV ها منجر به افزایش شدید فلورسانس می شود که نشان دهنده آزادسازی موفقیت آمیز محموله است - تقریباً 15٪ رهاسازی پس از 10 دقیقه قرار گرفتن در معرض FUS. نکته مهم این است که قرار گرفتن در معرض FUS بدون GV ها باعث ایجاد پاسخ فلوروژنیک نمی شود و تأیید می کند که GV ها نقش اساسی به عنوان مبدل های آکوستو مکانیکی ایفا می کنند.
در مرحله بعد، محققان بررسی کردند که آیا این سیستم برای آزادسازی دارو با تحریک مکانیکی مناسب است یا خیر. آنها عامل شیمی درمانی کامپتوتسین را به مکانیفور و سپس پلیمریزاسیون برای ایجاد PMSEA-CPT کونژوگه کردند و از FUS برای ایجاد رهاسازی کنترل شده استفاده کردند. پس از 10 دقیقه قرار گرفتن در معرض FUS به علاوه GVهای زیست سازگار، تقریباً 8 درصد کمپتوتسین آزاد شد. همانطور که برای مولکول فلوروژنیک یافت شد، در غیاب GV ها هیچ رهایش دارویی مشاهده نشد.
به گفته نویسنده اول یوکسینگ یائواین اولین بار است که نشان داده شده است که FUS یک واکنش شیمیایی خاص را در یک محیط بیولوژیکی کنترل می کند. یائو میگوید: «قبلاً از اولتراسوند برای مختل کردن چیزها یا حرکت دادن اشیا استفاده میشد. اما اکنون با استفاده از مکانیک شیمی این مسیر جدید را برای ما باز می کند.
برای ارزیابی پتانسیل آینده پلت فرم برای شیمی درمانی هدفمند در بیماران، محققان سمیت سلولی آن را بررسی کردند. در شرایط in vitro روی سلول های راجی لنفوبلاست مانند سلولهای انکوبه شده به مدت دو روز با PMSEA-CPT که قبلاً در معرض FUS و GVs قرار گرفته بودند، کاهش قابلتوجهی در زندهمانی نشان دادند. در مقابل، هیچ سمیت سلولی قابلتوجهی در سلولهای انکوبهشده با PMSEA-CPT که در معرض FUS یا PMSEA-CPT در معرض FUS قرار نگرفتهاند، اما بدون GVs مشاهده نشد.

دستگاه کاشتنی با تحریک نور، تحویل دارو قابل برنامه ریزی را فراهم می کند
محققان می نویسند: "رهاسازی مکانیکی بارهای مولکولی از پلیمرها در محیط های آبی، قدرت این رویکرد را برای تصویربرداری غیرتهاجمی زیستی و کاربردهای درمانی مکانیک پلیمری نشان می دهد." به طور گستردهتر، این مطالعه رویکردی را برای دستیابی به کنترل از راه دور واکنشهای شیمیایی خاص تحت شرایط مرتبط با زیست پزشکی با دقت فضایی و زمانی و نفوذ بافت ارائه شده توسط FUS نشان میدهد.
پس از این آزمایشات اولیه در شرایط آزمایشگاهی کنترل شده، محققان اکنون قصد دارند پلت فرم خود را در موجودات زنده آزمایش کنند. ما در حال کار برای ترجمه این کشف اساسی هستیم در داخل بدن راب می گوید: برنامه های کاربردی برای تحویل دارو و سایر فناوری های زیست پزشکی دنیای فیزیک.
- محتوای مبتنی بر SEO و توزیع روابط عمومی. امروز تقویت شوید.
- PlatoData.Network Vertical Generative Ai. به خودت قدرت بده دسترسی به اینجا.
- PlatoAiStream. هوش وب 3 دانش تقویت شده دسترسی به اینجا.
- PlatoESG. کربن ، CleanTech، انرژی، محیط، خورشیدی، مدیریت پسماند دسترسی به اینجا.
- PlatoHealth. هوش بیوتکنولوژی و آزمایشات بالینی. دسترسی به اینجا.
- منبع: https://physicsworld.com/a/biocompatible-focused-ultrasound-delivers-cancer-drugs-on-target/
- : دارد
- :است
- :نه
- :جایی که
- 1
- 10
- ٪۱۰۰
- 3000
- a
- توانایی
- دانشگاه
- دست
- دستیابی به
- فعال کردن
- فعال سازی
- فراهم شده است
- پس از
- عامل
- عاملان
- هدف
- an
- و
- برنامه های کاربردی
- اعمال می شود
- روش
- تقریبا
- هستند
- دور و بر
- AS
- ارزیابی کنید
- مرتبط است
- At
- نویسنده
- مستقر
- BE
- بوده
- بیومدیکال
- بدن
- کران
- گسترده
- اما
- by
- کالیفرنیا
- CAN
- سرطان
- علت
- سلول ها
- تبادل
- شیمیایی
- سقوط - فروپاشی - اضمحلال
- همکاران
- شرایط
- شامل
- کنتراست
- کنترل
- کنترل
- میتوانست
- ایجاد
- ایجاد شده
- چرخه
- چرخه
- آسیب رساندن
- روز
- کاهش
- عمیق
- ارائه
- تحویل
- نشان دادن
- نشان
- نشان می دهد
- شناسایی شده
- توسعه
- دستگاه
- تشخیصی
- DID
- کشف
- مختل کردن
- مختلف
- دارو
- مواد مخدر
- پیش از آن
- اثرات
- قادر ساختن
- انرژی
- به طور کامل
- محیط
- ضروری است
- مثال
- آزمایش
- توضیح می دهد
- قرار گرفتن در معرض
- ارائه
- یافته ها
- نام خانوادگی
- بار اول
- تمرکز
- متمرکز شده است
- به دنبال
- برای
- استحکام
- یافت
- از جانب
- تابع
- اساسی
- آینده
- GAS
- بود
- آیا
- بالا بردن
- کمک
- زیاد
- اما
- HTTPS
- شناسایی
- نشان می دهد
- تصویر
- انفجار
- مهمتر
- in
- افزایش
- جوجه کشی شده است
- اطلاعات
- اول
- موسسه
- به
- موضوع
- ITS
- JPG
- شناخته شده
- لابراتوار
- آزمایشگاه
- رهبری
- ترک کرد
- محدود
- لینک
- زندگی
- کاهش
- حداکثر عرض
- بیشترین
- مکانیکی
- رسانه ها
- پزشکی
- برنامه های پزشکی
- روش
- دقیقه
- مولکولی
- مولکول
- حرکت
- بسیار
- ملی
- ضروری
- منفی
- جدید
- نه
- اکنون
- of
- on
- فقط
- افتتاح
- or
- دیگر
- پارامترهای
- مسیر
- pacientes
- اوج
- نفوذ
- برای
- شبح
- فیزیکی
- فیزیک
- دنیای فیزیک
- برنامه
- سکو
- سیستم عامل
- افلاطون
- هوش داده افلاطون
- PlatoData
- بازی
- به علاوه
- پلیمرها
- پتانسیل
- قدرت
- دقیقا
- دقت
- حضور
- فشار
- فشار
- قبلا
- قابل برنامه ریزی
- پروتئين
- ارائه
- ارائه
- فراهم می کند
- نبض
- محدوده
- واکنش
- واکنش
- آزاد
- منتشر شد
- مربوط
- دور
- ضروری
- محققان
- پاسخ
- نتیجه
- نشان داد
- راست
- نقش
- امن
- امن تر
- همان
- می گوید:
- مشاهده گردید
- حساسیت
- محیط
- طرف
- قابل توجه
- کوچک
- کوچکتر
- راه حل
- منبع
- خاص
- بیانیه
- محرک
- قوی
- مورد مطالعه قرار
- مطالعات
- مهاجرت تحصیلی
- موفق
- مناسب
- سیستم
- هدف
- هدف قرار
- فن آوری
- پیشرفته
- می گوید
- آزمون
- تست
- که
- La
- منبع
- شان
- آنها
- سپس
- اینها
- آنها
- اشیاء
- این
- از طریق
- کوچک
- زمان
- به
- ترجمه کردن
- ماشه
- باعث شد
- درست
- تبدیل
- دو
- زیر
- تحت تاثیر قرار می گیرد
- us
- استفاده کنید
- استفاده
- استفاده
- با استفاده از
- معمولا
- بسیار
- از طريق
- زنده ماندن
- بود
- we
- چه زمانی
- چه
- که
- با
- در داخل
- بدون
- کارگر
- جهان
- نوشتن
- زفیرنت