برداشتن بافت سرطانی با جراحی یک درمان رایج است که برای کاهش احتمال گسترش سرطان به بافتهای سالم استفاده میشود. با این حال، اثربخشی چنین جراحی به شدت به توانایی جراح در تشخیص بافت سرطانی و سالم بستگی دارد.
مشخص است که فعالیت های متابولیک بافت سرطانی و سالم به طور قابل توجهی متفاوت است: بافت های سرطانی اغلب دارای جریان خون آشفته همراه با سطوح پایین اکسیژن یا هیپوکسی هستند. با توجه به نواحی هیپوکسیک رایج در بافت سرطانی، شناسایی دقیق هیپوکسی می تواند به تمایز بافت سرطانی از بافت سالم در طول جراحی کمک کند.
محققان از دانشکده مهندسی تایر در دارتموث و دانشگاه ویسکانسین مدیسون در حال بررسی استفاده از پروب های فلورسنت برای تصویربرداری بلادرنگ از غلظت موضعی اکسیژن در بافت در طول جراحی هستند. آنها یافته های خود را در مجله اپتیک زیست پزشکی.
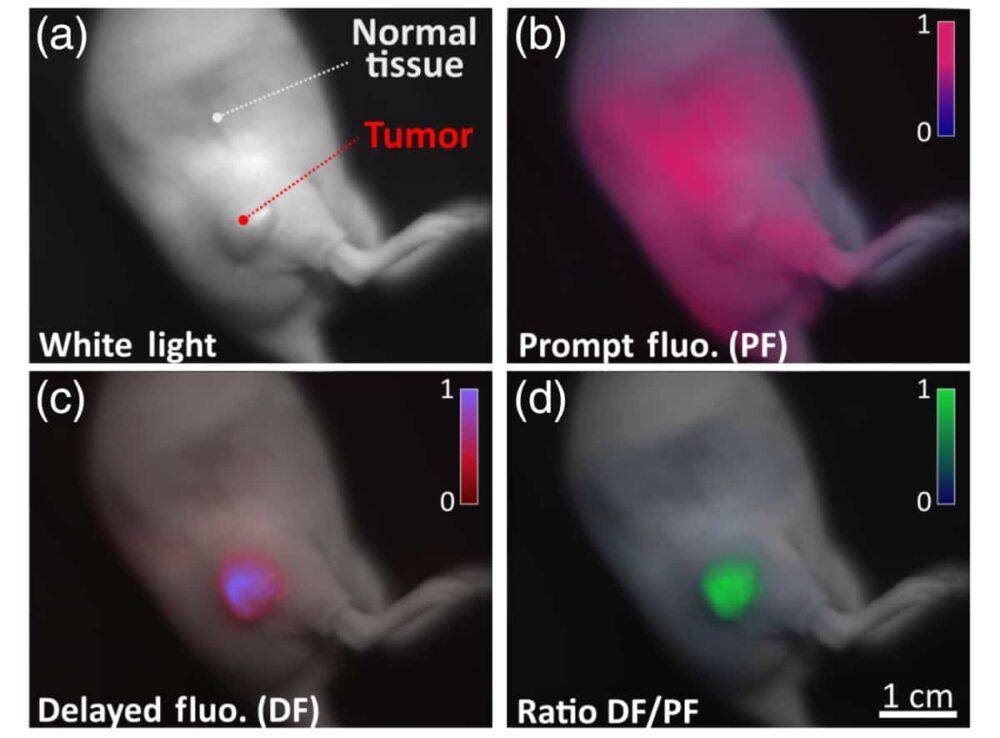
هنگامی که کاوشگرهای فلورسنت توسط نور برانگیخته می شوند، به حالت پایه باز می گردند و نور را با انرژی متفاوتی ساطع می کنند. بلافاصله پس از روشن شدن، کاوشگرها پالس نوری کوتاهی را منتشر می کنند که به عنوان فلورسانس سریع شناخته می شود. برخی از کاوشگرها نیز می توانند سیگنال فلورسانس تاخیری را مدتی پس از روشن شدن تولید کنند.
اگرچه سیگنالهای فلورسانس فوری و تاخیری در طول زمان تحلیل میروند، سیگنال فلورسانس سریع در مقایسه با واپاشی طولانیمدت فلورسانس تاخیری به سرعت تحلیل میرود. کاهش تاخیر سیگنال فلورسانس را می توان برای درک بهتر فعالیت متابولیک بافت مجاور مشاهده و تجزیه و تحلیل کرد.
ارزیابی اکسیژن رسانی در زمان واقعی
نویسنده اول آرتور پتوسو و همکاران از یک سیستم تصویربرداری نوری برای نظارت بر نور ساطع شده توسط پروب مولکولی درون زا پروتوپورفیرین IX (PpIX) در مدل موش سرطان پانکراس که در آن مناطق هیپوکسیک وجود دارد، استفاده کردند.

محققان PpIX را به عنوان یک پماد توپولوژیکی یا از طریق تزریق به پهلوی حیوان تجویز کردند و با استفاده از یک دیود لیزر مدوله شده 635 نانومتری به عنوان منبع تحریک، فلورسانس تولید کردند. آنها دریافتند که نسبت فلورسانس تاخیری به فلورسانس سریع با فشار جزئی اکسیژن موضعی در بافت نسبت معکوس دارد.
شدت ضعیف سیگنال فلورسانس تاخیری، تشخیص آن را از نظر فنی چالش برانگیز می کند. برای غلبه بر این موضوع، محققان از یک سیستم تصویربرداری با دریچه زمانی استفاده کردند که نظارت متوالی سیگنال فلورسانس را فقط در پنجره های زمانی کوچک امکان پذیر می کند. این آنها را قادر میسازد تا تشخیص نویز پسزمینه را کاهش دهند و تغییرات سیگنال فلورسانس تاخیری را بهطور دقیق نظارت کنند.
تجزیه و تحلیل بیشتر نشان داد که سیگنال فلورسانس تأخیری که از سلول های هیپوکسیک سرطانی به دست می آید، پنج برابر بیشتر از سیگنال فلورسانس به دست آمده از بافت سالم و دارای اکسیژن کافی است. علاوه بر این، تیم همچنین دریافت که سیگنال فلورسانس تاخیری را میتوان با لمس بافت (اعم از فشار به پوست در طول معاینه فیزیکی)، که هیپوکسی گذرا را افزایش میدهد و کنتراست زمانی بین دو سیگنال را امکانپذیر میکند، بیشتر تقویت کرد.
پتوسو می گوید: «از آنجایی که اکثر تومورها هیپوکسی میکرو ناحیه ای دارند، تصویربرداری سیگنال های هیپوکسی از فلورسانس تاخیری PpIX امکان کنتراست عالی بین بافت طبیعی و تومورها را فراهم می کند.
طیفسنجی چندوجهی تومورهای مغزی را تشخیص میدهد در داخل بدن
محققان به این نتیجه رسیدند که نظارت بر فلورسانس تاخیری ناشی از انتشار منحصر به فرد پروب فلورسنت PpIX در حضور هیپوکسی، مزایای متعددی در تشخیص بافت سالم و سرطانی در طول جراحی دارد. آنها می گویند: «دستیابی به فلورسانس سریع و تأخیر در یک چرخه متوالی سریع امکان تصویربرداری از سطح اکسیژن را به روشی مستقل از غلظت PpIX فراهم می کند.
فناوری ساده مورد نیاز، و قابلیت سرعت فریم سریع همراه با سمیت کم PpIX، این مکانیسم کنتراست را برای انسان قابل ترجمه می کند. پتوسئو ادعا می کند که می تواند در آینده به راحتی به عنوان یک مکانیسم کنتراست ذاتی برای هدایت جراحی انکولوژیک استفاده شود.