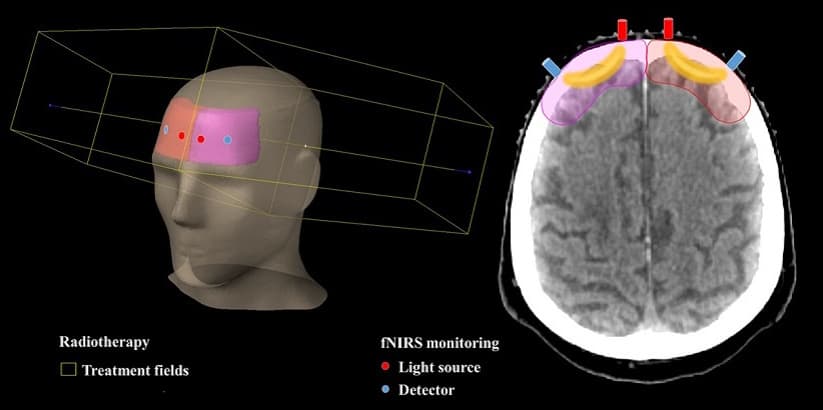
Verenvirtaus ja kasvainten hapen saanti muuttuvat muutaman ensimmäisen sädehoidon viikkojen aikana. Tutkijat uskovat tällä hetkellä, että uudelleenhapettuminen tapahtuu kasvaimen kutistumisen, vähentyneen hapenkulutuksen ja lisääntyneen perfuusion vuoksi. Lääkärit toivovat, että näitä ja muita mahdollisia muutoksia voitaisiin hyödyntää parantamaan potilaan vastetta sädehoitoon.
Mahdollisena askeleena kohti yksilöllisiä syöpähoitoja suomalaiset tutkijat käyttävät toiminnallista lähi-infrapunaspektroskopiaa (fNIRS) mittaamaan reaaliaikaista hemoglobiinipitoisuutta, joka on epäsuora kudosten hapetuksen indikaattori kokoaivojen sädehoidon aikana.
Teemu Myllylä mistä Oulun yliopisto johtaa fNIRS-tutkimusta yhteistyössä Juha Nikkinen, pääfyysikko sädehoidon kliinisen lääketieteellisen fysiikan divisioonassa Oulun yliopistollinen sairaala. Myllylä sanoo, että heidän tutkimustyönsä tavoitteena on soveltaa fNIRS:ää paikkaamaan joitakin aukkoja tiedossamme kudosten ja kasvainten hapettumisesta ja vasteesta sädehoidon aikana ja sen jälkeen.
Funktionaalista lähi-infrapunaspektroskopiaa on käytetty useiden vuosikymmenten ajan reaaliaikaisen aivojen toiminnan tutkimiseen vasteena erilaisiin ärsykkeisiin ja kognitiivisiin tehtäviin. Suhteellisen halvalla, kannettavalla ja ei-invasiivisella menetelmällä voidaan mitata aivojen hemodynamiikkaa jopa 2 cm:n syvyydestä aikuisen ihmisen aivoissa. FNIRS-laite mittaa infrapunavalon avulla reaaliaikaisia muutoksia hemoglobiinin alueellisissa pitoisuuksissa – korvike veren tilavuuden muutoksille ja sitä kautta hapen pääsylle kudoksiin – aivoissa.
Heidän äskettäisessä proof-of-concept -tutkimuksessaan, joka raportoi Journal of Biomedical OpticsTutkijat käyttivät fNIRS:ää hemoglobiinipitoisuuden mittaamiseen palliatiivisen kokoaivojen sädehoidon aikana. Ryhmä havaitsi lisääntynyttä verenkiertoa hoitojen aikana 10 potilaalla, joille tehtiin useita kokoaivojen säteilytyksiä. Mitään vaikutusta ei havaittu ennen säteilytystä tai säteilytyksen päättymisen jälkeen.
Tiimi kiinnitti moniaallonpituiseen fNIRS-laitteeseen kuituoptiset kärjet kohtisuoraan aivoihin nähden ja vahvisti, että ne eivät häirinneet säteilyn asetusta tai toimittamista. Säteilyannos annettiin käyttämällä staattisen kentän kokoaivojen sädehoitoa, joka käsitti kaksi vastakkaista 6 MV-kenttää. Eteenpäin suuntautuvaa intensiteettimoduloitua sädehoitoa, joka lisää pienempiä kenttiä samasta suunnasta kuin pääkentät, sovellettiin koko aivojen tasaisen annoksen peittämiseksi.
Koska NIRS-laite mittaa vain hemoglobiinin suhteellista pitoisuutta koko aivoissa, eri potilailla on erilaiset fNIRS-signaalin amplitudit. Tutkijat normalisoivat signaalin amplitudit suodattamalla fNIRS-signaalin erittäin matalalla taajuuskaistalla ja vähentämällä sitten signaalin säteilytyksen alussa kokonaisista vastaavista signaaleista. He käyttivät satojen terveiden yksilöiden lepotilatietoja kontrollitietoina.
Kasvainhypoksiaa seurataan reaaliajassa sädehoidon aikana
Ryhmä kerää nyt fNIRS-tietoja osallistujilta, joilla on kiinteitä kasvaimia yrittääkseen erottaa hemoglobiinipitoisuudet kasvaimessa ja terveessä kudoksessa ja tutkia kasvaimen vasteita säteilylle. He myös tutkivat, miksi he havaitsivat eroja kudosten hapettumisessa ensimmäisen ja toisen säteilytyksen välillä Journal of Biomedical Optics opiskella. Mahdollisia selityksiä ovat pienempi absorboitunut annos toisessa säteilytyksessä, monilehtinen kollimaattori tai muut mittausasetukset tai fysiologiset vasteet.
"[fNIRS]-tekniikka on helppo suorittaa kliinisissä olosuhteissa, eikä se käytännössä häiritse tai hidasta potilaille tehtäviä normaaleja sädehoitotoimenpiteitä", Myllylä sanoo. "FNIRS:n hyödyntäminen kliinisissä tilanteissa on suuri, koska se on turvallinen tekniikka ja sitä voidaan käyttää yhdessä käytännössä kaikkien tällä hetkellä käytettävien kliinisen neurokuvantamisen ja terapiatekniikoiden kanssa."
- SEO-pohjainen sisällön ja PR-jakelu. Vahvista jo tänään.
- Platoblockchain. Web3 Metaverse Intelligence. Tietoa laajennettu. Pääsy tästä.
- Lähde: https://physicsworld.com/a/real-time-monitoring-of-brain-tissue-oxygenation-could-personalize-radiotherapy/
- :On
- $ YLÖS
- 1
- 10
- 28
- a
- toiminta
- Lisää
- Aikuinen
- Jälkeen
- AL
- Kaikki
- ja
- sovellettu
- käyttää
- lähestymistapa
- OVAT
- AS
- At
- Bändi
- BE
- koska
- ennen
- alkaa
- Alku
- Uskoa
- välillä
- biolääketieteen
- veri
- Aivot
- Aivojen toimintaa
- by
- CAN
- Syöpä
- muuttaa
- Muutokset
- päällikkö
- napsauttaa
- Kliininen
- kliinikot
- lähellä
- kognitiivinen
- yhteistyö
- Kerääminen
- yhdistelmä
- Sisältää
- keskittyminen
- CONFIRMED
- kulutus
- ohjaus
- vastaava
- voisi
- kattavuus
- Tällä hetkellä
- tiedot
- vuosikymmeninä
- syvä
- toimitettu
- toimitus
- laite
- DID
- erot
- eri
- eriyttää
- suunta
- Divisioona
- alas
- aikana
- vaikutus
- vaikutukset
- Koko
- Käyttää hyväkseen
- hyödynnetään
- laajentaminen
- harvat
- ala
- Fields
- suodatus
- Suomi
- Etunimi
- virtaus
- varten
- alkaen
- koko
- toiminnallinen
- saada
- tavoite
- Olla
- terve
- Korkea
- toivoa
- Miten
- HTTPS
- ihmisen
- Sadat
- kuva
- Imaging
- parantaa
- in
- sisältää
- kasvoi
- Osoitin
- henkilöt
- tiedot
- häiritä
- kysymys
- IT
- jpg
- tuntemus
- Liidit
- tasot
- valo
- tärkein
- max-width
- mitata
- toimenpiteet
- lääketieteellinen
- Lääketieteellinen fysiikka
- ehkä
- seuranta
- moninkertainen
- normaali
- of
- on
- avata
- optiikka
- Muut
- Happi
- osallistujat
- potilas
- potilaat
- Suorittaa
- Personoida
- yksilöllinen
- Fysiikka
- Platon
- Platonin tietotieto
- PlatonData
- mahdollinen
- mahdollinen
- käytännössä
- menettelyt
- toimittaa
- Sädehoito
- todellinen
- reaaliaikainen
- vastaanottaa
- äskettäinen
- alueellinen
- suhteellisesti
- raportoitu
- tutkimus
- Tutkijat
- vastaus
- turvallista
- sama
- sanoo
- tutkijat
- Toinen
- settings
- setup
- useat
- signaali
- signaalit
- tilanteita
- hidas
- pienempiä
- vankka
- jonkin verran
- Spektroskopia
- Osavaltio
- Vaihe
- opinnot
- tutkimus
- toimittaa
- tehtävät
- joukkue-
- tekniikat
- Elektroniikka
- että
- -
- heidän
- Nämä
- kauttaaltaan
- thumbnail
- aika
- vinkit
- että
- kohti
- Seuranta
- totta
- yliopisto
- tilavuus
- viikkoa
- HYVIN
- joka
- koko
- with
- zephyrnet