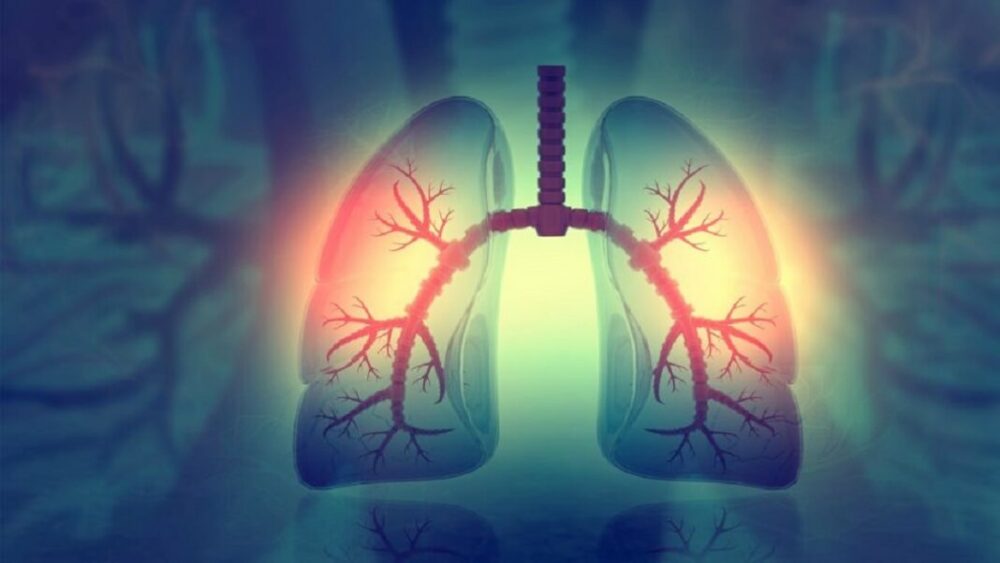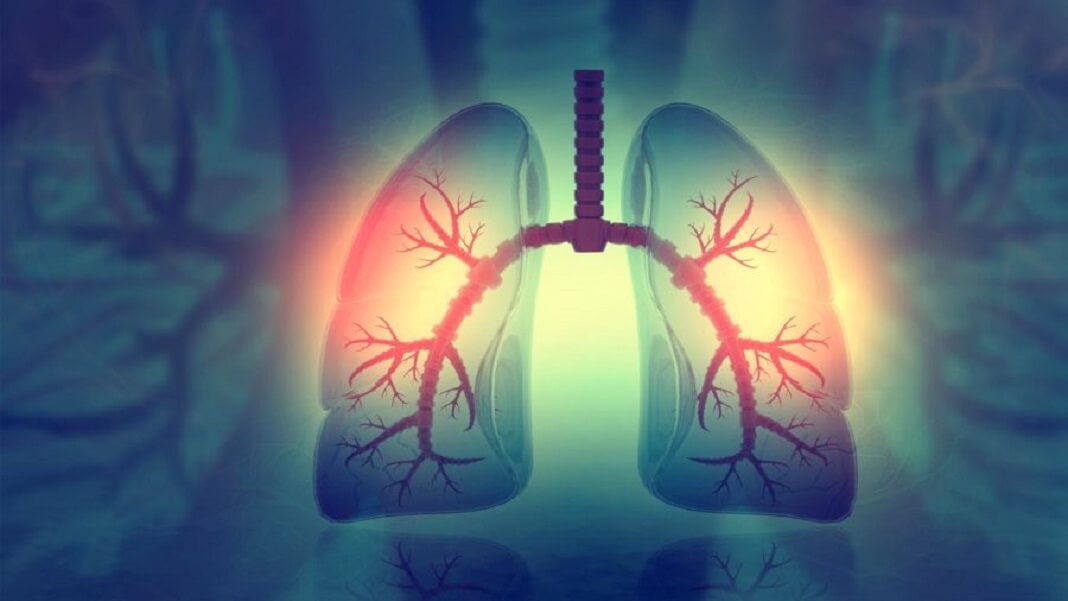
कोविड-19 के बाद से हम सभी फेफड़ों के स्वास्थ्य के बारे में अधिक जागरूक हो गए हैं।
हालाँकि, अस्थमा और क्रॉनिक ऑब्सट्रक्टिव पल्मोनरी डिजीज (सीओपीडी) से पीड़ित लोगों के लिए फेफड़ों की समस्याओं से निपटना जीवन भर का संघर्ष है। सीओपीडी वाले लोग अत्यधिक सूजन वाले फेफड़ों के ऊतकों से पीड़ित होते हैं जो वायुमार्ग में सूजन और बाधा उत्पन्न करते हैं, जिससे सांस लेना मुश्किल हो जाता है। यह बीमारी आम है, अकेले अमेरिका में इसके सालाना तीन मिलियन से अधिक मामले सामने आते हैं।
हालांकि प्रबंधन योग्य है, इसका कोई इलाज नहीं है। एक समस्या यह है कि सीओपीडी वाले फेफड़े बहुत सारा चिपचिपा बलगम बाहर निकालते हैं, जो उपचार को फेफड़ों की कोशिकाओं तक पहुंचने से रोकने में बाधा उत्पन्न करता है। चिपचिपा पदार्थ - जब खांसी से बाहर नहीं निकाला जाता - बैक्टीरिया को भी आकर्षित करता है, जिससे स्थिति और बिगड़ जाती है।
एक नए अध्ययन से in विज्ञान अग्रिम एक संभावित समाधान का वर्णन करता है। वैज्ञानिकों ने फेफड़ों में एंटीबायोटिक्स पहुंचाने के लिए एक नैनोकैरियर विकसित किया है। एक जैविक अंतरिक्ष यान की तरह, वाहक के पास "दरवाजे" होते हैं जो संक्रमण से लड़ने के लिए बलगम परत के अंदर एंटीबायोटिक्स खोलते हैं और छोड़ते हैं।
"दरवाजे" स्वयं भी घातक हैं। एक छोटे प्रोटीन से बने, वे बैक्टीरिया की झिल्लियों को तोड़ते हैं और फेफड़ों की कोशिकाओं को पुराने संक्रमण से मुक्त करने के लिए उनके डीएनए को साफ करते हैं।
टीम ने नैनोकैरियर का उपयोग करके एंटीबायोटिक का एक इनहेलेबल संस्करण तैयार किया। सीओपीडी के एक चूहे के मॉडल में, उपचार ने केवल तीन दिनों में उनके फेफड़ों की कोशिकाओं को पुनर्जीवित कर दिया। उनके रक्त में ऑक्सीजन का स्तर सामान्य हो गया, और फेफड़ों की क्षति के पिछले लक्षण धीरे-धीरे ठीक हो गए।
टीम ने कहा, "यह इम्यूनोएंटीबैक्टीरियल रणनीति सीओपीडी प्रबंधन के वर्तमान प्रतिमान को बदल सकती है।" लिखा था लेख में।
मुझे सांस लेने दें
फेफड़े बेहद नाजुक होते हैं. शरीर में ऑक्सीजन के प्रवाह को समन्वित करने में मदद करने के लिए लोबों में विभाजित कोशिकाओं की पतली लेकिन लचीली परतों का चित्र बनाएं। एक बार जब वायु श्वासनली से प्रवाहित होती है, तो यह तेजी से शाखाओं के एक जटिल नेटवर्क में फैल जाती है, जिससे हजारों वायु थैलियाँ भर जाती हैं जो शरीर को कार्बन डाइऑक्साइड से मुक्त करते हुए ऑक्सीजन की आपूर्ति करती हैं।
ये संरचनाएं आसानी से क्षतिग्रस्त हो जाती हैं, और धूम्रपान एक आम ट्रिगर है। सिगरेट के धुएं के कारण आसपास की कोशिकाएं एक चिपचिपा पदार्थ बाहर निकालती हैं जो वायुमार्ग को बाधित करता है और वायुकोशों को ढक देता है, जिससे उनके लिए सामान्य रूप से कार्य करना मुश्किल हो जाता है।
समय के साथ, बलगम एक प्रकार का "गोंद" बनाता है जो बैक्टीरिया को आकर्षित करता है और बायोफिल्म में संघनित हो जाता है। यह अवरोध ऑक्सीजन के आदान-प्रदान को और अवरुद्ध कर देता है और फेफड़ों के वातावरण को बैक्टीरिया के विकास के लिए अनुकूल वातावरण में बदल देता है।
गिरावट को रोकने का एक तरीका बैक्टीरिया को ख़त्म करना है। ब्रॉड-स्पेक्ट्रम एंटीबायोटिक्स सबसे व्यापक रूप से इस्तेमाल किया जाने वाला उपचार है। लेकिन चिपचिपी सुरक्षात्मक परत के कारण, वे फेफड़ों के ऊतकों के अंदर गहराई तक बैक्टीरिया तक आसानी से नहीं पहुंच पाते हैं। इससे भी बदतर, लंबे समय तक उपचार से एंटीबायोटिक प्रतिरोध की संभावना बढ़ जाती है, जिससे जिद्दी बैक्टीरिया को खत्म करना और भी मुश्किल हो जाता है।
लेकिन सुरक्षात्मक परत में एक कमज़ोरी है: यह थोड़ी ज़्यादा खट्टी है। अक्षरशः।
खुले द्वार की नीति
नींबू की तरह, चिपचिपी परत स्वस्थ फेफड़ों के ऊतकों की तुलना में थोड़ी अधिक अम्लीय होती है। इस विचित्रता ने टीम को एक आदर्श एंटीबायोटिक वाहक का विचार दिया जो केवल अम्लीय वातावरण में अपना पेलोड जारी करेगा।
टीम ने सिलिका से खोखले नैनोकण बनाए - एक लचीला बायोमटेरियल - उन्हें एक सामान्य एंटीबायोटिक से भर दिया, और दवाओं को जारी करने के लिए "दरवाजे" जोड़े।
इन छिद्रों को अतिरिक्त लघु प्रोटीन अनुक्रमों द्वारा नियंत्रित किया जाता है जो "ताले" की तरह काम करते हैं। सामान्य वायुमार्ग और फेफड़ों के वातावरण में, वे दरवाजे पर मुड़ जाते हैं, अनिवार्य रूप से एंटीबायोटिक दवाओं को बुलबुले के अंदर जमा कर लेते हैं।
सीओपीडी के साथ फेफड़ों में जारी, स्थानीय अम्लता लॉक प्रोटीन की संरचना को बदल देती है, इसलिए दरवाजे खुलते हैं और एंटीबायोटिक दवाओं को सीधे बलगम और बायोफिल्म में छोड़ते हैं - अनिवार्य रूप से बैक्टीरिया की सुरक्षा को तोड़ते हैं और उन्हें उनके घरेलू मैदान पर लक्षित करते हैं।
मिश्रण के साथ एक परीक्षण पेट्री डिश में प्रयोगशाला में विकसित बायोफिल्म में प्रवेश कर गया। यह पिछले प्रकार के नैनोकणों की तुलना में कहीं अधिक प्रभावी था, मुख्यतः क्योंकि वाहक के दरवाजे बायोफिल्म के अंदर एक बार खुलते थे - अन्य नैनोकणों में, एंटीबायोटिक्स फंसे रहते थे।
वाहक संक्रमित क्षेत्रों में भी गहरी खुदाई कर सकते हैं। कोशिकाओं में विद्युत आवेश होते हैं। वाहक और बलगम दोनों में नकारात्मक चार्ज होते हैं, जो - दो चुम्बकों के समान रूप से चार्ज किए गए सिरों की तरह - वाहक को बलगम और बायोफिल्म परतों के अंदर और अंदर धकेलते हैं।
रास्ते में, बलगम की अम्लता धीरे-धीरे वाहक के चार्ज को सकारात्मक में बदल देती है, ताकि एक बार बायोफिल्म के बाद, "लॉक" तंत्र खुल जाए और दवा जारी हो जाए।
टीम ने नैनोकणों की बैक्टीरिया को ख़त्म करने की क्षमता का भी परीक्षण किया। एक डिश में, उन्होंने कई सामान्य प्रकार के संक्रामक बैक्टीरिया को मिटा दिया और उनके बायोफिल्म को नष्ट कर दिया। उपचार अपेक्षाकृत सुरक्षित प्रतीत हुआ। एक डिश में मानव भ्रूण के फेफड़ों की कोशिकाओं के परीक्षण में विषाक्तता के न्यूनतम लक्षण पाए गए।
हैरानी की बात यह है कि वाहक स्वयं भी बैक्टीरिया को नष्ट कर सकता है। अम्लीय वातावरण के अंदर, इसके सकारात्मक चार्ज ने बैक्टीरिया की झिल्लियों को तोड़ दिया। फूटे हुए गुब्बारों की तरह, कीड़ों ने अपने परिवेश में आनुवंशिक सामग्री छोड़ी, जिसे वाहक ने उड़ा लिया।
आग बुझाना
फेफड़ों में जीवाणु संक्रमण अतिसक्रिय प्रतिरक्षा कोशिकाओं को आकर्षित करता है, जिससे सूजन हो जाती है। वायुकोशों के आसपास की रक्त वाहिकाएं भी पारगम्य हो जाती हैं, जिससे खतरनाक अणुओं का प्रवेश आसान हो जाता है। ये परिवर्तन सूजन का कारण बनते हैं, जिससे सांस लेना मुश्किल हो जाता है।
सीओपीडी के एक माउस मॉडल में, साँस लेने योग्य नैनोकण उपचार ने अति सक्रिय प्रतिरक्षा प्रणाली को शांत कर दिया। कई प्रकार की प्रतिरक्षा कोशिकाएं सक्रियण के स्वस्थ स्तर पर लौट आईं - जिससे चूहों को अत्यधिक सूजन वाली प्रोफ़ाइल से संक्रमण और सूजन से लड़ने वाली प्रोफ़ाइल पर स्विच करने की अनुमति मिली।
जिन चूहों को इनहेलेबल नैनोपार्टिकल से इलाज किया गया, उनके फेफड़ों में लगभग 98 प्रतिशत कम बैक्टीरिया थे, उन चूहों की तुलना में जिन्हें वाहक के बिना वही एंटीबायोटिक दिया गया था।
बैक्टीरिया ख़त्म होने से चूहों को राहत की सांस मिली। उन्होंने आसानी से सांस ली. उनके रक्त में ऑक्सीजन का स्तर बढ़ गया, और रक्त अम्लता - जो खतरनाक रूप से कम ऑक्सीजन का संकेत है - सामान्य हो गई।
माइक्रोस्कोप के तहत, इलाज किए गए फेफड़ों ने सामान्य संरचनाओं को बहाल किया, मजबूत वायु थैलियों के साथ जो धीरे-धीरे सीओपीडी क्षति से उबर गए। उपचारित चूहों के फेफड़ों में तरल पदार्थ जमा होने के कारण सूजन भी कम हुई, जो आमतौर पर फेफड़ों की चोटों में देखी जाती है।
परिणाम, आशाजनक होते हुए भी, केवल चूहों में धूम्रपान से संबंधित सीओपीडी मॉडल के लिए हैं। उपचार के दीर्घकालिक परिणामों के बारे में अभी भी हम बहुत कुछ नहीं जानते हैं।
हालाँकि अभी तक साइड इफेक्ट के कोई संकेत नहीं थे, लेकिन यह संभव है कि नैनोकण समय के साथ फेफड़ों के अंदर जमा हो सकते हैं और अंततः नुकसान पहुंचा सकते हैं। और यद्यपि वाहक स्वयं जीवाणु झिल्ली को नुकसान पहुंचाता है, उपचार ज्यादातर इनकैप्सुलेटेड एंटीबायोटिक पर निर्भर करता है। साथ एंटीबायोटिक प्रतिरोध वृद्धि के साथ, सीओपीडी के लिए कुछ दवाएं पहले से ही अपना प्रभाव खो रही हैं।
फिर समय के साथ यांत्रिक क्षति की संभावना रहती है। सिलिकॉन-आधारित नैनोकणों को बार-बार अंदर लेने से लंबे समय में फेफड़े खराब हो सकते हैं। इसलिए, जबकि नैनोकण सीओपीडी प्रबंधन के लिए रणनीतियों को बदल सकते हैं, यह स्पष्ट है कि हमें अनुवर्ती अध्ययन की आवश्यकता है, टीम ने लिखा।
छवि क्रेडिट: क्रिस्टल प्रकाश / Shutterstock.com
- एसईओ संचालित सामग्री और पीआर वितरण। आज ही प्रवर्धित हो जाओ।
- प्लेटोडेटा.नेटवर्क वर्टिकल जेनरेटिव एआई। स्वयं को शक्तिवान बनाएं। यहां पहुंचें।
- प्लेटोआईस्ट्रीम। Web3 इंटेलिजेंस। ज्ञान प्रवर्धित। यहां पहुंचें।
- प्लेटोईएसजी. कार्बन, क्लीनटेक, ऊर्जा, पर्यावरण, सौर, कचरा प्रबंधन। यहां पहुंचें।
- प्लेटोहेल्थ। बायोटेक और क्लिनिकल परीक्षण इंटेलिजेंस। यहां पहुंचें।
- स्रोत: https://singularityhub.com/2024/02/12/an-antibiotic-you-inhale-can-deliver-medication-deep-into-the-lungs/
- :हैस
- :है
- :नहीं
- $यूपी
- 98
- a
- क्षमता
- About
- संचय करें
- जोड़ा
- अतिरिक्त
- आकाशवाणी
- वायुमार्ग
- सब
- अकेला
- पहले ही
- भी
- के बीच में
- an
- और
- वार्षिक
- अलग
- छपी
- हैं
- क्षेत्रों के बारे में जानकारी का उपयोग करके ट्रेडिंग कर सकते हैं।
- लेख
- At
- आकर्षित
- को आकर्षित करती है
- जागरूक
- बैक्टीरिया
- अवरोध
- क्योंकि
- बन
- किया गया
- बिट
- ब्लॉक
- रक्त
- परिवर्तन
- के छात्रों
- शाखाएं
- तोड़कर
- सांस
- तोड़ दिया
- बुलबुला
- कीड़े
- बनाता है
- लेकिन
- by
- कर सकते हैं
- कार्बन
- कार्बन डाइआक्साइड
- वाहक
- मामलों
- कारण
- का कारण बनता है
- के कारण
- कोशिकाओं
- संयोग
- परिवर्तन
- प्रभार
- आरोप लगाया
- प्रभार
- स्वच्छ
- स्पष्ट
- सामान्य
- सामान्यतः
- तुलना
- जटिल
- मनगढ़ंत कहानी
- शर्त
- Consequences
- नियंत्रित
- समन्वय
- सका
- COVID -19
- श्रेय
- इलाज
- वर्तमान
- क्षति
- खतरनाक
- दिन
- व्यवहार
- गहरा
- और गहरा
- गढ़
- उद्धार
- वर्णन करता है
- को नष्ट
- नष्ट
- विकसित
- मुश्किल
- डीआईजी
- सीधे
- रोग
- थाली
- श्रीमती
- dont
- द्वारा
- दरवाजे
- नीचे
- नीचे
- औषध
- आसान
- आसानी
- प्रभाव
- प्रभावी
- प्रभाव
- समझाया
- समाप्त होता है
- इंजीनियर
- वातावरण
- वातावरण
- अनिवार्य
- और भी
- अंत में
- एक्सचेंज
- अत्यंत
- दूर
- अनुकूल
- लड़ाई
- भरने
- लचीला
- प्रवाह
- प्रवाह
- तरल पदार्थ
- के लिए
- रूपों
- पाया
- से
- समारोह
- आगे
- दे दिया
- आनुवंशिक
- मिल
- दी
- विकास
- था
- कठिन
- है
- स्वास्थ्य
- स्वस्थ
- मदद
- अत्यधिक
- होम
- HTTPS
- मानव
- विचार
- आदर्श
- प्रतिरक्षा
- इम्यून सिस्टम
- in
- बढ़ जाती है
- संक्रमित
- संक्रमणों
- संक्रामक
- अंदर
- में
- IT
- आईटी इस
- खुद
- जेपीजी
- केवल
- जानना
- बड़े पैमाने पर
- परत
- परतों
- बिक्रीसूत्र
- कम
- स्तर
- स्तर
- जीवन भर
- पसंद
- थोड़ा
- स्थानीय
- ताला
- लंबा
- लंबे समय तक
- हार
- निम्न
- बनाया गया
- निर्माण
- प्रबंधनीय
- प्रबंध
- सामग्री
- मई..
- यांत्रिक
- तंत्र
- इलाज
- माइक्रोस्कोप
- दस लाख
- कम से कम
- आदर्श
- अधिक
- अधिकांश
- अधिकतर
- बहुत
- कफ
- विभिन्न
- आवश्यकता
- नकारात्मक
- नेटवर्क
- नया
- नहीं
- साधारण
- सामान्य रूप से
- अभी
- of
- on
- एक बार
- ONE
- केवल
- खुला
- खोला
- उद्घाटन
- खोलता है
- अन्य
- आउट
- के ऊपर
- ऑक्सीजन
- मिसाल
- अतीत
- स्टाफ़
- प्रतिशत
- चित्र
- प्लेटो
- प्लेटो डेटा इंटेलिजेंस
- प्लेटोडाटा
- सकारात्मक
- संभव
- संभावित
- रोकने
- पिछला
- मुसीबत
- समस्याओं
- प्रोफाइल
- होनहार
- रक्षात्मक
- प्रोटीन
- पंप
- तेजी
- पहुंच
- तक पहुंच गया
- अपेक्षाकृत
- और
- रिहा
- विज्ञप्ति
- राहत
- बने रहे
- बार बार
- प्रतिरोध
- परिणाम
- छुटकारा
- वृद्धि
- सुरक्षित
- वही
- विज्ञान
- वैज्ञानिकों
- देखा
- पाली
- कम
- Shutterstock
- पक्ष
- हस्ताक्षर
- लक्षण
- उसी प्रकार
- के बाद से
- धीरे से
- छोटा
- धुआं
- So
- समाधान
- कुछ
- कुंडली
- फिर भी
- रुकें
- रणनीतियों
- स्ट्रेटेजी
- संरचना
- संरचनाओं
- संघर्ष
- पढ़ाई
- पदार्थ
- आपूर्ति
- आसपास के
- स्विच
- प्रणाली
- को लक्षित
- टीम
- अवधि
- परीक्षण
- परीक्षण किया
- परीक्षण
- से
- कि
- RSI
- लेकिन हाल ही
- उन
- अपने
- चिकित्सा
- वहाँ।
- इन
- वे
- पतला
- इसका
- उन
- हालांकि?
- हजारों
- तीन
- यहाँ
- पहर
- सेवा मेरे
- टन
- भी
- फंस गया
- इलाज किया
- उपचार
- उपचार
- ट्रिगर
- दो
- टाइप
- प्रकार
- us
- प्रयुक्त
- का उपयोग
- संस्करण
- था
- मार्ग..
- we
- दुर्बलता
- चला गया
- थे
- कौन कौन से
- जब
- व्यापक रूप से
- पोंछ
- साथ में
- बिना
- काम
- बदतर
- होगा
- लिखा था
- आप
- जेफिरनेट