Az új rákterápia a mennyben teremtett gyufa.
Az egyik oldalon a CRISPR, az a génszerkesztő technológia, amely a géntechnológiát viharba ejtette. A másik a CAR-T nevű terápia, amely a normál immunsejteket szuperkatonákká alakítja, amelyek specifikus rákokra vadásznak.
A tudósok régóta arra törekedtek, hogy ezt a két nagy előrelépést a rákos megbetegedések „veszélyeztetési zónájában” egyesítsék – egy cellás vadászrepülőgéppel, amely precíz rákos sejteket vadászik le, és eláll a köhögéstől a lélegzetüktől. (Top Gun, valaki?)
Az ötlet viszonylag egyszerű: a CAR-T géntechnológiát alkalmaz, hogy az immunsejteket fejlett nyomkövetési képességekkel ruházza fel, amelyek egy bizonyos típusú ráktípust céloznak meg. A CRISPR az az eszköz, amely beilleszti a nyomkövető géneket az immunsejtekbe.
De gyakorlatilag a duó a „legbonyolultabb terápia valaha”.
A genetikai módosításokat úgy alakították ki, hogy megtámadják az ember saját rákját, és minden egyes daganatát egy meghatározott fehérjekészlet tarkítja. Most a Nature tanulmányában a Los Angeles-i Kaliforniai Egyetemen dolgozó csapat 16 különböző rákos megbetegedésben, például mell- vagy vastagbélrákban szenvedő embernél tesztelte a kezelést. Egy egyedi algoritmus segítségével a tudósok genetikailag módosított immunsejtekből álló brigádot terveztek, hogy megcélozzák és megsemmisítsék minden egyes ember bizonyos típusú rákját. Ezek a sejtek személyre szabott fehérjecélpontokhoz juthatnak, miközben kímélik az egészséges szöveteket.
A csapat heteken belül azt találta, hogy a módosított immunsejtek annyira benyúltak a rákos szövetekbe, hogy a módosított sejtek a rákos minta 20 százalékát tették ki. Ez nem egy ezüstgolyó – ez az első próba csak a biztonság felmérésére szolgál. De ez azt mutatja, hogy a CRISPR és a CAR-T összefogása megvalósítható rákos betegeknél. A tanulmány az első lépés a jelenlegi rákkezelések potenciális felülvizsgálata felé, személyesebbé és hatékonyabbá téve azokat, és kevesebb mellékhatást okozva.
"Valószínűleg ez a legbonyolultabb terápia, amelyet a klinikán valaha is kipróbáltak" - mondta Dr. Antoni Ribas, a tanulmány szerzője, a Los Angeles-i Kaliforniai Egyetem munkatársa. "Megpróbálunk hadsereget alkotni a páciens saját T-sejtjéből."
A rák dilemma
A rákos sejtek rendkívül okosak.
Mint minden sejt, a rákos sejtek membránjukon kívül fehérjeköpennyel vannak tarkítva. Egyes fehérjék egészséges sejtként álcázzák őket. Mások odaadják őket. A rákos sejtek felszámolásának fő célja az, hogy ezekben az egyedülálló rákfehérje „jelzőfényekben” találkozzon, amelyek nincsenek jelen az egészséges sejtekben. Ez lehetővé teszi a rákos megbetegedések kiirtását, miközben a normális sejteket magára hagyja.
A kemoterápiától az immunterápiáig jó eredményeket értünk el a daganatok megcélzásában. Kétségtelen, hogy a kezelések életeket mentettek meg. De a terápiák a szervezetet is drasztikusan megviselik, főként azért, mert nem tudják megkülönböztetni a rákot más gyorsan növekvő sejtektől, például az őssejtektől.
„Azoknál a betegeknél, akiket a klinikán látunk rákos betegeknél, az immunrendszer valamikor elvesztette a csatát, és a daganat nőtt” – mondta Dr. Stephanie Mandl, a tanulmány szerzője, a kaliforniai dél-san franciscói PACT Pharma tudományos igazgatója.
Szóval mit csináljunk? Írja be a T cellát.
"Az emberi immunrendszer egyedülállóan alkalmas" a rákos megbetegedések felszámolására, miközben más sejteket megkímél - mondta a csapat. A T-sejtek, az immunrendszer részei, különösen jó gyilkosok, amelyek a T-sejt-receptornak vagy TCR-nek nevezett „spyglass” fehérje segítségével képesek levadászni a rákot. Gondoljon a TCR-re a végső biológiai megfigyelő kamerára: egyetlen DNS-mutációt képes észlelni, amely egy sejt rákos fordulatát jelzi.
A probléma az, hogy ezek az immunsejtek könnyen túlterheltek: a rákos megbetegedések több mint 24,000 XNUMX különböző mutációja miatt a T-sejtek nem tudnak lépést tartani mindegyikkel. A CAR-T egy módja annak, hogy fokozzák képességüket specifikus mutációk felismerésére. A „neoantigéneknek” nevezett fehérjék a rákos sejteket lobogtatják, mivel a normál sejtekben nincsenek jelen. Fordítás? A neoantigének tökéletes célpontjai a CAR-T-nek.
A vadászat kezdődik
A csapat minden betegtől két mintával indult: az egyik a daganatból, a másik a vérből. Furcsán hangzik, de a vérsejtek normál genetikai adatok „üres lapját” szolgáltatták háttérként, amely alapján a kutatók levadászhatták a mutált géneket egy rákmintában. Az eredmény meglepően sok mutációt eredményezett, egyes betegeknél akár 500-at is.
„A mutációk minden rák esetében eltérőek” – mondta Ribas.
Az adatok birtokában a csapat egy algoritmust használt, hogy több lehetséges CAR-T terápiás célpontot – a neoantigéneket vagy neoTCR-eket – tervezzen meg. Mindegyiket kifejezetten a T-sejtes támadás kiváltására választották ki, végül egy CAR-T-csapatot hoztak létre több mint 175 új rákos sejtfehérje célponttal.
Bár ez kockázatos üzlet. A CAR-T átírása a szervezet immunrendszere, ami súlyos mellékhatásokhoz vezethet. A csapat jól tudja: először egészséges donor T-sejtekben tesztelték a neoTCR jelölteket Petri-csészékben, hogy végül betegenként három rákos célpontot határozhassanak meg. Más szavakkal, minden beteg T-sejtjeit úgy alakították ki, hogy három rákhelyet célozzanak meg.
Írja be a CRISPR-t. A csapat minden betegtől vért vett, és izolálta a T-sejtjeit. Ezután a sejteket CRISPR-rel kezelték, hogy kiirtsák két immunrendszerrel kapcsolatos gént, és beillesztették azokat, amelyek a neoTCR-eket kódolják. Ez egy biológiai csali és kapcsoló: az újonnan bekapcsolt CAR-T-k elméletileg elhivatott rákvadászok, amelyek nem károsítják a normál sejteket.
Összességében ez egy elég gyors folyamat volt: a csapat mindössze 11 nap alatt növelte a szuperkatonasejtek számát. Miután a betegek gyógyszert szedtek, hogy korlátozzák normális immunsejtszámukat, a csapat bejuttatott szervezetükbe a mesterséges rákellenes sejteket. Több vérvételt követően a csapat azt találta, hogy nagy mennyiségű szerkesztett sejt kering a vérükben, és az egyes daganatok körül fészkelődött.
Szilárd Út
A próba főként a biztonság felmérésére irányult. De úgy tűnt, hogy a betegek hasznot húznak belőle. Egy hónappal az infúzió után öt ember rákja stabilizálódott – vagyis nem nőtt a daganat –, és csak ketten tapasztaltak immunmellékhatásokat a kezelés hatására.
„Ez a tanulmány… fontos, mivel az első humán kísérlet szilárd rákos megbetegedéseken, amely olyan betegspecifikus, CRISPR által tervezett T-sejtek használatát mutatja be, amelyek képesek azonosítani a specifikus antigéneket vagy „jelzőket” a páciens daganatsejtjein, és arra késztetik őket, hogy megöljenek. őket” – mondta Dr. Astero Klampatsa, a londoni Rákkutató Intézet munkatársa, aki nem vett részt a vizsgálatban.
Noha a CAR-T óriási sikert aratott a vérdaganatok kezelésében, a technológia nehézségekbe ütközött, amikor a legtöbb daganatos megbetegedést, például a mell-, tüdő- vagy gyomorrák szilárd daganatait hozzuk létre.
A tanulmány nem mutatja be a végső gyógymódot. Egy beteg immunreakciót váltott ki lázzal és a fehérvérsejtek elvesztésével. Egy másikuk átmeneti agygyulladást tapasztalt, ami járási és írási problémákhoz vezetett, de a kezelés hatására gyorsan felépültek. És bár a mesterségesen kialakított T-sejtek magas szintje korrelált néhány, de nem mindegyik rákkal, amelyek mérete csökkent, a terápia hogyan segítheti elő a hosszú távú gyógyulást, még nem ismert.
Ennek ellenére egyelőre bizakodó a csapat.
A CRISPRed CAR-T-ek következő generációjára tekintve a csapat olyan sejteket képzel el, amelyek metabolikusan életre kelnek, miközben a közelben daganat nő, figyelmeztetve a szervezetet egy lehetséges rákra. Egy másik ötlet a genetikailag továbbfejlesztett sejtek védelme a rákos hadviselés ellen. A daganatsejtek olyan jeleket küldhetnek ki, amelyek elnyomják az immunsejteket – egy genetikai gát előnyhöz juttathat bennünket, lehetővé téve, hogy a módosított sejtek tovább tartsanak, miközben a rák jeleit keresve járőröznek a szervezetben.
Ezek olyan ötletek, amelyeken a csapat dolgozik. De egyelőre "érdekes lenne látni, hogy ezt a terápiát egy nagyobb kísérletben alkalmazzák-e, ahol a hatékonyságot, de a kísérleti protokollokat is tovább lehet tesztelni" - mondta Klampatsa.
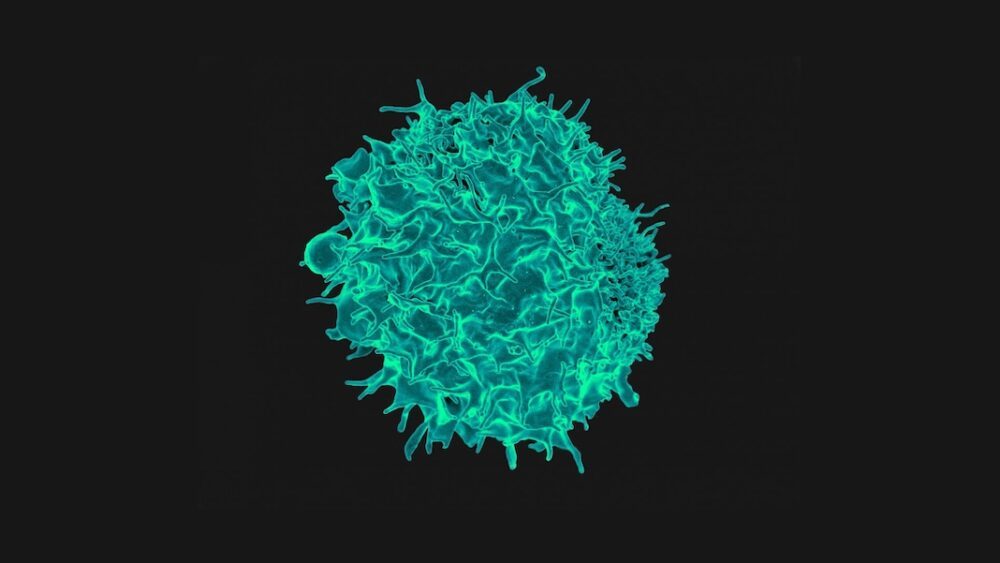
Kép: Egy T-sejt színes pásztázó elektronmikroszkópos felvétele. NIAD