תעתיק מרחבי ופרוטאומיקה מספקים מידע משלים ששינה את ההבנה שלנו לגבי תהליכים ביולוגיים מורכבים. עם זאת, שילוב ניסיוני של שיטות אלה מוגבל.
שיטה חדשה בשם Spatial Protein and Transcriptome Sequencing (SPOTS) יכולה להאיר את הזהויות והפעילויות של תאים ברחבי איבר או גידול ברזולוציה חסרת תקדים. פותח על ידי חוקרים ב רפואה וייל קורנל, NewYork-Presbyterian ומרכז הגנום של ניו יורק, SPOTS יכולים להאיר את הזהויות והפעילויות של תאים ברחבי איבר או גידול ברזולוציה חסרת תקדים.
הטכניקה שומרת מידע על המיקומים המדויקים של התאים תוך רישום דפוסי פעילות גנים ונוכחות חיוניים חלבונים בתאים על פני דגימות רקמה. זה מאפשר ליצור "מפות" מורכבות, עשירות בנתונים, של איברים, כולל איברים חולים וגידולים, מה שעשוי להועיל מאוד במחקר בסיסי וקליני כאחד.
מחבר שותף בכיר במחקר ד"ר דן לנדאו, פרופסור חבר לרפואה בחטיבה להמטולוגיה ואונקולוגיה רפואית וחבר במרכז הסרטן של סנדרה ואדוארד מאייר ב-Weill Cornell Medicine וחבר סגל ליבה במרכז הגנום של ניו יורק, אמר, "טכנולוגיה זו מרגשת כי היא מאפשרת לנו למפות את הארגון המרחבי של רקמות, כולל סוגי תאים, פעילויות תאים ואינטראקציות תא לתא, כפי שלא היה מעולם".
הגישה החדשה היא חלק מיוזמה גדולה יותר של מדענים ומהנדסים ליצור אמצעים יעילים יותר "לראות" ברמה המיקרוסקופית כיצד איברים ורקמות פועלים. בשנים האחרונות נראתה התקדמות משמעותית במחקר, בעיקר בשיטות ליצירת פרופיל של פעילות גנים ושכבות אחרות של נתונים בתאים בודדים או בקבוצות קטנות של תאים. עם זאת, יש לשחזר את המידע לגבי המיקומים המקוריים של התאים בעלי הפרופיל בתוך הרקמות, מכיוון שגישות אלו מבקשות לעיתים קרובות את פירוק הרקמות והפרדת התאים משכניהם. הטכניקה החדשה גם רושמת את הנתונים המרחביים הללו, והיא עושה זאת ברזולוציה מעולה.
השיטה מבוססת בחלקה על טכנולוגיית 10x Genomics הקיימת. הוא משתמש בשקופיות זכוכית המתאימות להדמיית דגימות רקמה בשיטות פתולוגיות רגילות המבוססות על מיקרוסקופ, אך גם מצופה באלפי מולקולות בדיקה מסוימות.
ה"ברקוד" הכימי של כל מולקולת בדיקה מזהה את מיקומה הדו-ממדי על השקף. מולקולות הבדיקה על השקף תופסות את RNA שליח (mRNAs), בעצם התמלילים של גנים מופעלים, מתאי שכנים כאשר דגימת רקמה פרוסה דקה מונחת על השקופית, התאים שלה הופכים לחדירים. נוגדנים מעצבים משמשים בהליך, והם נצמדים למולקולות הבדיקה הייחודיות והחלבונים המעניינים ברקמה.
חוקרים יכולים לזהות במהירות ובאופן אוטומטי את ה-mRNA שנאספו ואת החלבונים הנבחרים ולמפות אותם במדויק למיקומים המקוריים שלהם לאורך דגימת הרקמה. ניתן לשקול את המפות המופקות באופן עצמאי או בהשוואה להדמיית הפתולוגיה השגרתית של המדגם.
על רקמות מטחול בריא של עכבר, הצוות השתמש ב-SPOTS כדי להראות את הארכיטקטורה התפקודית המורכבת של איבר זה, כולל אשכולות מסוגי תאים שונים, מצבי התפקוד שלהם וכיצד השתנו מצבים אלה בהתאם למיקום התאים.
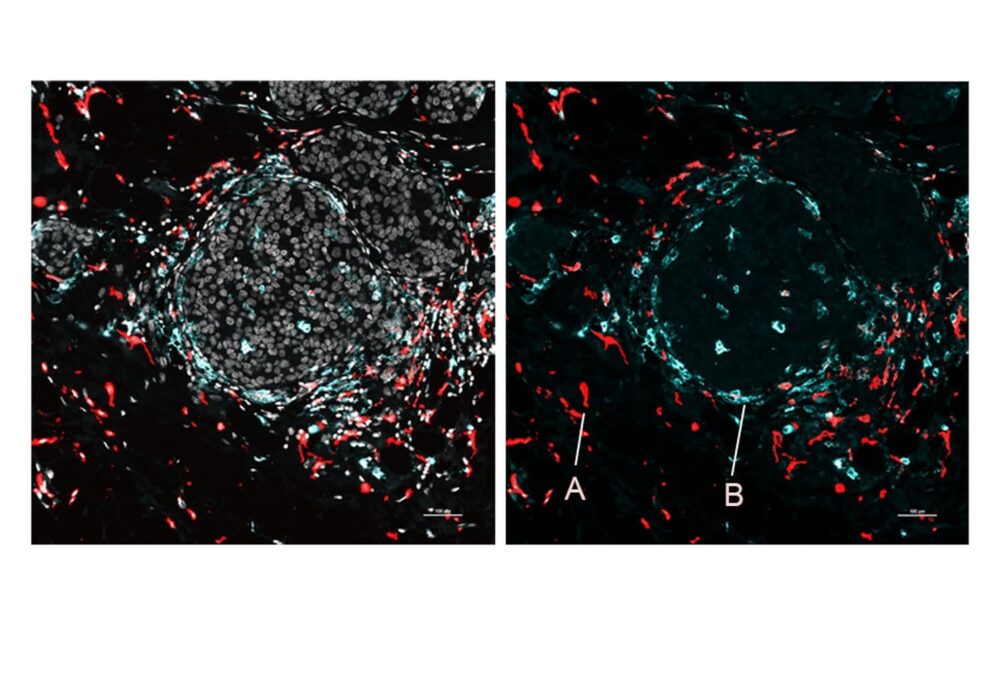
החוקרים השתמשו גם ב-SPOTS כדי למפות את המבנה התאי של גידול בשד עכבר, תוך הדגשת הפוטנציאל שלו לשימוש ב סרטן מחקר. המפה שנוצרה הראתה מקרופאגים, ותאי חיסון, בשני מצבים שונים, כל אחד מסומן על ידי סמן חלבון אחר: מצב אחד היה פעיל ונאבק בגידולים, בעוד השני היה מדכא חיסון ומקים מחסום להגנה על הגידול.
ד"ר לנדאו, אונקולוג במרכז הרפואי ניו-יורק-פרסביטריאן/ווייל קורנל, אמר, "יכולנו לראות ששתי תת-קבוצות המקרופאגים הללו נמצאות באזורים שונים של הגידול ומקיימים אינטראקציה עם תאים שונים - וההבדל במיקרו-סביבה כנראה מניע את מצבי הפעילות המובהקים שלהם."
"פרטים כאלה של הסביבה החיסונית של הגידול - פרטים שלעתים קרובות לא ניתנים לפתרון עקב דלילות תאי החיסון בתוך הגידולים - עשויים לעזור להסביר מדוע חלק מהחולים מגיבים ל טיפול לחיזוק מערכת החיסון וחלקם לא, ובכך יכולים להודיע על התכנון של אימונותרפיות עתידיות."
"לגרסה הראשונית הזו של SPOTS יש רזולוציה מרחבית כך שכל "פיקסל" של מערך הנתונים המתקבל מסכם מידע על פעילות הגנים עבור מספר תאים לפחות. עם זאת, החוקרים מקווים לצמצם בקרוב את ההחלטה הזו לתאים בודדים תוך הוספת שכבות אחרות של מידע סלולרי מרכזי."
עיון ביומן:
- Ben-Chetrit, N., Niu, X., Swett, AD et al. אינטגרציה של פרופיל מרחבי תעתיק שלם עם סמני חלבון. נט ביוטכנול (2023). DOI: 10.1038/s41587-022-01536-3