מבוא
לגרום לתאים חיים להבהב פלואורסצנטי כמו אורות מסיבה עשוי להישמע קל דעת. אבל ההדגמה שזה אפשרי יכולה להיות צעד לקראת מתישהו לתכנת את תאי החיסון של הגוף שלנו לתקוף סרטן בצורה יעילה ובטוחה יותר.
כך נקראת ההבטחה של התחום ביולוגיה סינתטית. בעוד שביולוגים מולקולריים מפשיטים תאים לגנים ולמולקולות המרכיבים אותם כדי לראות כיצד הם פועלים, ביולוגים סינתטיים מתעסקים בתאים כדי לגרום להם לבצע הישגים חדשים - מגלים סודות חדשים על איך החיים פועלים בתהליך. בפרק זה, סטיבן סטרוגאץ מדבר עם מיכאל אלוביץ, פרופסור לביולוגיה וביו-הנדסה במכון הטכנולוגי של קליפורניה וחוקר במכון הרפואי הווארד יוז.
תקשיב Apple Podcasts, Spotify, Google Podcasts, Stitcher, לכונן או אפליקציית הפודקאסט המועדפת עליך, או שאתה יכול להזרים את זה Quanta.
תמליל
סטיב סטרוגאץ (00:03): אני סטיב סטרוגאץ, וזהו השמחה של למה, פודקאסט מ מגזין Quanta זה לוקח אותך לכמה מהשאלות הגדולות ביותר ללא מענה במדע ובמתמטיקה כיום. בפרק זה, אנחנו הולכים לדבר על ביולוגיה סינתטית.
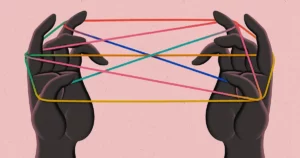
(00:18) מהי ביולוגיה סינתטית ומה מדענים מנסים לעשות איתה? במילים פשוטות, נוכל לומר שביולוגיה סינתטית היא מיזוג של ביולוגיה, במיוחד ביולוגיה מולקולרית, והנדסה. הדבר הייחודי בו הוא שהוא מתייחס לתאים כאל מכשירים הניתנים לתכנות. זו מעין גישת צעצוע טינקר שבונה מעגלים, אבל לא מחוטים ומתגים כמו שאנחנו רגילים אליהם, אלא דווקא מתוך רכיבים ביולוגיים, כמו חלבונים וגנים. תכנות תאים בצורה זו לא ממש שונה מתכנות מחשבים, אלא ששפת התכנות היא לא Python, או C++. זו שפת הביולוגיה, שפת ה-DNA, במטרה ליצור חלבונים שיתקשרו זה עם זה בדרכים חכמות.
(01:10) היישומים הרפואיים הפוטנציאליים של ביולוגיה סינתטית הם עצומים. אבל גם, הגישה טומנת בחובה הבטחה להאיר כיצד החיים עובדים ברמה העמוקה ביותר. זה דבר אחד להפשיט תאים כדי לראות איך הם עובדים. זו הגישה הקלאסית לביולוגיה מולקולרית. אבל זה דבר אחר להתעסק בתאים כדי לנסות לגרום להם לבצע טריקים חדשים, וזה משהו שהאורח שלי, מיכאל אלוביץ', עושה. לדוגמה, לפני זמן מה, הוא עיצב תאים שיהבהבו ויכבו כמו אורות חג המולד. וזו רק ההתחלה. מייקל אלוביץ' הוא פרופסור לביולוגיה והנדסה ביולוגית במכון הרפואי קלטק והווארד יוז. ברוך הבא, מייקל.
מיכאל אלוביץ (01:51): תודה, סטיב. זה נהדר להיות כאן.
סטרוגאץ (01:53): אז בואו נדבר על הרעיון הבסיסי של ביולוגיה סינתטית. הזכרתי את זה בהקדמה, כלומר - שתאים חיים, אנחנו יכולים לחשוב עליהם כעל מכשירים הניתנים לתכנות. התחום, ביולוגיה סינתטית, נראה שיש לכם את הפילוסופיה הזו שאתם יכולים ללמוד על תאים על ידי בניית פונקציונליות לתאים בעצמכם. במקום לפרק דברים, תלמדו על ידי יצירה. בערך כמו ילד שמשחק בארגז חול או משהו כזה.
אלוביץ' (02:23): כן, אז אני מניח, אתה יודע, אני חושב, במובן מסוים, יש כל מיני דרכים שונות להעריך ולהבין מערכות ביולוגיות. והגישה הביולוגית הקלאסית היא להתחיל עם המורכבות המדהימה של תא או אורגניזם שלם ולנסות באמת לנתח אותו ולפרק אותו. ולכן אתה שואל לעתים קרובות שאלות כמו, אילו גנים נחוצים לתא כדי לעשות משהו מעניין, למצוא את האוכל שלו או למצוא בן זוג או משהו כזה? אז אתה סוג של מפרק מערכת מורכבת ומנסה להבין את הפונקציה של הרכיבים האישיים שלה, ואיך כולם עובדים יחד כדי לתת לך את הפונקציה הזו. זה סוג של, אתה יודע, במובן מסוים ביולוגיה רגילה.
(03:02) ביולוגיה סינתטית מעין, מעיפה אותה על הראש, והיא מעין מנסה להגיע לזה - שאלות דומות אבל מהגישה ההפוכה. הוא אומר, בוא נפשט הכל ונשאל לא מה צריך אלא מה מספיק? מהי הסט המינימלי של רכיבים ואינטראקציות שמספיקות כדי לאפשר לתא לעשות משהו? למצמץ ולכבות. ללכת - אתה יודע, הפוך למצב אחר, מה שאתה רוצה. אז זה סוג של גישה בונה, סוג של בנייה מלמטה. והוא יכול לענות על סוגים שונים של שאלות. כאילו, דבר אחד שהוא מאפשר לך לעשות הוא להשוות סוגים שונים של עיצובים עבור אותה פונקציה ולשאול, אתה יודע, "האם יש יתרונות לתכנון מעגל אחד על פני עיצוב מעגל אחר?" לדוגמה.
(03:43) זה קשה לעשות במערכת טבעית, שבה אתה מתחיל עם עיצוב מעגל מסובך אחד. אתה לא באמת מבין בזה הכל, אתה יודע, ואתה לא באמת יכול להחליף אותו לגמרי בהכרח בעיצוב אחר לגמרי. זה מה שהביולוגיה הסינתטית מאפשרת לך לעשות.
סטרוגאץ (03:56): אה-הא. אז אני קצת מבולבל לגבי השימוש שלך במילה "מעגל". לי, תא מרגיש יותר כמו עיר שהרבה קורה בה. כל השחקנים השונים האלה ו... אבל מה יש לך בראש כשאתה מדבר על מעגל? איך זה תא, או - האם מערכת הבקרה של התא היא המעגל? או מה? מה האנלוגי כאן?
אלוביץ' (04:15): כן, אני מניח שהאנלוגיה היא באמת זה, אתה יודע - מה יש בתוך התא? יש DNA, שהוא - הגנום שלך, המכיל את הרצפים של כל החלבונים השונים. אז התאים שלך מלאים בגן חיות של החלבונים השונים האלה. וחלבונים, שונים, יכולים לבצע תגובה כימית, או שהם יכולים ליצור מבנים בתוך התא, או שהם יכולים לעבד מידע במקרים רבים. והדרך שבה הם עושים זאת היא שכל אחד מהחלבונים האלה יכול לשנות ביעילות, בדרך מסוימת, חלבון אחר.
(04:49) אז האנלוגיה עם המעגל האלקטרוני היא באמת שכמו שיש לך נגדים וטרנזיסטורים וכן הלאה שמחוברים על ידי חוטים, בתא יש לך סוגים שונים של חלבונים שעושים דברים ספציפיים אחד לשני בצורה מאוד ספציפית דרכים. והחוט - האנלוגיה של החוט היא ממש כמו הספציפיות המולקולרית. זו העובדה, שאתה יודע, חלבון אחד ייצמד לסוג חלבון אחר וישפיע עליו בצורה מסוימת.
סטרוגאץ (05:15): אה-הא. זה דבר ממש מעניין עבור כל מי שאי פעם ניסה לבנות משהו. אתה בדרך תמיד נתקל בבעיות. ואתה יודע, יש אסטרטגיה אחת, והיא שאתה יכול להנדס לאחור משהו שכבר נבנה. כמו, נניח, אם אתה רוצה לבנות רדיו, אתה יכול למצוא רדיו, לפרק אותו, להסתכל על כל החלקים ולנסות להבין מה הם עושים. אבל זה נשמע כאילו מה שאתה אומר הוא שיש את הגישה ה"בסיסית" הזו שבה אתה מתחיל - אני אוהב את מה שאמרת, "מספיק, במקום...". או רגע, אמרת "הכרחי" ולא "מספיק"?
אלוביץ' (05:45): זה מספיק ולא הכרחי. אז מה הדבר המינימלי שמספיק לעשות משהו ולא מה שצריך. אבל אולי אוכל להוסיף לזה, כאילו, אני חושב שמה שמוזר בזה קצת זה שזה לא לגמרי כמו לבנות את זה מאפס. זה לא חיים מלאכותיים, זה לא יצירת תא רק מתוך מולקולות. אנחנו לוקחים גנים וחלבונים ומכניסים אותם לתא כדי שהם יבצעו פונקציה מסוימת שתכננו. אבל הם - כדי לעשות זאת, הם צריכים לעשות שימוש בכל היכולות שכבר קיימות בתא.
(06:14) לדוגמה, אם אני מכניס גן לתא הזה, הגן הזה יבוא לידי ביטוי, מה שאומר שייווצר ממנו חלבון. וזה יתבצע על ידי סט שלם של מכונות מולקולריות, הפולימראז ודברים כאלה, שבעצם עושים את זה כל הזמן בתא. אז מצד אחד, אנחנו בונים את הפונקציה שאכפת לנו ממנה, אבל אנחנו עושים את זה בתוך סוג של מערכת הפעלה בצורה שהתא מספק שמספק, אתה יודע, את כל התשתית הדרושה לנו מעגל לרוץ.
סטרוגאץ (06:42): אז אתה מסתובב עם מה שכבר יש. אבל אתה באמת יכול לגרום לזה לעשות, כמו שאתה אומר, פונקציות חדשות אולי לפי רצונך - בתקווה, לפי רצונך.
אלוביץ' (06:51): כן, זה הדבר המטריף בביולוגיה. זה, אתה יודע, זה לא היה חייב להיות נכון, שהמנגנון של התא תומך לא רק בתפקודים שהתפתחו איתו באופן טבעי, אלא גם בפונקציות חדשות שאתה מחבר או משתיל מאורגניזמים אחרים. יש היבט כזה של תאימות בין, אתם יודעים, גן מ - גן אינסולין אנושי ניתן להכניס לחיידק וליצור אינסולין למרות שהאב הקדמון המשותף האחרון של אדם וחיידק היה לפני מיליארדי שנים. אז זה די מדהים. כאילו, אתה לא יכול לקחת את אפליקציית Windows ולהפעיל אותה על מק, אבל אתה יכול לקחת גן אנושי ולבטא אותו בחיידק. כך…
סטרוגאץ (07:28): אז זו נקודה ממש מעניינת, כל העניין הזה ש- בוא נראה אם אני יכול, אולי נפרק את זה קצת ביחד. אתה אומר שעל ידי ניסיון לגרום לתא לבצע פונקציה חדשה כלשהי, אולי חשבתם שהדרישות האלה או שהן יבצע משהו שהוא לא התפתח לעשות עשוי לשבור את התא, נכון? כאילו זה עלול לגרום להכל להתפרק. והרבה מהגאדג'טים שבני אדם מעצבים, שלעתים קרובות עוברים אופטימיזציה בדרך זו או אחרת, הם מאוד שבירים, נכון? אם אתה, אם אתה שואל, דוחף אותם מאזור הנוחות שלהם, הם מתפרקים. אתה אומר שזה לגמרי לא מה שקורה בתאים שאתה עובד איתם.
אלוביץ' (08:05): זה נכון. זה מה שמדהים. והשאלה היא בערך, אתה יודע, יש שאלה עמוקה לגבי למה התא הוא כזה. מדוע יש לו את הגמישות להכיל סוגים חדשים של תוכניות שאתה מכניס לתוכו. למה זה לא שביר, כמו שאמרת. ואני יכול לשער על זה קצת.
סטרוגאץ: בטוח.
אלוביץ' (08:23): בסדר. אני, אתה יודע, אני חושב שזה באמת קשור לעקרון של התפתחות. זה הרעיון שהמערכות שיש לנו בתא לא רק טובות במה שהן עושות בתא הזה. אלו מערכות שהמשיכו להתפתח במשך מיליארדי שנים ומאפשרות לאורגניזם להתפתח. וכדי לעשות זאת, הם צריכים להיות בעלי הגמישות לתמוך בסוגים חדשים של פונקציות שיכולות להתעורר דרך האבולוציה. ולכן אותו דבר שהופך אורגניזמים לניתנים להתפתחות עשוי גם להפוך אותם לניתנים להנדסה.
סטרוגאץ (08:53): אה אה. מעניין, נכון. אז מכיוון שהאבולוציה תלויה ביכולת לשנות - כלומר, על זה המילה "להתפתח", זה סוג של שינוי לאורך זמן. לכן, התא צריך להיות מסוגל לעמוד בדרישות מסוג זה כדי להיות מסוגל להשתנות בהדרגה או לפעמים אפילו בקפיצות גדולות. ואתה אומר, אם כן, מה שזה לא יהיה שמאפשר לתאים לעשות את זה, גם מאפשר לך לעשות להם את זה בכך שאתה גורם לך לכפות עליהם את השינויים ולא על העולם החיצון.
אלוביץ' (09:22): בדיוק. כֵּן. אז, אתה יודע, אלו סוג של רעיונות קלאסיים. ובעצם, יש ספר יפה מאת [ג'ון] גרהרט ו[מארק] קירשנר, בערך על זה רעיון של וריאציה קלה. אבל אני חושב שזה די מעניין לחשוב איך, אתה יודע, כמה ברור שהתא לא התפתח כדי לאפשר ביולוגיה סינתטית, עד כמה שאנחנו יודעים. אבל, אתה יודע, המאפיינים האלה כן מאפשרים את זה, לפחות במידה מסוימת.
סטרוגאץ (09:45): בסדר, אבל אולי כדאי שנגיע לנקודה של זה. כמו למה אתה רוצה לתכנת תאים? למה אתה מתעסק ומתעסק ברמה הסלולרית? מה אתה מנסה לעשות?
אלוביץ' (09:55): אני חושב שיש סוג של שתי סיבות לעשות ביולוגיה סינתטית, שני סוגים של סיבות. ואחד הוא שיש מגוון עצום של יישומים, אתה יודע? אתה יכול להנדס תאים להיות מפעלים קטנים שמייצרים תרופות, חומרים, דלקים, סוגים אחרים של כימיקלים. ואתה יכול לעשות זאת על ידי הכנסת גנים לאנזימים. ועל ידי סוג של לקיחת אנזימים מאורגניזמים אחרים וחיבורם באורגניזם אחד, אתה יכול להפוך את התא למעין בית חרושת קטן. והוא יכול לייצר, לייצר את הכימיקלים האלה בזול יותר, לעתים קרובות יותר, ליתר דיוק, וליצור סוגים שונים של כימיקלים ממה שאתה יכול לעשות בתהליך סינתזה כימי קונבנציונלי. אז זה סוג של דבר פשוט מאוד שימושי וחזק.
(10:37) יש גם סוג של יישומים סביבתיים. אתה יודע, כמו אנשים מהנדסים חיידקים או חיידקים שיכולים לתקן חנקן או לתקן פחמן. זה סוג של ממש מרגש, ומשהו שיכול להיות בעל השפעה רבה, פוטנציאלית, על הסביבה לקיימות. ואז יש יישומים שהם סוג של הצד הטיפולי. ואני חושב שאלו, אני חושב, גם מרגשים במיוחד. כי, אתה יודע, תא, אם אתה יכול לתכנת אותו, יכול להיות תרופה מדהימה, נכון? הרבה יותר חזק ממולקולה. אז אתה יודע, תרופה מולקולרית יכולה להיות מאוד ספציפית למטרה שלה. אבל תא יכול להיות מתוכנת לזהות הרבה מידע שונה בסביבה, לעבד את המידע הזה, לקבל החלטות, אתה יודע, לנסות למצוא תאי מטרה ספציפיים ולשנות את התנהגותם או להרוג אותם. יש לו הרבה סוג של גמישות ניתנת לתכנות כמכשיר טיפולי.
(11:25) אז זהו, אתה יודע, אני חושב שכל אלה ביחד הם סוג של סיבה אחת טובה לנסות להבין איך לתכנת תאים. הצד השני של זה הוא היכולת הזו ללמוד על עקרונות הביולוגיה בדרך זו. שבדיוק כשאתה מתחיל לשחק עם הרכיבים האלה, אתה שואל שאלות שונות על התא ממה שהיית שואל אם אתה מפרק מערכת ממש מורכבת. אתה יודע, אולי אתה, אתה לומד על - יש מרכיבים בתא שמפרקים חלבונים. ואז אתה מתחיל לשאול, "בסדר, איך אני יכול להשתמש בהם כדי לפרק כל חלבון שאני רוצה?" לדוגמה. אז אתה מתחיל קצת לקחת נקודת מבט של משתמש. זה קצת כמו לעבור ממישהו שמשתמש במחשב למישהו שהוא כמו לנסות לפרוץ או לתכנת מחשב. פשוט, אתה שואל שאלות שונות על המחשב, אז.
סטרוגאץ (11:25): בסדר, אז אלו שלושה כיוונים ממש מעניינים עבורנו לחקור. תן לי לראות אם אני יכול לסכם. אז ביולוגיה סינתטית, בשירות של יצירת סוגים חדשים של מפעלים לייצור אינסולין או מולקולות שימושיות אחרות. ביולוגיה סינתטית, הזכרת, לדברים שאינם בהכרח רפואיים, אבל אולי הם יכולים לתפוס פחמן מהאטמוספרה או מהאוקיינוס כדי אולי לעזור לנו עם שינויי אקלים ודברים מהסוג הזה, או אולי לעכל פלסטיק וכל הזבל הזה שצף מסביב באוקיינוס. ואז, כחלון לביולוגיה עצמה.
(12:40) האם אתה יכול להגדיר לנו את ההקשר מבחינת ההיסטוריה או מאיפה השדה עצמו הגיע? אז כאילו, מאיפה זה התחיל? האם זה נושא ישן מאוד? האם זה נושא חדש מאוד?
אלוביץ' (12:52): בעיני, כמו שאחת ההשראות הגדולות באמת מגיעה מהעידן הקלאסי של הביולוגיה המולקולרית, כשאנשים כמו [פרנסואה] ג'ייקוב ו[ז'אק] מונוד ואחרים ניסו להבין כיצד תאים לווסת את הביטוי של הגנים שלהם. איך הם יודעים מתי - כמו חיידק נחשף לסוכר חדש. איך הוא יודע להפעיל את הגנים הדרושים לחילוף החומרים של הסוכר הזה? והם גילו מדכאים, שהם חלבונים שמכבים את הביטוי של גן. והם הבינו שבנוכחות הסוכר, הסוכר יכול להשבית את המדכא. אז זה כבר לא יכבה את הביטוי של הגן שהיה הכרחי לעיכול הסוכר. אז זה היה כמו מעגל רגולציה פשוט מאוד. למעשה, הסוכר היה לקטוז. וזה הפך לפרדיגמה של ביולוגיה מולקולרית להבנת ויסות גנים.
סטרוגאץ (13:39): אני רק רוצה שתעצור כאן, כי אני מרגיש שכאשר אנחנו מדברים על ויסות גנים או רצפים רגולטוריים, או סוג כזה, אני תמיד מרגיש שזה סוג של רעיון מופשט שהוא באמת עוצר נשימה ומרגש, כשמבינים אותו, אבל פשוט נשמע כמו הרבה מילים כשזה לא מובן. אז החלבונים יכולים לעשות כל מיני דברים בתאים. הם יכולים להיות מבניים, כמו שכולם יודעים שהשיער שלהם עשוי ממנו, יש להם קולגן, נכון? אז יש לנו, אתה יכול להשתמש בחלבונים כדי ליצור מבנים אמיתיים כמו שיער, או שהם יכולים לשחק תפקיד בעור שלך או כל דבר אחר. בסדר, יש את זה. אז חלבונים יכולים לעשות את הדבר הצנוע הזה - פשוט להיות חלק מהבניין. אז הם גם יכולים לעשות דברים כמו לעזור לתגובות כימיות לעבור מהר יותר ממה שהם היו עושים אחרת. הם יכולים להיות אנזימים, הם יכולים להיות זרזים, הם יכולים לעשות דברים כאלה.
(13:45) אבל הדבר המטורף באמת שחלק מהחלבונים יכולים לעשות, לפי דרך החשיבה שלי כאדם נאיבי לגבי ביולוגיה, הוא שהם יכולים להפעיל או לכבות גנים. כאילו, אתה מדבר על מדכאים. אז חלבון יכול למעשה לעזור לגן אחר לייצר יותר מחלבון אחר, כולל עצמו. כלומר, שם אתה באמת נכנס ללולאות לוגיות מוזרות. אני חלבון שאומר לגן שלי "עושה ממני יותר" או "עושה ממני פחות". זה קטע הרגולציה, נכון?
אלוביץ' (14:58): כן, בהחלט. ואני חושב ששם הדברים נעשים ממש כיף, כי, אתה יודע, בדיוק כמו שאמרת, חלבון יכול לכבות את עצמו - או לכבות את הגן שלו או להפעיל את הגן שלו, מה שבאמת אומר לשלוט ברמה שלו. ולמעשה, זה לא רק שהוא יכול לעשות את זה. זה כן עושה את זה. אז אני חושב שסוג כזה של מעגל - שהוא באמת המעגל המעניין הפשוט ביותר שאתה יכול לדמיין, גן שמכבה את עצמו - מתרחש הרבה יותר ממה שהיית מצפה במקרה. אתה יודע, זה קורה כל הזמן שגנים מווסתים את עצמם. והם יכולים לעשות את זה בצורה שלילית, להדחיק את עצמם. יש גם חלבונים שמפעילים גנים שיכולים להפעיל את עצמם באותה מידה, ויש להם סוגים אחרים של פונקציות.
(15:37) אז אם אתה מתחיל להכליל את זה, ואתה מדמיין סוג של רשת, שבה יש לך חבורה של חלבונים אלה, וכולם מווסתים זה את זה בדרכים שונות. ואז, אתה יודע, פשוט דמיינו לעצמכם גרף עם חבורה של גנים אלה והחצים שאומרים אילו מהם מווסתים אילו אחרים. אתה מתחיל קצת, אתה יודע, להמשיג את המורכבות של הרגולציה של התא - שיש את כל החצים השונים האלה בין כל אחד מהרגולטורים האלה, וכל אחד מהאחרים. והם סוג של... מה כל זה עושה? אילו סוגים של התנהגויות זה מייצר?
סטרוגאץ (16:06): אני מתכוון, בדיוק, כי הדבר הזה מתחיל להישמע לי כמו מחשב, שבו יש מעגלי מיתוג שמפעילים כל אחד, אתה יודע, דבר - אלמנטים שמדליקים או מכבים אחד את השני. ואם אני דולק, אני גורם לך לרדת, אז עכשיו אתה כבוי, אבל עכשיו החופש שלך מאפשר למשהו אחר להימשך. זה גם מתחיל להישמע כמו מוח, נכון? כלומר, למוח יש את כל הנוירונים האלה שמעכבים זה את זה או מפעילים זה את זה. אז אתה מתחיל להרגיש שהתא יכול, במובן כימי מסוים, לחשוב.
אלוביץ': בהחלט.
סטרוגאץ: או מחשוב או משהו.
אלוביץ' (16:36): כן. הם - הם בהחלט מחשבים, וזה - אתה יכול לראות את זה בהרבה מערכות שונות בביולוגיה. שזה לא סתם קליטת מידע באופן פסיבי. זה מעבד את המידע הזה, וזה עושה את זה דרך המעגלים המולקולריים האלה.
סטרוגאץ (16:49): מה השאלה, או מכלול השאלות שבלב המחקר שלך?
אלוביץ' (16:54): ובכן, אני חושב, אתה יודע, בשבילי, זה באמת כמו: מה צריך כדי להפוך את הביולוגיה לניתנת לתכנות? כדי שנוכל ליצור באופן חזוי, אתה יודע, כמעט כל פונקציה חדשה שנרצה מתוך התאים. אוקיי, אז זה סוג של הנושא הגדול. זו בעיה גדולה, קשה, גדולה - זו בעיה גדולה.
סטרוגאץ: זה גדול.
אלוביץ' (17:11): כן. אז, אתה יודע, אני חושב שהנחת היסוד איתה אנחנו עובדים - האם זה רק, כאילו, עבור מעגלים אלקטרוניים? אתה לא הולך, בנקודת הזמן הזו, אתה לא הולך רק לחבר טרנזיסטורים אקראיים ופשוט לראות מה קורה. אתה הולך להשתמש בחבורה של עקרונות עיצוב מעגלים מוגדרים היטב ואלקטרוניקה שאנשים גילו במשך עשורים רבים. ולכן יש לנו תחושה לגבי אילו סוגי מעגלים טובים עבור אילו סוגי פונקציות.
(17:37) ולכן הנחת היסוד שלנו היא באמת שיש עקרונות מקבילים לתכנון מעגלים ביולוגיים. ורבים מהם כנראה עדיין לא התגלו. אבל אפשר לגלות אותם, והם צריכים לחול באותה מידה על מעגלים טבעיים, או שהם יכולים לחול באותה מידה על מעגלים טבעיים שהתפתחו. וגם יאפשר לנו ליצור מעגלים שפועלים בצורה צפויה יותר בתא. במילים אחרות, אנחנו מנסים קצת להבין את העקרונות של מעגלים - עיצוב מעגלים שלא רק מיובאים מהנדסת חשמל, אלא למעשה מתאימים יותר לאופן שבו התא פועל. כי אחרי הכל, אלה מעגלים מולקולריים, הם לא מעגלים אלקטרוניים.
(18:14) אז זה בערך כמו השאלה. אבל אז איך בעצם עושים את זה? אוקיי, אז אתה יודע, אתה לא יכול פשוט לחכות עד שהעקרונות יירדו, אתה יודע, עליך. אתה צריך לצאת ולנסות לחפש אותם. וכרגע, מה שאנחנו באמת מתלהבים ממנו הוא שרוב הביולוגיה הסינתטית, הייתי אומר, עד כה התמקדה בפונקציות שניתן לתכנת בתא בודד. אז אתה יכול לגדל את התא הזה לאוכלוסייה, אבל כל התאים באוכלוסייה הזו יעשו את אותו הדבר.
(18:40) אבל אנחנו יודעים שהרבה מהדברים הכי מרגשים בביולוגיה מנצלים את העובדה שתאים אוהבים לעבוד יחד. אז אנחנו אורגניזם רב תאי ענק המורכב מטריליוני תאים. ואפילו חיידקים, שאנשים חושבים עליהם כעל אורגניזמים חד-תאיים, הם רק לעתים רחוקות לבד. אתה יודע, הם, הם מקיימים אינטראקציה זה עם זה ועם מיקרואורגניזמים אחרים בסביבות מורכבות. ולכן הרבה מהפונקציונליות שבאמת מדהימה בתאים נובעת מהיכולת שלהם לפעול יחד כמערכות רב-תאיות. והיינו רוצים להביא את הביולוגיה הסינתטית לרמה הרב-תאית הזו, על-ידי בניית מעגלים המנצלים את הרב-תאיות כדי לעשות דברים שיהיה קשה לעשות עבור תא בודד.
סטרוגאץ (19:19): אני מתכוון, זה סיפור כל כך עשיר לדבר על ההתנהגות הקולקטיבית של התאים, במיוחד כשיש להם תפקידים מובחנים. אבל אני מרגיש שאנחנו צריכים לדבר על היבט המעגל קודם. אז אני תוהה אם נוכל, לפני שנכנס להתנהגות קולקטיבית, פשוט לדבר על, איך מעגל ביולוגי זהה או במה הוא שונה ממעגל אלקטרוני?
אלוביץ' (19:42): אחד הדברים האהובים עלי שבאמת נוגע להבדל המהותי בין, אתה יודע, מעגל אלקטרוני למעגל ביולוגי הוא משהו שאנו מכנים רעש. אז למערכת יכולה להיות אקראיות מהותית. במילים אחרות, ייתכן שההתנהגות אינה ניתנת לחיזוי לחלוטין. זה לא דטרמיניסטי. כל אלה רק דרכים שונות לומר את אותו הדבר. ובמעגל אלקטרוני, יש רעש, אתה יודע, יש רעש בזרימת אלקטרונים לאורך חוט. רק שתכננו מעגלים אלקטרוניים כך שגודל הרעש הזה כמעט אף פעם לא משפיע על התנהגות המעגל. אז המעגל האלקטרוני הזה במחשב שלך הולך להתנהג באופן דטרמיניסטי. לגמרי צפוי.
(20:21) נראה שהחיים אינם פועלים במשטר הזה. בתוך התא, הביטוי של גן יכול להשתנות, ותנודות אלו הן אקראיות. הם אקראיים מטבעם, והם בדרך כלשהי מעבר לשליטת התא. התא יכול לומר, "אני רוצה יותר מהגן הזה או פחות", יכול לשלוט על דברים כמותית. אבל כמות החלבון המדויקת שהוא מייצר, למשל, אינה נקבעת במדויק. וזה, כשחושבים על זה, רק מהנדסת חשמל, זה פשוט מתחיל להיראות כאילו, ובכן, תאים הם פשוט לא טובים. הם לא טובים כמו המכשירים האלקטרוניים שלנו.
אבל לאחר זמן מה, אתה מתחיל להבין שזו, אתה יודע, תכונה ולא רק באג במובנים רבים. אז זה משהו שנותן לתאים את היכולת לקבל, באופן מסוים, מחוללי מספרים אקראיים קטנים משלהם כדי להשתמש באסטרטגיות מופצות. אז למשל, כדי לחלק את הלידה, אולי יש לי אוכלוסיית תאים, התאים כולם שווים באופן נומינלי זה לזה. אבל על ידי ניצול רעש, אני יכול לומר שאני רוצה ש-30% מהתאים האלה יעשו את הדבר הזה ו-70% יעשו את הדבר האחר הזה.
סטרוגאץ (21:27): אז בוא נדבר על כמה מהדברים שעשית במעבדה, מייקל. ולמעשה, אם אני מקווה שאני לא להביך אותך, אני מתכוון, אתה די ידוע. אתה, למשל, יצרת משהו שנקרא המדכא, שזה סוג של שילוב של משהו שעושה הדחקה ותנודה. אתה יכול לספר לנו על זה? מה עושה מדכא?
אלוביץ' (21:48): המדכא הוא מעגל סינטטי שיוצר - הוא מתנהג כמו שעון קטן בתוך תא. אז הוא יוצר תנודות ברמות החלבונים שלו. אבל השאלה היא בערך, אני חושב, למה לבנות משהו כזה? אז זה משהו ש- הייתי סטודנט לתואר שני בפרינסטון, ועבדתי איתו סטניסלס לייבלר במעבדה שלו, והתחלנו להתעניין, באמת בשאלות על המאפיינים של סוגים שונים של מעגלים. ומה שהתחלנו לתהות זה האם אתה באמת יכול לבנות מעגל סינטטי שעושה משהו לא טריוויאלי מאפס. והשאלה הייתה, כמובן, איזה סוג של מעגל היית בונה? אתה יכול לבנות הרבה סוגים שונים של דברים, מתגים או כמעט כל דבר שאתה יכול לדמיין.
(22:31) אתה יודע, אני חושב שאחד הדברים הכי מרתקים בביולוגיה הם מעגלי השעון האלה. אז יש לנו שעונים צירקדיים משלנו. מחזור תא הוא סוג של שעון שגורם לתא לגדול ולהתחלק, ולגדול ולהתחלק, שוב ושוב. יש כל מיני שעונים בביולוגיה. ובמהלך המדע והפיסיקה בפרט, מתנדים הם תמיד חשובים.
(22:53) אז קצת תהינו, האם נוכל לבנות משהו כזה? ומה שבסופו של דבר הגענו אליו היה עיצוב שאנחנו קוראים לו עכשיו המדכא. וזה סוג של משחק אבן-מספריים-נייר של חלבונים בתוך תא. אז הרעיון של המעגל הוא שהוא בנוי משלושה סוגים של חלבון, שנקראים, עליהם דיברנו כבר, המדכאים האלה. וכל אחד מהמדכאים האלה יכול להדחיק ספציפית את המדכא הבא במעגל. אז Repressor 1 מדחיק את Repressor 2, Repressor 2 מדחיק את Repressor 3, וה-Repressor 3 מדחיק את Repressor 1 שוב. אז זה סוג של טופולוגיית הסלע-מספריים-נייר, אם אתה רוצה.
אלוביץ' (23:33): אז אם אתה קצת מתחיל לדמיין מה המעגל הזה יכול לעשות, דמיין שפתאום יש לי הרבה מדחיק 1. זה יפחית את הביטוי של מדחיק 2, אז תתחיל לעשות פחות ממנו זה. בסופו של דבר Repressor 2 ייעלם. אם הוא נעלם, זה מאפשר ל-Repressor 3 להידלק. וכך תתחיל לעשות הרבה מ-Repressor 3, וזה יכבה שוב את Repressor 1. אז בסופו של דבר שינוי במדכא אחד, לאחר שהוא מתפשט לולאת המשוב הזו, גורם לסוג של השפעה שלילית על עצמו, אבל עם עיכוב זמן. ומסתבר שזה מספיק כדי לתת לך תנודות המקיימות את עצמן שפשוט ימשיכו עוד ועוד ועוד, כשהתא גדל ומתחלק.
סטרוגאץ (24:09): ועכשיו לא מצאת דרך לעשות את זה גלוי, כמו בעין בלתי מזוינת?
אלוביץ' (24:15): כן, אז זה קריטי. וזה גם די מעניין מבחינה מדעית, אתה יודע, בשנות ה-90, הייתה השינוי המדהים הזה בביולוגיה בגלל השיבוט של החלבון הפלורסנטי הירוק, שהיה גן ממדוזות שמייצר חלבון ניאון ירוק, ומכאן שמו. ואנשים - מרטין צ'לפי סוג של שיבט את זה מתוך המדוזה וביטא אותו בחיידקים והראה שהגן הזה כשלעצמו מספיק כדי ליצור חלבון ירוק. אז עכשיו אתה יכול להסתכל על דברים שקורים בתא מבלי להרוג את התא, או לגדל אוכלוסייה עצומה של תאים.
(24:48) אז מה שעשינו זה, לקחנו שלושה מהגנים המדכאים המאופיינים בצורה הטובה ביותר, וסוג של הנדסנו אותם לתוך מעגל שלושת החלבונים הזה. ואז הכנסנו את החלבון הפלורסנטי הירוק הזה והיה לנו אחד משלושת החלבונים ששלטים בו. ולכן הרעיון הוא שאם התנודות מתרחשות בתוך התא ואנחנו עושים סרט של התאים, אז אתה יכול פשוט להסתכל על התאים, ותוכל לצפות בהם בסרט, ותראה אותם נעשה בהיר יותר ועמום יותר, ובהיר יותר ועמום יותר עם הזמן.
(25:15) אז זהו, וזה, למעשה - אני מתכוון, הדבר המעניין אותי הוא שבזמן שבניתי את זה, באמת לא היה לי מושג אם זה יעבוד. אז כשבעצם הכנסנו את המערכת הזו לתא והתחלנו לעשות סרטים, ואז למעשה ראיתי את התאים סוג של, אתה יודע, מהבהבים ונכבים לאורך זמן. זה באמת היה רגע די יוצא דופן עבורי.
סטרוגאץ (25:36): האם אתה זוכר משהו שאתה יכול לחלוק איתנו לגבי האישי שלך - כמו, האם התקשרת להורים שלך או, אתה יודע, לחבר הכי טוב או משהו כזה?
אלוביץ' (25:45): אני זוכר שהגדרתי את הניסוי, למעשה לא היה לי מושג אם הוא יעבוד או לא. ובזמן לעשות את הסרטים, המיקרוסקופ שהיה לנו היה מאבד מיקוד. אז ישנתי תנומות על ספה קטנה בסמוך למעבדה. ואז הייתי קם ומגדיר אזעקה כל שעה כדי ללכת ולמקד מחדש את המיקרוסקופ. אז די איבדתי שינה. ואז קשה לראות את זה בזמן אמת, כי התנודות איטיות. הם כמו, אתה יודע, תקופה של כמה שעות. וכך אתה לא יכול פשוט להסתכל, לצפות בו בזמן אמת. אתה יכול לומר לעצמך, "חשבתי שהתא הזה היה מבריק לפני כן. אני חושב שעכשיו זה עמום." אבל רק כשאתה סוג - אחרי, אתה יודע, בבוקר, סוג של משחק חוזר של כל הסרט ורואה אותו, אז אתה באמת יכול לראות את התאים מהבהבים לסירוגין. אז כן, סיפרתי לאנשים. סיפרתי לכולם בסביבה, ויותר ממה שהם רצו לדעת. אז זה היה, אתה יודע, מאוד מרגש.
סטרוגאץ (26:37): תודה ששיתפת אותנו בסיפור הזה. כי זה חלק מהכיף בלהיות מדען, שלפעמים דברים כן עובדים וזה, אתה יודע, כנגד כל הסיכויים, כי כמו שאתה אומר, ביולוגיה היא מסובכת. יש כל כך הרבה דברים שיכולים להשתבש. אבל כן היה לך בעל ברית אחד לצידך בכל זה, שהיה ענף של מתמטיקה, ענף המתמטיקה שאני במקרה אוהב - דינמיקה לא לינארית - שאני, אני רוצה להאמין שעזר לך בעבודתך, אבל אני לא אוהב. לא ממש מכיר את סיפור הרקע כאן. אז האם זה נכון? האם, האם מתמטיקה עזרה לך לעצב את המדכא?
אלוביץ' (27:13): כן, אני מתכוון, אני חושב שזה באמת נכון. למעשה יש לי את הספר הקלאסי של סטיב סטרוגאץ, דינמיקה וכאוס לא ליניארית. ולמעשה, מה זה אומר לעצב את המעגל, יש סוג של שתי רמות של עיצוב, ואחת היא בניית פיסות ה-DNA האלה ומבין בדיוק באילו רצפים להשתמש. אבל השני הוא ההיבט המתמטי. אז אתה יודע, אם אתה חושב על המעגל הזה שתיארתי, המדכא, הוא יכול להתנדנד כמו שאמרתי עכשיו, אתה יודע, כשכל החלבונים עולים ויורדים ללא הרף. אבל לאותו מעגל יכול להיות גם התנהגות מאוד משעממת, שבה פשוט תכין מעט מכל אחד משלושת החלבונים וזה מספיק כדי שתמשיך לייצר מספיק מכולם. והכל עקבי בעצמו, ושום דבר מעניין לא קורה באמת. למעשה, אותו מעגל, באופן עקרוני, יכול לעשות את שני הדברים. והשאלה הייתה, איך אתה מבטיח שהוא עושה את הדבר שאתה רוצה שהוא יעשה, התנודה, ולא מסוג הדברים המשעממים?
(28:03) אז מה שעשינו זה שרשמנו בדיוק, בעזרת השיטות שבספר שלך, קבוצה של משוואות דיפרנציאליות, שמתארות כיצד קצב השינוי של כל אחד משלושת החלבונים צריך להיות תלוי בכל אחד מהחלבונים האחרים ב המעגל. וכשאתה רושם את המשוואות האלה, ועושה ניתוח יציבות ליניארי, אתה סוג של מגלה שלמעגל הזה יש רק מצב יציב אחד. במילים אחרות, נקודה אחת שבה אם תשים את המעגל בנקודה זו, הוא יישאר שם. והשאלה אם היא עומדת להתנודד או לא מסתכמת בשאלה האם הנקודה הזו יציבה או לא יציבה. אז אם הוא יציב, זה אומר שאם תרחיק אותו קצת, הוא יחזור מיד אחורה. זה הפתרון המשעמם.
(28:40) אבל בתנאים מסוימים, הוא הופך לבלתי יציב. ואז המערכת מפתחת את מה שאתה יודע טוב מאוד. זה נקרא מחזור גבול, שבו אין לו ברירה אלא רק להמשיך להסתובב סביב ומסביב ומסביב. וזו ההתנהגות היציבה היחידה, או ההתנהגות - לא יציבה, אלא ההתנהגות היחידה שהיא יכולה לעשות. וזה מה שבאמת רצינו. וסוג כזה של תכונה מתמטית של מחזור הגבלה יהיה ממש רצוי כי אם יש סוג של דברים בלתי נשלטים בתוך התא שמפריעים לתא, המערכת הזו שהכנסנו, היינו רוצים שהיא תצטרך לחזור ל מחזור הגבול הזה - יצטרך להמשיך להתנודד ולא שהתנודה לא תפגע על ידי כל הדברים האלה.
(29:14) אז זה דבר יפה לגבי המדכאים: יש לו סוג כזה של פתרון מגביל מחזור. ומה שלמדנו מהמתמטיקה זה בעצם מה שהיית צריך לעשות למעגל כדי להגדיל את הסיכוי שהוא יתנודד. ומה שלמדנו הוא שהיינו צריכים לוודא שהגנים מתבטאים ברמה גבוהה, אבל שהחלבונים אינם יציבים, שהם מתכלים במהירות בתוך התא. וזה דרש סוג של תגים קטנים הנדסיים על החלבונים שגורמים לתא לבזות אותם, וזה מנוגד לאינטואיציה. כֵּן.
סטרוגאץ (29:40): אה, מעניין. נקי. אז בגלל, אתה יודע, לפעמים בתור מתמטיקאים, אנחנו אוהבים להאמין שאנחנו מועילים למדענים בתחומים אחרים, ובמיוחד בביולוגיה, כאחד הנושאים הכי מרגשים שיש. אבל זה, לא תמיד קל למצוא דוגמאות טובות באמת לכך שהמתמטיקה הייתה מועילה בשירות הביולוגיה. אז אני מעריך לשמוע שזה היה מקרה אחד שבו עשינו משהו טוב.
אלוביץ' (30:04): אני יכול גם להוסיף דבר אחד קטן -
סטרוגאץ: כן, בבקשה.
אלוביץ': זה לא רק שימושי, זה ממש חיוני. כי אפילו עם מדכא, שהוא רק שלושה גנים - וככל שמתחילים להגיע למעגלים מורכבים יותר, הבעיה הזו מחמירה עוד יותר - אתה לא יכול לנמק באופן אינטואיטיבי מה המעגל הולך לעשות. זה מסובך מדי. אתה באמת צריך את הכלים המתמטיים האלה.
סטרוגאץ (30:20): אם אני מבין נכון, אתה ועמיתיך עשיתם לאחרונה עבודה על השאלה עתיקת היומין הזו של איך אפשר לצאת מתאי שלכולם יש אותו גנום, ובכל זאת יכולים בסופו של דבר להפוך למספר עצום כזה. של סוגים שונים אפשריים של... יכולים להיות להם כל הגורלות השונים האלה. הם יכולים להפוך לתאי כבד, תאי חיסון, תאי דם, כל סוג של דבר, אפילו עם אותם גנים. אז זו, כמובן, שאלה ענקית בביולוגיה, השאלה איך אתה מבדיל. איך משיגים מורכבות?
מה כולכם עשיתם לאחרונה? אני יודע, זה נקרא בשם רב גורל, אבל על מה כל זה?
אלוביץ' (30:59): בטח, כן. בדיוק כמו שאמרת, זו כמו שאלת היסוד הזו בביולוגיה. כמו, למה או איך תאים יוצרים סוגי תאים נפרדים? בדיוק כמו שאמרת: כבד, דם, נוירון, אתה יודע, ועוד הרבה מאוד תתי סוגים שונים של כל הדברים האלה ו - אתה יודע, ולא איזה תערובת גדולה של תערובות ביניים של כל הדברים האלה. ואחד הרעיונות היסודיים הוא שלמרות שלכל התאים יש את אותו הגנום (בדיוק כמו שאמרת), התאים יכולים להתקיים במצבים שונים אלה והמצבים יציבים. הם כמו ישיבה - בשפה של מערכות דינמיות - בסוג של מושכים יציבים. כך שאם יש הפרעה קטנה או תנודה בריכוז של אחד הרכיבים, זה בסדר, כי זה יציב, והוא יחזור מיד למצב הזה.
(31:43) אז השאלה היא בעצם, אילו סוגי מעגלים יכולים ליצור מספר מושכים או נקודות יציבות כאלה? ואז אם אתה חושב על איך אורגניזמים מתפתחים על פני לוחות זמנים אבולוציוניים, המורכבות יכולה לגדול, נכון? יש לנו הרבה יותר סוגי תאים מאשר זבוב. ועדיין, אנו משתמשים בהרבה מאותם סוגים של גנים וחלבונים כדי ליצור את סוגי התאים האלה כמו הזבוב. אז יש משהו במעגלי הבקרה של גורל התא, הטבעיים שבהם, שהוא סוג של הרחבה או הרחבה. זה מאפשר לאורגניזם לפתח גורלות חדשים לאורך זמן.
(32:18) אז חשבנו על זה כבעיית יסוד לרב-תאית סינתטית. ימין? אם אנחנו הולכים ליצור מערכת רב-תאית סינתטית, אנחנו חייבים להיות מסוגלים להחזיק תא שיכול להיכנס לחבורה של המצבים השונים האלה ולשבת שם ביציבות. וזה יהיה נחמד אם היו לו גם חבורה של נכסים אחרים.
(32:35) היה לי תלמיד מבריק ויצירתי באמת, רון ג'ו. ואתה יודע, הוא הגיע למעבדה, דיברנו על הדברים האלה והוא התחיל לחשוב, בערך, מה יידרש כדי לבנות מערכת גורל של תאים סינתטיים מאפס? אז במקום לנסות להבין איך הדברים הטבעיים עובדים, האם באמת נוכל לבנות אחד? והתחלנו להסתכל על מה שאנשים יודעים על כמה ממערכות השליטה בגורל התא הטבעי המובנות בצורה הטובה ביותר. לדוגמה, יש מערכות השולטות בגורל השריר שדוחפות סוגים מסוימים של תאי גזע להפוך לשריר. ובאופן דומה, ישנם מעגלים אחרים שדוחפים תאים להפוך, תאי גזע להפוך לסוג של נוירון, למשל.
(33:11) ויש משהו מוזר במעגלים האלה בטבע, והוא שחלבוני המפתח השולטים בגורל הם אותו סוג של - חלבונים אלה השולטים בוויסות הגנים, כמו המדכאים והמפעילים עליהם דיברנו מוקדם יותר. אבל יש להם את התכונה המוזרה הזו, כלומר שהם נוטים לתפקד לא לבד, כמו שהם פועלים בחיידקים - אלא באורגניזם רב-תאים, הם נוטים לתפקד בשילוב. אז בעצם, אתה יכול לקבל, אתה יודע, חלבון שיידבק למה שאנו מכנים "דימריז", הוא יידבק לעותק אחר של עצמו, או שהוא יכול להיצמד לעותק של אחד מהחלבונים האחרים. ויש משפחות של חלבונים אלה, והם נדבקים יחד בכל השילובים השונים האלה.
(33:48) אז זה קצת מוזר. למה זה ככה? וזוגות שונים יכולים לעשות דברים שונים. אז יכול להיות שיש זוג אחד שמפעיל ביטוי של אחד מהחלבונים בזוג הזה, וזוג אחר שאולי לא יעשה כלום. זה יכול פשוט להיצמד אחד לשני, ולא להיקשר ל-DNA ולא לעשות כלום.
(34:04) אז אם אתה מסתכל על המעגלים האלה, יש סוג של נושא זה של - המילה המפוארת שבה אנו משתמשים עבור זה היא "דימריזציה קומבינטורית". ואנחנו רואים את זה כנושא במעגלים האלה. וניסינו לחשוב על, כמו, מה העיצוב הפשוט ביותר שמשתמש בנושא הזה אבל עדיין ניתן להנדס אותו לתא יונק? והמעגל שאנו מכנים, בסופו של דבר, "Multifate" מבוסס על הנושא הזה.
(34:25) והרעיון הוא שיש לו קבוצה של חלבונים - אנחנו יכולים פשוט לקרוא להם A, B, C וכן הלאה. וכל אחד מאלה יכול להתאים עם עצמו לדימר. אז זה כמו דימר AA, והדימר הזה יכול להפעיל יותר ביטוי של A. ובאופן דומה B יכול - הגן B ייצור B ו-B יתחבר עם B אחר וייצור BB, ו-BB יפעיל ביטוי של B, וכן הלאה. . אבל החוכמה היא שהם יכולים גם להתחבר זה לזה. אז אתה יכול גם לעשות AB ו-BC, וכן הלאה. והחלבונים האלה בעיצוב הזה לא עושים כלום. אז העובדה שהם לא עושים כלום אומרת שאם אתה עושה הרבה A, זה יכול לספוג כמו ספוג חלק מה-B ולמנוע מ-B לעשות משהו, ולהיפך.
סטרוגאץ: אה, בסדר, נחמד.
אלוביץ' (35:07): זה מה שמוביל לסוג של דינמיקה מעניינת. אתה יכול לנתח את המערכת ומה שאתה מבין זה שהיא יכולה ליצור מספר מושכים, מספר מצבים יציבים. אז לדוגמה, אם אתה לוקח שניים מהחלבונים האלה, רק A ו-B, אתה יכול לעשות שלושה מצבים.
סטרוגאץ (35:23): תן לי לראות אם אני מבין את זה. אז עם A ו-B, אני יכול לעשות, אני יכול לעשות משהו שעושה מה AA, BB או AB. האם אלה השלושה?
אלוביץ' (35:32): כן, יכול להיות לך מצב שיוצר רק A, מצב שיוצר רק B, או מצב שיוצר רק יחס ספציפי של A ו-B ביחד.
סטרוגאץ (35:39): בסדר. אז משניים, לא השתמשנו במילה גורם שעתוק, אתה פשוט קורא להם חלבונים, מה שלא יהיה.
אלוביץ' (35:45): אנחנו יכולים לקרוא להם גורמי תמלול.
Strogatz: בסדר, תקרא להם איך שאתה רוצה.
אלוביץ': כן, הם גורמי תמלול, כן.
סטרוגאץ (35:50): אז היו לך שניים מהם והם יכלו ליצור שלושה, אפשר לומר סוגי תאים?
אלוביץ' (35:54): יש שלוש מדינות. והנקודה היא שאלו יציבים, כך שאם תפריעו לתא הרחק ממנו, תפריעו קצת לרמה של A או B, זה יחזור מיד אחורה, בעצם, לכל אחד מהמצבים האלה,
סטרוגאץ (36:05): ואם לומר "חזור" לכל מה שאתה מדבר עליו - התא כולו מבטא הרבה, הרבה חלבונים אחרים מאלה שאנחנו מדברים עליהם. אז אתה אומר שיש דפוס מסוים של הפעלת גנים עבור כל החלבונים האחרים האלה ללא שם, וזה הדבר שיציב. האם לזה את מתכוונת?
אלוביץ' (36:23): לא לגמרי. כי אני חושב שאנחנו מניחים ששאר התא רק מספק פלטפורמה - זו הנחה - למעגל שלנו. והמצבים האלה הם מצבים של המעגל הרב-גורלי שלנו. וכל השאר בתא הוא סוג של הומיאוסטטי שם, רק מספק את כל המכונות שהמעגל שלנו צריך.
סטרוגאץ (36:42): אני מבין. אז שאר התא רק שומר על האורות.
אלוביץ': בדיוק.
סטרוגאץ (36:46): בזמן שהמעגל הסינטטי הקטן שלך שאתה משחק איתו עושה את שלו, בערך ברקע. והתא הגדול והמסובך הזה הוא כמו, "לא משנה, אפילו לא אכפת לי מזה ומזה." זה דבר כל כך מצחיק שאתה עושה. אתה משחק את המשחק הזה בתוך תא. יש את המילייה של התא, התא עושה את שלו. בינתיים, אתה משחק את המשחק שלך עם זה, כמו, צעצוע-טנקר, מעט מלאכותי - ובכן, "סינטטי" היא המילה היפה יותר - מעגל.
אלוביץ' (37:11): זה נכון. ואם נעשה את זה נכון, אז המעגל הסינתטי שלנו לא מעמיס יותר מדי על שאר התא. אם נעשה זאת בצורה לא טובה, אז אם נביע יתר על המידה את החלבונים האלה, הם יכולים להתחיל לבלבל את התנהגות התא. אז זה תמיד עניין של ביולוגיה סינתטית. זה לא ממש מדויק לומר שזה לא משפיע על שאר התא בכלל. אבל זה סוג של קירוב שאנחנו מנסים להגיע אליו.
סטרוגאץ (37:36): אוקיי, אז הזכרת שעם שני סוגי החלבונים, הצלחת לקבל שלושה מצבים. ואז אתה, מה, אתה משתמש באיזה, אותו טריק עם צבעים, כדי שעכשיו תוכל לראות אותם? או שניסית גם דברים עם שלושה חלבונים וקיבלת שבעה מצבים, אני זוכר נכון?
אלוביץ' (37:51): זה בדיוק נכון. אז אחד הדברים היפים בכל העסק הזה הוא לדמיין מה קורה. אז אנחנו לוקחים A ואנחנו מצמידים לזה חלבון אדום. ב, אנו מצמידים לו חלבון ירוק. ואז אנחנו יכולים למעשה לצפות בתאים ולראות שהם במצב מסוים. ואז נוכל לראות כיצד המצב הזה משתנה עם הזמן כשהתאים גדלים ומתחלקים על ידי יצירת סרטי זמן-lapse במיקרוסקופ. אבל אז מה שבאמת רצינו לבדוק היה האם למערכת הזו יש את תכונת ההרחבה. זה מה שעושה את זה באמת מעניין, זה שאתה יכול להתחיל לקבל יותר ויותר מצבים ככל שאתה מוסיף עוד גורמים. והמדינה, מספר המצבים גדל באופן אקספוננציאלי עם מספר החלבונים הללו. אז אם נוסיף חלבון שלישי, עכשיו בכחול, נוכל לעבור משלושה מצבים לשבעה מצבים. ואם נוסיף חלבון רביעי, נוכל להגיע ל-15 מצבים. זה בערך הולך כמו 2n-1.
סטרוגאץ: או נחמד.
אלוביץ' (38:40): כן. אז זה סוג של צמיחה אקספוננציאלית פחות או יותר, אתה יודע, עד שאתה מגיע לנקודה מסוימת שבה - אתה לא יכול לצמוח אקספוננציאלית לנצח. אבל אתה יכול, באופן עקרוני, לזמן מה. ועכשיו לקחנו את זה לרמה של 15 מדינות במעבדה.
סטרוגאץ (38:53): באמת? הו וואו. זה מדהים. יש לך חלום מה יכול להיות Multifate יום אחד?
אלוביץ' (38:59): ובכן, אנחנו חושבים על זה כמו סוג של בסיס להנדסת מערכות רב-תאיות. ואתה יודע, דרך אחת - שוב, לחשוב על סוג של חזון גדול - יש לנו את המערכת החיסונית, באופן טבעי. ומערכת החיסון שלנו בנויה מתוך מערך עצום, גן חיות גדול של סוגי תאים שונים: תאי הורגים טבעיים ותאי T ותאי B וכל סוגי התאים השונים שמקיימים אינטראקציה זה עם זה.
(39:22) וכך אתה יכול לדמיין לנסות להנדס - מה צריך כדי להנדס מערכת סינתטית שפועלת כמו מערכת החיסון? זה מתגוון למצבים שונים, מספק סוגים שונים של זיכרון? ויכול - מאפשר לתאים להתמחות לביצוע פונקציות שונות? אז אני חושב על Multifate כמספק סוג של בסיס לאיזו מערכת מהונדסת עתידית מסוג זה.
(39:46) ואז, אתה יודע, באופן כללי יותר, אני חושב שאחד התחומים המרגשים כרגע בביולוגיה סינתטית הוא היכולת שלה לאפשר סוגים אחרים של שיטות טיפוליות. אז, אתה יודע, יש משהו שנקרא טיפולי תאים מהונדסים, כלומר, באופן מסוים תכנות תאים לפעול באופן טיפולי. ואחת הדוגמאות הטובות ביותר לכך היא מה שנקרא CAR T-cells. אז זו גישה שאנשים רבים אולי שמעו עליה שבה אתה לוקח את תאי ה-T של המטופל, ואתה מוסיף קולטן מהונדס סינתטי שמכוון לתאים האלה. אז תאי T, אני צריך לומר, יכולים - טובים מאוד בלהרוג תאי מטרה שהם מזהים עם הקולטן הרגיל שלהם. אבל הנה, במקום זאת אתה מכניס קולטן חדש שתכננת, שלוקח את הכוח האדיר הזה שתאי ה-T צריכים להרוג, ומכוון אותו ישירות לתאי הגידול.
(40:37) זו הייתה ממש התקדמות מהפכנית ברפואה. זה היה מאוד מוצלח בלימפומות מסוימות של תאי B. והסיבה שאנשים כל כך מתלהבים מזה היא שבאופן עקרוני, זה סוג של פלטפורמה שאפשר להרחיב אותה כדי למקד לכל מיני סוגי תאים שונים. וזה הפך לסוג של מגרש משחקים, הייתי אומר, לחקר מה ביולוגיה סינתטית יכולה לעשות מבחינה טיפולית. כי הגרסאות הפשוטות ביותר של זה פשוט הכניסו קולטן אחד חדש. אבל אתה יכול גם לדמיין הוספת סוגים שונים של היגיון לתאים האלה כדי שהם יזהו, אתה יודע, "אולי אני אתקוף את הגידול הזה, אבל רק כשאהיה בסביבה מסוימת. ורק כשאני מזהה חלבון אחר שנמצא גם על התא". כמו לעשות קומבינטורית, לוגיקה, שערים AND, שערים OR, כל מיני דברים כאלה.
סטרוגאץ (41:21): תן לי לראות אם אני מבין את הרעיון האחרון, כי זה ממש פרוע. שגדלנו עם הרעיון של תרופות שיכולות לכוון לסוגים ספציפיים של, נניח, תאי גידול. אבל עכשיו אתה אומר שיש תקווה לעצב תרופות, תרופות, שתהיה להן סוג של יכולת הגיונית שהם לא יחפשו בהכרח סוג מסוים של תאים להרוג, וזה כבר יהיה דבר טוב. אבל שהם יכולים אולי לחפש את התא הזה כדי להרוג בנסיבות מסוימות, אבל לא באחרים.
אלוביץ' (41:52): זה חלק מהחלום שאנשים יאהבו. מכיוון שלעתים קרובות זה כאילו, אתה יודע, ייתכן שתא המטרה לא - יכול להיות שאין עליו חלבון יעד קסום אחד שאומר "בוא וקבל אותי". יכול להיות שיש לזה, כאילו, זה יכול להיות שונה ברמות הביטוי של הרבה חלבונים. וייתכן שתצטרך קצת לנסות להתנתק או לנסות להבחין בין התא הזה בצורה מורכבת יותר מתאים אחרים שאינם תאי המטרה שלך. אז זה, במובן מסוים, אתגר גדול ברפואה. לא קשה להרוג תא. קשה להרוג את התא הנכון.
(42:20) תחום נוסף שמאוד התלהבנו ממנו הוא סוג של ביניים בין סוג של תא מהונדס כטיפול, לבין סוג של משהו פשוט יותר כמו ריפוי גנטי. אז ריפוי גנטי אומר שאתה פשוט מכניס גן כדי להחליף גן פגום. אבל אתה יכול גם לדמיין מעגל, מעגל מהונדס שיכול לנסות לתת לך ספציפיות על ידי פעולה בתוך תאים שונים וניסיון לראות "באיזה סוג של תא אני נמצא בתוכו?" אז אם הייתי יכול לזהות את הפעילות של חלבונים שונים, הייתי יכול לומר, "בסדר, זה כנראה תא גידול," כי זה, יש לו רמת פעילות גבוהה מאוד של חבורה של מסלולי איתות אונקוגניים, למשל. ולכן, אני הולך לגרום לתא למות באופן סלקטיבי. אבל אני, אבל אם אני בתא רגיל, אני יכול לדעת שזה תא רגיל, ואני לא אעשה כלום.
(43:04) עבדנו על גישות אחרות כדי לנסות לממש את החזון הזה. וקבוצות רבות מנסות לעשות דברים כאלה. אז זה היה די כיף לנסות לחשוב על זה. אילו סוגי מעגלים אנחנו יכולים ליצור? איך נכניס אותם לתאים? ואיך אנחנו גורמים להם לבצע את משימת ההבחנה הזו של הרג תאי מטרה, אבל לא תאים מחוץ למטרה או לעשות דברים אחרים לצורך העניין?
(43:23) ודבר אחד שבאמת הייתי רוצה להוסיף הוא שבגלל שטכנולוגיות הביולוגיה הסינתטיות האלה הן כל כך חזקות, זה באמת חשוב שבזמן שאנחנו מפתחים אותן, אנחנו באמת מודעים לכך שהן משמשות בבטחה, ושאנחנו ודא שההטבות שלהם מופצות ברחבי העולם, ושהן מוסדרות כראוי.
סטרוגאץ (43:41): וואו, מייקל, תודה על תיאור העולם החדש והאמיץ הזה של ביולוגיה סינתטית. נראה שהשמיים הם הגבול כאן. תודה רבה על שדיברת איתנו היום.
אלוביץ' (43:50): תודה, סטיב. זה היה ממש כיף. אז תודה רבה.
כָּרוֹז (43:55): אם אהבת השמחה של למה, לבדוק את פודקאסט המדע של מגזין Quanta בהנחייתי, סוזן ואלוט, אחת מהמפיקות של התוכנית הזו. כמו כן, ספרו לחברים שלכם על הפודקאסט הזה ותנו לנו לייק או מעקב במקום שבו אתם מאזינים. זה עוזר לאנשים למצוא השמחה של למה פודקאסט.
סטרוגאץ (44: 16): השמחה של למה הוא פודקאסט מ מגזין Quanta, פרסום עצמאי מבחינה עריכה הנתמך על ידי קרן סימונס. להחלטות המימון של קרן סימונס אין השפעה על בחירת הנושאים, האורחים או החלטות עריכה אחרות בפודקאסט זה, או ב מגזין Quanta. השמחה של למה מופק על ידי סוזן ואלוט ופולי סטרייקר. העורכים שלנו הם ג'ון רני ותומס לין, עם תמיכה של מאט קרלסרום, אנני מלצ'ור ואליסון פרשל. מוזיקת הנושא שלנו הולחנה על ידי ריצ'י ג'ונסון. תודה מיוחדת לברט אודום-ריד באולפני קורנל ברודקאסט. הלוגו שלנו הוא של ג'קי קינג. אני המארח שלך סטיב סטרוגאץ. אם יש לך שאלות או הערות עבורנו, אנא שלח לנו דוא"ל לכתובת תודה על הקשבה.
- הפצת תוכן ויחסי ציבור מופעל על ידי SEO. קבל הגברה היום.
- Platoblockchain. Web3 Metaverse Intelligence. ידע מוגבר. גישה כאן.
- מקור: https://www.quantamagazine.org/can-we-program-our-cells-20230308/
- :הוא
- ][עמ'
- $ למעלה
- 1
- 10
- 11
- 28
- 39
- a
- יכולת
- יכול
- אודות
- בנוגע לזה
- בהחלט
- תקציר
- להתאים
- מדויק
- לפעול
- הפעלה
- פעילות
- מעשים
- למעשה
- לקדם
- יתרון
- יתרונות
- להשפיע על
- לאחר
- נגד
- ותיק
- אזעקה
- תעשיות
- מאפשר
- בן ברית
- לבד
- כְּבָר
- בסדר
- תמיד
- מדהים
- כמות
- אנליזה
- לנתח
- ו
- אחר
- לענות
- כל אחד
- בנפרד
- האפליקציה
- תפוח עץ
- יישומים
- החל
- להעריך
- מעריך
- גישה
- גישות
- מתאים
- ARE
- AREA
- אזורים
- סביב
- מערך
- מלאכותי
- AS
- אספקט
- הנחה
- At
- אווירה
- לצרף
- לתקוף
- בחזרה
- רקע
- בַּקטֶרִיָה
- רע
- מבוסס
- בעיקרון
- BE
- יפה
- כי
- להיות
- הופך להיות
- התהוות
- לפני
- להתחיל
- ההתחלה
- להיות
- תאמינו
- הטבות
- הטוב ביותר
- מוטב
- בֵּין
- מעבר
- גָדוֹל
- הגדול ביותר
- מיליארדים
- לאגד
- ביולוגיה
- קצת
- דם
- כָּחוֹל
- ספר
- משעמם
- תַחתִית
- מוֹחַ
- סניף
- אמיץ
- לשבור
- בָּהִיר
- בהיר יותר
- מבריק
- להביא
- מביאים
- מִשׁדָר
- בְּהַרְחָבָה
- חרק
- לִבנוֹת
- בִּניָן
- בונה
- נבנה
- צרור
- ניטל
- עסקים
- by
- C + +
- קליפורניה
- שיחה
- נקרא
- קוראים
- CAN
- יכולות
- קיבולת
- מכונית
- פַּחמָן
- אשר
- לשאת
- מקרה
- מקרים
- זרזים
- לגרום
- גורמים
- תאים
- מסוים
- לאתגר
- סיכוי
- שינוי
- שינויים
- מאופיין
- לבדוק
- כימי
- בחירה
- חַג הַמוֹלָד
- בנסיבות
- עִיר
- קלאסי
- אַקלִים
- שינוי אקלים
- שעון
- שעונים
- עמיתים
- קבוצתי
- COLUMBIA
- שילוב
- שילובים
- איך
- נוחות
- מגיע
- הערות
- Common
- לְהַשְׁווֹת
- תאימות
- לחלוטין
- מורכב
- מורכבות
- מסובך
- רְכִיב
- רכיבים
- מורכב
- לחשב
- המחשב
- מחשבים
- ריכוז
- תנאים
- מחובר
- מכיל
- הקשר
- תמיד
- להמשיך
- נמשך
- לִשְׁלוֹט
- שליטה
- מקובל
- יכול
- קורס
- לִיצוֹר
- נוצר
- יוצרים
- יְצִירָתִי
- קריטי
- מחזור
- עשרות שנים
- החלטות
- עמוק
- העמוק ביותר
- עיכוב
- דרישות
- תלוי
- למטה
- לתאר
- מְתוּאָר
- עיצוב
- עקרונות עיצוב
- מעוצב
- תכנון
- עיצובים
- נחוש
- לפתח
- מפתחת
- מכשיר
- התקנים
- DID
- למות
- הבדל
- אחר
- להבחין
- מובחנים
- תקציר
- ישירות
- גילה
- מגלה
- מופץ
- ה-DNA
- לא
- עושה
- לא
- מטה
- חלום
- תרופה
- סמים
- דינמיקה
- כל אחד
- מוקדם יותר
- עריכה
- השפעה
- יעילות
- אֶלֶקטרוֹנִי
- מכשירי חשמל
- אלקטרונים
- אלמנטים
- אמייל
- לאפשר
- מהנדס
- הנדסה
- מספיק
- לְהַבטִיחַ
- סביבה
- סביבתי
- סביבות
- באותה מידה
- משוואות
- שווה
- תקופה
- במיוחד
- חיוני
- אֲפִילוּ
- בסופו של דבר
- אי פעם
- כל
- כולם
- הכל
- אבולוציה
- להתפתח
- התפתח
- בדיוק
- דוגמה
- דוגמאות
- אלא
- נרגש
- מרגש
- לְהַרְחִיב
- ניתן להרחבה
- לצפות
- לְנַסוֹת
- לחקור
- היכרות
- מעריכי
- אקספוננציאלית
- חשוף
- אקספרס
- ביטא
- יוצא דופן
- עין
- הקל
- מפעלים
- גורמים
- מפעל
- ליפול
- משפחות
- מקסים
- מהר יותר
- גורל
- חביב
- מאפיין
- מָשׁוֹב
- שדה
- שדות
- תרשים
- ראשון
- לסדר
- גמישות
- פליפ
- צף
- תזרים
- להשתנות
- תנודות
- תנודות
- להתמקד
- מרוכז
- לעקוב
- מזון
- בעד
- לנצח
- טופס
- קרן
- רביעית
- חבר
- חברים
- החל מ-
- מלא
- כֵּיף
- פונקציה
- פונקציונלי
- פונקציות
- יסודי
- מימון
- מצחיק
- היתוך
- עתיד
- גאדג'טים
- מִשְׂחָק
- גייטס
- בדרך כלל
- ליצור
- מייצר
- גנרטורים
- לקבל
- מקבל
- ענק
- לתת
- נותן
- ברחבי עולם
- Go
- מטרה
- Goes
- הולך
- טוב
- לתפוס
- בוגר
- גרף
- גדול
- ירוק
- קבוצה
- לגדול
- מְגוּדָל
- גדל
- צמיחה
- אוֹרֵחַ
- אורחים
- לפרוץ
- שיער
- יד
- לקרות
- מתרחש
- קורה
- קשה
- יש
- יש
- ראש
- נשמע
- שמיעה
- לֵב
- לעזור
- עזר
- מועיל
- עוזר
- כאן
- גָבוֹהַ
- היסטוריה
- מחזיק
- לקוות
- אני מקווה
- המארח
- אירח
- שעות
- איך
- איך
- http
- HTTPS
- עצום
- בן אנוש
- i
- חולה
- רעיון
- רעיונות
- מערכת חיסונית
- פְּגִיעָה
- חשוב
- שהוטל
- in
- באחר
- כולל
- להגדיל
- מדהים
- עצמאי
- בנפרד
- להשפיע
- מידע
- תשתית
- למשל
- במקום
- מכון
- אינטראקציה
- אינטראקציה
- יחסי גומלין
- מעוניין
- מעניין
- מהותי
- באופן מהותי
- סוגיה
- IT
- שֶׁלָה
- עצמו
- ג'ון
- ג'ונסון
- קפיצות
- רק אחד
- שמור
- שמירה
- מפתח
- יֶלֶד
- לַהֲרוֹג
- סוג
- המלך
- לדעת
- ידוע
- מעבדה
- עבודה
- שפה
- גָדוֹל
- אחרון
- מוביל
- לִלמוֹד
- למד
- מאפשר לי
- רמה
- רמות
- החיים
- כמו
- סביר
- להגביל
- האזנה
- קְצָת
- כבד
- חי
- הגיוני
- סֵמֶל
- עוד
- נראה
- הסתכלות
- להפסיד
- לאבד
- מגרש
- אהבה
- מק
- מכונות
- מכונה
- עשוי
- מגזין
- קסם
- לעשות
- עושה
- עשייה
- רב
- הרבה אנשים
- חומרים
- מתמטיקה
- מתימטי
- מתימטיקה
- דבר
- אומר
- בינתיים
- רפואי
- יישומים רפואיים
- רפואה
- זכרון
- מוּזְכָּר
- שיטות
- מיכאל
- מיקרוסקופ
- יכול
- אכפת לי
- מינימלי
- לשנות
- מולקולרי
- מולקולה
- רֶגַע
- יותר
- בוקר
- רוב
- סרט
- סרטים
- מספר
- כלי נגינה
- שם
- טבעי
- טבע
- בהכרח
- הכרחי
- צורך
- צרכי
- שלילי
- באופן שלילי
- רשת
- נוירונים
- חדש
- הבא
- רעש
- נוֹרמָלִי
- מספר
- ים
- קטטה
- of
- בסדר
- זקן
- on
- ONE
- להפעיל
- פועל
- מערכת הפעלה
- מול
- אופטימיזציה
- מסלול
- אחר
- אחרים
- אַחֶרֶת
- בחוץ
- שֶׁלוֹ
- זוגות
- פרדיגמה
- הורים
- חלק
- מסוים
- במיוחד
- חלקים
- צד
- תבנית
- אֲנָשִׁים
- לְבַצֵעַ
- תקופה
- אדם
- אישי
- פילוסופיה
- פיסיקה
- חתיכות
- מקום
- פלסטיק
- פלטפורמה
- אפלטון
- מודיעין אפלטון
- אפלטון נתונים
- לְשַׂחֵק
- שחקנים
- משחק
- אנא
- תקע
- פודקאסט
- Podcasting
- נקודה
- נקודת מבט
- נקודות
- אוכלוסייה
- אפשרי
- פוטנציאל
- פוטנציאל
- כּוֹחַ
- חזק
- בדיוק
- צפוי
- נוכחות
- להציג
- יפה
- למנוע
- עקרון
- עקרונות
- כנראה
- בעיה
- בעיות
- תהליך
- תהליך
- לייצר
- מיוצר
- מפיק
- פרופסור
- תָכְנִית
- מתוכנה
- תכנות
- תוכניות
- הבטחה
- כמו שצריך
- נכסים
- רכוש
- מוּגָן
- חֶלְבּוֹן
- חלבונים
- מספק
- מתן
- פרסום
- דחוף
- גם
- מכניס
- פיתון
- קוונטמגזין
- שאלה
- שאלות
- רדיו
- אקראי
- אקראי
- מהר
- ציון
- במקום
- יחס
- לְהַגִיעַ
- תגובה
- תגובות
- ממשי
- זמן אמת
- להבין
- הבין
- טעם
- סיבות
- לסכם
- לאחרונה
- להכיר
- Red
- משטר
- רגיל
- מוסדר
- תקנה
- רגולטורים
- רגולטורים
- לזכור
- זוכר
- להחליף
- נדרש
- מחקר
- REST
- מהפכני
- עשיר
- תפקיד
- תפקידים
- נתיבים
- הפעלה
- בבטחה
- אמר
- אותו
- ארגז חול
- אומר
- להרחבה
- מדע
- מַדְעָן
- מדענים
- נראה
- מבחר
- תחושה
- שרות
- סט
- הצבה
- שבע
- כמה
- שיתוף
- שיתוף
- הסטה
- צריך
- לְהַצִיג
- צד
- דומה
- באופן דומה
- פָּשׁוּט
- בפשטות
- since
- יחיד
- ישיבה
- עור
- הם
- לִישׁוֹן
- להאט
- So
- עד כה
- פִּתָרוֹן
- כמה
- ביום מן הימים
- משהו
- קול
- לדבר
- מיוחד
- מתמחים
- ספציפי
- במיוחד
- ספֵּצִיפִיוּת
- Spotify
- יציבות
- יציב
- התחלה
- החל
- החל
- התחלות
- מדינה
- הברית
- להשאר
- יציב
- גֶזַע
- תאי גזע
- שלב
- סטיב
- עוד
- סיפור
- אסטרטגיות
- אִסטרָטֶגִיָה
- מִבנִי
- סטודנט
- האולפנים
- נושא
- מוצלח
- כזה
- מספיק
- תמיכה
- נתמך
- תומך
- סוזן
- קיימות
- סינטטי
- מערכת
- מערכות
- תאי T
- לקחת
- לוקח
- נטילת
- לדבר
- מדבר
- שיחות
- יעד
- מטרות
- המשימות
- טכנולוגיות
- טכנולוגיה
- מונחים
- מבחן
- תודה
- זֶה
- השמיים
- המדינה
- שֶׁלָהֶם
- אותם
- נושא
- עצמם
- שם.
- לכן
- אלה
- דבר
- דברים
- חושב
- שְׁלִישִׁי
- מחשבה
- שְׁלוֹשָׁה
- דרך
- בכל
- זמן
- ל
- היום
- יַחַד
- גַם
- כלים
- נושאים
- לְגַמרֵי
- לקראת
- לשנות
- טרנספורמציה
- טריליונים
- נָכוֹן
- תור
- פנייה
- סוגים
- תחת
- להבין
- הבנה
- הבין
- ללא שם
- us
- להשתמש
- משתמש
- מגוון
- לצפיה
- כמעט
- נראה
- חזון
- לחכות
- רציתי
- שעון
- דֶרֶך..
- דרכים
- webp
- ברוך הבא
- טוֹב
- מוגדר היטב
- מה
- מה
- אם
- אשר
- בזמן
- כל
- בר
- יצטרך
- חלונות
- חוט
- עם
- בתוך
- לְלֹא
- Word
- מילים
- תיק עבודות
- לעבוד יחד
- עובד
- עובד
- עוֹלָם
- היה
- לכתוב
- טעות
- שנים
- אתה
- עצמך
- זפירנט
- גן חיות