סוג חדש של מודל ממוחשב שיכול לחשוף נזקי קרינה ברמה התאית יכול לשפר את תוצאות הקרנות לחולי סרטן ריאות.
רומן באואר, מדען מוח חישובי ב- אוניברסיטת סורי בבריטניה, בשיתוף עם מרקו דוראנטה ו ניקולו קוניו החל מ- GSI Helmholtzzentrum für Schwerionenforschung בגרמניה, יצרו את המודל, המדמה כיצד קרינה מקיימת אינטראקציה עם הריאות על בסיס תא לתא.
למעלה ממחצית מכלל החולים בסרטן הריאות מטופלים באמצעות הקרנות. למרות שגישה זו יעילה, היא מותירה עד 30% מהנמענים עם פציעות הנגרמות מקרינה. אלה עלולים לעורר מצבים חמורים המשפיעים על הנשימה, כגון פיברוזיס - שבו רירית המכתשות (שקיות האוויר) בריאות מתעבה ומתקשה - ודלקת ריאות - כאשר דפנות המכתשות מתדלקות.
על מנת להגביל את נזקי הקרינה לרקמה בריאה תוך הרג תאים סרטניים, טיפול בקרינה מועבר במספר "שברים" נפרדים. זה מאפשר מתן מנה גבוהה יותר - ולכן יעילה יותר - בסך הכל מכיוון שחלק מהתאים הבריאים הפגועים יכולים לתקן את עצמם בין כל חלק.
נכון לעכשיו, סכימות חלוקת הקרנות נבחרות על סמך ניסיון העבר ומודלים סטטיסטיים כלליים, ולכן אינן מותאמות למטופלים בודדים. לעומת זאת, ניתן להשיג רפואה מותאמת אישית הודות למודל החדש הזה, שכדוראנטה, מנהל ה- המחלקה לביופיזיקה ב-GSI מסביר, בוחן "רעילות ברקמות החל מהתגובות התאיות הבסיסיות ולכן [מסוגל] לחזות מה קורה לכל חולה" כאשר נבחרות סכימות חלוקה שונות.
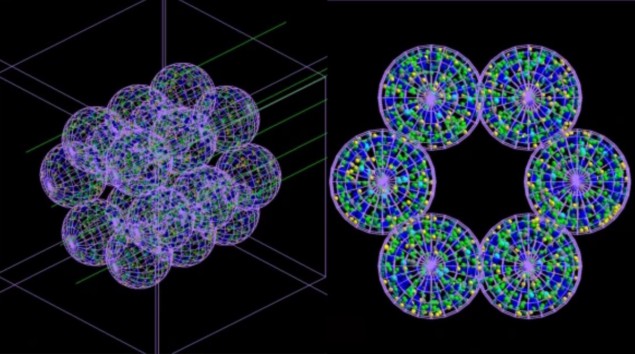
הצוות פיתח מודל "מבוסס סוכן" (ABM) המורכב מיחידות או סוכנים נפרדים באינטראקציה - שבמקרה זה מחקים תאי ריאה - יחד עם סימולטור מונטה קרלו. ה-ABM, המתואר ב רפואת תקשורת, בונה ייצוג של מקטע מכתשית המורכב מ-18 אלווולי כל אחד בקוטר של 260 מיקרומטר. לאחר מכן, סימולציות של מונטה קרלו של הקרנה של alveoli אלו מתבצעות בקנה מידה מיקרוסקופי וננוסקופי, ומידע על מנת הקרינה המועברת לכל תא והתפלגותו מוזנת חזרה ל-ABM.
ה-ABM משתמש במידע זה כדי להבין אם כל תא יחיה או ימות, ומוציא את התוצאות הסופיות בצורה של תמונה תלת מימדית. באופן מכריע, המודל המצמד יכול לדמות את חלוף הזמן ובכך להראות את חומרת נזקי הקרינה - ואת התקדמות המצבים הרפואיים שהוא עלול לגרום - שעות, ימים, חודשים ואפילו שנים לאחר הטיפול.
"מה שמצאתי מרגש מאוד הוא שהסימולציות החישוביות הללו הניבו למעשה תוצאות שהתואמו עם תצפיות ניסוי שונות מקבוצות שונות, מעבדות ובתי חולים. כך שבאופן עקרוני ניתן להשתמש בגישה החישובית שלנו בתוך סביבה קלינית", אומר באואר, דובר הארגון הבינלאומי שיתוף פעולה של BioDynaMo, שמטרתה להכניס שיטות חישוביות חדשות לבריאות באמצעות חבילת התוכנה המשמשת לבניית מודל זה.
באואר החל לעבוד על מודלים של סרטן חישובי לאחר שחבר קרוב מת מהמחלה בגיל 34 בלבד. "כל סרטן הוא שונה וכל אדם הוא שונה, עם איברים בצורת שונה, נטיות גנטיות ואורח חיים שונה", הוא מסביר. תקוותו היא שניתן יהיה להזין מידע מסריקות, ביופסיות ובדיקות אחרות לתוך הדגם החדש כדי לספק תמונה של כל אדם. לאחר מכן ניתן ליצור פרוטוקול טיפול בעזרת בינה מלאכותית, שיוציא תוכנית טיפול מותאמת באופן הדוק, המשפרת את סיכויי ההישרדות של המטופל.
תכנון ספציפי למטופל יכול לשפר את תוצאות הטיפול בהקרנות
באואר מחפש כעת משתפי פעולה מדיסציפלינות אחרות, כולל פיזיקה, כדי לעזור להתקדם לקראת ניסוי קליני בעקבות חולי סרטן ריאות במשך מספר שנים. בינתיים, הצוות מתכוון להרחיב את השימוש במודל לתחומי רפואה נוספים.
דוראנט, למשל, מקווה לחקור זיהום ויראלי עם מודל ריאות זה מכיוון שהוא "עשוי לחזות את דלקת הריאות שנגרמה על ידי זיהום COVID-19". בינתיים, באואר החלה לדמות התפתחות של מעגלים במוחם של פגים, במטרה להבין טוב יותר "באיזו נקודת זמן להתערב וכיצד".
- הפצת תוכן ויחסי ציבור מופעל על ידי SEO. קבל הגברה היום.
- PlatoData.Network Vertical Generative Ai. העצים את עצמך. גישה כאן.
- PlatoAiStream. Web3 Intelligence. הידע מוגבר. גישה כאן.
- PlatoESG. פחמן, קלינטק, אנרגיה, סביבה, שמש, ניהול פסולת. גישה כאן.
- PlatoHealth. מודיעין ביוטכנולוגיה וניסויים קליניים. גישה כאן.
- מקור: https://physicsworld.com/a/modelling-lung-cells-could-help-personalize-radiotherapy/
- :יש ל
- :הוא
- :לֹא
- $ למעלה
- 135
- 3d
- a
- יכול
- אודות
- AC
- הושג
- למעשה
- מנוהל
- להשפיע על
- לאחר
- זקן
- סוכנים
- מטרות
- AIR
- תעשיות
- מאפשר
- למרות
- an
- ו
- כל
- גישה
- ARE
- אזורים
- AS
- At
- בחזרה
- מבוסס
- בסיסי
- בסיס
- BE
- כי
- להיות
- החל
- התחיל
- מוטב
- בֵּין
- נשימה
- להביא
- לִבנוֹת
- בונה
- by
- CAN
- מחלת הסרטן
- תאים סרטניים
- נשא
- מקרה
- לגרום
- תא
- תאים
- סיכויים
- נבחר
- קליני
- סְגוֹר
- מקרוב
- שיתוף פעולה
- משתפי פעולה
- חישובית
- המחשב
- תנאים
- מורכב
- לעומת זאת
- יכול
- יחד
- תקופת הקורונה
- נוצר
- באופן מכריע
- כיום
- נזק
- ימים
- נתן
- מַחלָקָה
- מְתוּאָר
- מפותח
- צעצועי התפתחות
- למות
- מת
- אחר
- מְנַהֵל
- דיסציפלינות
- מַחֲלָה
- הפצה
- מנה
- כל אחד
- אפקטיבי
- אֲפִילוּ
- כל
- מרגש
- לְהַרְחִיב
- ניסיון
- ניסיוני
- מסביר
- הפד
- סופי
- הבא
- בעד
- טופס
- מצא
- שבריר
- חבר
- החל מ-
- הכללה
- גנטי
- גרמניה
- מטרה
- קבוצה
- חצי
- קורה
- he
- בריאות
- בריא
- לעזור
- גבוה יותר
- שֶׁלוֹ
- לקוות
- מקווה
- בתי חולים
- שעות
- איך
- HTTPS
- i
- לשפר
- משפר
- in
- כולל
- בנפרד
- מידע
- פציעות
- למשל
- מתכוונת
- אינטראקציה
- אינטראקטיבי
- ברמה בינלאומית
- להתערב
- אל תוך
- סוגיה
- IT
- שֶׁלָה
- jpg
- רק
- הרג
- מעבדות
- רמה
- אורח חיים
- להגביל
- בטנה
- לינקדין
- לחיות
- נראה
- מתאים
- max-width
- מאי..
- בינתיים
- רפואי
- רפואה
- שיטות
- מִיקרוֹסקוֹפִּי
- מודל
- דוּגמָנוּת
- מודלים
- חודשים
- יותר
- המהלך
- טבע
- חדש
- הבא
- of
- on
- אופטימיזציה
- or
- להזמין
- אחר
- שלנו
- הַחוּצָה
- תוצאות
- תפוקה
- פלטים
- יותר
- מקיף
- מעבר
- עבר
- חולה
- חולים
- אדם
- אישית
- אישית
- פיסיקה
- עולם הפיזיקה
- תמונה
- תכנית
- תכנון
- אפלטון
- מודיעין אפלטון
- אפלטון נתונים
- נקודה
- לחזות
- מוקדם מדי
- עקרון
- התקדמות
- פרוטוקול
- לספק
- רדיותרפיה
- תגובות
- נמענים
- לתקן
- נציגות
- תוצאות
- לגלות
- אומר
- סולם
- סריקות
- תוכניות
- מחפשים
- קטע
- נפרד
- רציני
- הצבה
- כמה
- מְעוּצָב
- לְהַצִיג
- לדמות
- סימולציות
- מדמה
- So
- תוכנה
- כמה
- דובר
- החל
- סטטיסטי
- עוד
- לימוד
- כזה
- מערכת
- Surrey
- הישרדות
- מותאם
- נבחרת
- בדיקות
- תודה
- זֶה
- השמיים
- בריטניה
- עצמם
- אז
- תרפיה
- לכן
- אלה
- זֶה
- תמונה ממוזערת
- כָּך
- זמן
- ל
- לקראת
- טופל
- טיפול
- מִשׁפָּט
- להפעיל
- נָכוֹן
- סוג
- Uk
- הבנה
- יחידות
- להשתמש
- מְשׁוּמָשׁ
- שימושים
- באמצעות
- שונים
- מאוד
- באמצעות
- נגיפי
- מה
- מתי
- אם
- אשר
- בזמן
- עם
- בתוך
- תיק עבודות
- להתאמן
- עובד
- עוֹלָם
- היה
- שנים
- זפירנט