放射性同位体で覆われた自走式の粒子の軍隊が、塵の斑点の 2500 ~ 10,000 倍小さいもので、体内に注入されると、がん性腫瘍を探して付着し、がん性腫瘍を破壊する様子を想像してみてください。サイエンスフィクションのように聞こえますか?膀胱がんのマウスの場合はそうではありません。
スペインの研究者らは、放射性ヨウ素を含み、尿素と反応すると飛び出すナノ粒子には、膀胱癌性腫瘍と健康な組織を区別する能力があると報告している。これらの「ナノボット」は腫瘍の細胞外マトリックスに侵入して内部に蓄積し、放射性核種治療が正確な標的に到達することを可能にします。で行われた研究では、 カタロニア生物工学研究所 バルセロナの (IBEC) では、この治療を単回投与されたマウスは、未治療の動物と比較して膀胱腫瘍のサイズが 90% 減少しました。
この新しいアプローチは、いつか膀胱がんの治療に革命をもたらすかもしれません。世界保健機関の世界がん観測所によると、膀胱がんは世界で600,000番目に多いがんで、2022年には世界で220,000万人以上が新たに診断され、XNUMX万人以上が死亡している。
症例の75%を占める非筋層浸潤性膀胱がんは、現在、腫瘍切除とそれに続く膀胱への化学療法薬または免疫療法薬の膀胱内注射によって治療されています。しかし、薬物送達は、尿路上皮(尿路の内側を裏打ちする組織)の透過性が低く、尿の内容物が満たされ、その後薬物が洗い流されるため、特に困難です。また、このプロセスは患者にとっても不快なものであり、薬が膀胱壁の全側面に届くようにうつ伏せになりながら時々体を回転させる必要がある。治療後、30 年以内に再発するリスクは 70 ~ XNUMX% あります。
臨床転帰を改善するために、主任研究者は、 サミュエル・サンチェス 博士らは、革新的でより効果的な膀胱がん治療法を開発し、その過程で再発率を低下させることを目指しています。さらに、単回投与療法により、現在14~XNUMX回の入院が必要な治療費が大幅に削減される。
研究チームは、表面にさまざまな機能成分を備えたメソポーラスシリカナノ粒子からナノボットを作成した。これらには、PET 可視化や放射性核種治療のための放射性同位体や、尿中の尿素と反応してナノボットの推進を可能にするタンパク質ウレアーゼが含まれます。
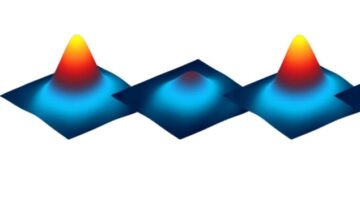
書き込む 自然ナノテクノロジー、研究者らは、300 mM 尿素を含む溶液にナノボットの液滴を添加すると、ナノボットが群がる動きを示し、活発で活発な前線と三次元渦を形成したと報告しています。尿素がなければ、ナノボットは単に添加部位の近くに沈降するだけであった。
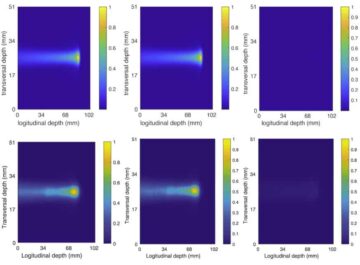
ナノボットが腫瘍に到達できるかどうかを調べる インビボの、チームは腫瘍を持ったマウスでの行動を評価しました。陽電子放出断層撮影法(PET)画像は、放射性標識ナノボットからのシグナルが、MRIで測定された腫瘍の位置と同じ位置にあり、主に標的腫瘍部位で放射能が見られることを示した。ナノボットと尿素を注射したマウスのみが腫瘍塊へのかなりの蓄積を示しました。ナノボットは水で送達され、対照ナノ粒子(ウレアーゼなし)は水または尿素で送達されましたが、腫瘍への取り込みは最小限でした。
研究者らは、ナノボットの機動性が腫瘍塊への侵入に役立つと示唆している。 「ナノボットには腫瘍を認識するための特異的な抗体が欠けており、腫瘍組織は通常、健康な組織よりも硬いですが、膀胱腫瘍の場合はそうではありません」と共筆著者は説明する メリチェル セラ カサブランカス IBECの。 「私たちは、これらのナノロボットが自己推進型の化学反応によって局所的に pH を上昇させることにより、腫瘍の細胞外マトリックスを破壊できることを観察しました。この現象により、腫瘍の侵入が促進されました。」研究者らは、ナノボットは尿路上皮に壁であるかのように衝突するが、より海綿状である腫瘍を貫通すると考えている。
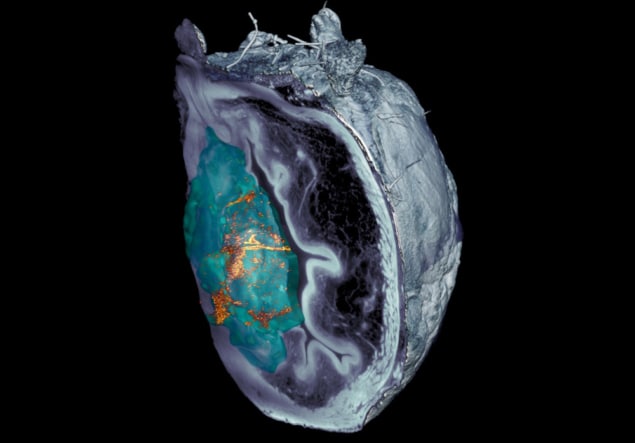
研究チームは、解剖した組織の顕微鏡画像からナノボットを特定するのは困難だったと指摘している。共焦点光学顕微鏡技術が失敗した後、研究者たちは バルセロナ IRB は、膀胱のさまざまな層をスキャンして器官全体の 3D 再構成を作成できる、平面レーザー照明に基づくライトシートベースの顕微鏡システムを開発しました。
「私たちが開発した散乱弾性ライトシート顕微鏡システムにより、腫瘍自体によって反射される光を除去することができ、前例のない解像度で、事前の標識なしで臓器全体のナノ粒子を識別して位置を特定できるようになりました。」 ジュリアン・コロンベリ IRBバルセロナより。

操作されたバクテリアは癌を殺す放射性同位体を腫瘍に引き寄せます
この技術の治療効果を評価するために、研究チームはナノボットにヨウ素 131 (131I(放射性核種治療に一般的に使用される放射性同位体)を腫瘍担持マウスに投与しました。減量による治療 131尿素中のナノボットは腫瘍の増殖を阻止したが、高用量では 131尿素中で投与されたα-ナノボットは、未治療の動物と比較して腫瘍体積のほぼ90%の減少をもたらした。
サンチェスは言う 物理学の世界 研究チームの次のステップは、現在化学療法で使用されている小さな薬剤をカプセル化し、薬剤キャリアとしてのナノボットの効率をテストし続けることだという。彼らは最終的にはナノボットをスケールアップし、IBECのスピンオフを通じて今後3~4年以内に最初の臨床試験に向けて規制経路を研究するつもりだ。 ナノボット治療学.
- SEO を活用したコンテンツと PR 配信。 今日増幅されます。
- PlatoData.Network 垂直生成 Ai。 自分自身に力を与えましょう。 こちらからアクセスしてください。
- プラトアイストリーム。 Web3 インテリジェンス。 知識増幅。 こちらからアクセスしてください。
- プラトンESG。 カーボン、 クリーンテック、 エネルギー、 環境、 太陽、 廃棄物管理。 こちらからアクセスしてください。
- プラトンヘルス。 バイオテクノロジーと臨床試験のインテリジェンス。 こちらからアクセスしてください。
- 情報源: https://physicsworld.com/a/self-propelling-nanobots-shrink-bladder-tumours-in-mice-by-90/
- :は
- :not
- $UP
- 000
- 10
- 135
- 14
- 2022
- 220
- 300
- 3d
- 600
- a
- 能力
- 従った
- アカウント
- 累積する
- 累積
- アクティブ
- 追加されました
- 添加
- さらに
- 投与
- 後
- 目指す
- すべて
- 許可
- また
- an
- および
- 動物
- アプローチ
- です
- 軍
- 逮捕された
- AS
- 評価された
- At
- アタッチ
- 引き付ける
- 著者
- 細菌
- バルセロナ
- ベース
- 行動
- 信じる
- の間に
- ボディ
- ボディ
- ブレーク
- 焙煎が極度に未発達や過発達のコーヒーにて、クロロゲン酸の味わいへの影響は強くなり、金属を思わせる味わいと乾いたマウスフィールを感じさせます。
- by
- 缶
- 癌
- できる
- キャリア
- 場合
- 例
- 挑戦
- 化学物質
- 臨床
- 臨床試験
- 同僚
- 衝突する
- COM
- コマンドと
- 一般に
- 比べ
- コンポーネント
- 実施
- コンテンツ
- 続ける
- コントロール
- 費用
- 作成した
- 作成
- 現在
- 中
- 死亡
- 配信
- 配達
- 決定
- 開発する
- 発展した
- 異なります
- 見分けます
- 線量
- ダウン
- 薬
- 薬物
- 原因
- ほこり
- 効果
- 効果的な
- 効率
- 排除する
- エミッション
- enable
- 使用可能
- 可能
- 有効にする
- 全体
- EU
- 評価する
- 最終的に
- 調べる
- 展示した
- 説明
- Failed:
- フィクション
- 充填
- 名
- 五
- 続いて
- フォロー中
- 4
- から
- 機能的な
- グローバル
- グローバルに
- 大きい
- 成長性
- 持っていました
- 持ってる
- 健康
- 健康
- ことができます
- しかしながら
- HTTPS
- 識別する
- 識別
- if
- 画像
- 免疫療法
- 改善します
- in
- include
- の増加
- 情報
- 革新的な
- 内部
- 予定
- に
- 問題
- IT
- ITS
- 自体
- JPG
- ラベリング
- 欠如
- レーザー
- 層
- ツェッペリン
- 光
- ような
- ライニング
- 局部的に
- ロー
- 質量
- マトリックス
- 最大幅
- 五月..
- 顕微鏡検査
- 最小限の
- モビリティ
- 他には?
- 最も
- モーション
- MRI検査
- 自然
- 近く
- ほぼ
- 必要
- 新作
- 次の
- 注意
- 小説
- 展望台
- of
- on
- ONE
- の
- or
- 成果
- が
- 特に
- 経路
- 患者
- 浸透
- 現象
- 物理学
- 物理学の世界
- プラトン
- プラトンデータインテリジェンス
- プラトデータ
- さらに
- 位置
- 正確な
- 主に
- 校長
- 事前の
- プロセス
- 推進します
- 推進
- タンパク質
- 価格表
- リーチ
- 反応
- 反応する
- 受け入れ
- 認める
- 再発
- 減らします
- 削減
- 反映
- レギュレータ
- レポート
- 必要
- 研究者
- 解像度
- 革命を起こす
- リスク
- 言う
- 規模
- スキャニング
- 散在する
- 科学
- サイエンスフィクション
- を検索
- 見て
- 示されました
- 側面
- 信号
- 著しく
- 単に
- ウェブサイト
- SIX
- サイズ
- 小さい
- より小さい
- So
- 溶液
- 音
- スペイン
- 特定の
- ステップ
- 勉強
- それに続きます
- かなりの
- 示唆する
- ターゲット
- チーム
- テクニック
- 伝える
- test
- より
- それ
- 世界
- アプリ環境に合わせて
- それら
- 自分自身
- 治療
- ボーマン
- 彼ら
- この
- 三
- 三次元の
- 介して
- 全体
- サムネイル
- <font style="vertical-align: inherit;">回数</font>
- 〜へ
- に向かって
- 治療
- 治療
- トリートメント
- 試験
- true
- 順番
- 一般的に
- 前例のない
- に
- 摂取
- us
- 中古
- さまざまな
- 、
- 可視化
- ボリューム
- 壁
- ました
- 水
- we
- した
- いつ
- かどうか
- which
- while
- 以内
- 無し
- 世界
- でしょう
- 年
- ゼファーネット