워싱턴 DC - 췌장암은 가장 치명적인 암 유형 중 하나입니다. 미국에서는 다음과 같이 추정됩니다. 88 % 이상 의 사람들이 진단 후 5년 이내에 질병으로 사망할 것입니다. 이러한 암울한 예후의 한 가지 이유는 대부분의 췌장암이 질병이 이미 신체의 다른 부위로 퍼지거나 전이된 후에 진단되기 때문입니다. 또 다른 이유는 췌장암이 표준 항암제에 내성을 보이는 경우가 많아 치료가 특히 어렵다는 것입니다.
국립생체의학영상생명공학연구소(니빕) 자금을 지원받은 연구자들은 이 치명적인 질병을 치료하기 위한 새로운 방법을 개발하고 있습니다. 그들의 공부, 최근에 출판됨 자연 생체 공학, 췌장암의 여러 마우스 모델에서 주사 가능한 방사성 젤과 전신 화학 요법을 결합했습니다. 이 치료는 평가된 모든 모델에서 종양 퇴행을 가져왔으며, 이는 유전적으로 다양하고 공격적인 유형의 암에 대한 전례 없는 결과였습니다.
NIBIB의 Discovery Science & Technology 부문 이사인 David Rampulla 박사는 “방사선 치료는 일반적으로 외부에서 전달되는데, 이는 건강한 조직을 방사선에 노출시키고 종양이 받는 선량을 제한하여 궁극적으로 그 효과를 제한합니다.”라고 말했습니다. “이 전임상 연구에서 조사된 방사성 생체재료는 종양에 직접 주입될 수 있어 국소적인 접근이 가능합니다. 게다가 이 생분해성 생체재료는 다른 이식형 방사선 치료법보다 더 높은 누적 방사선량을 허용합니다.”
방사선원을 신체 내부에 배치하는 근접 치료는 다양한 유형의 암을 치료하는 데 사용할 수 있습니다. 예를 들어, 초기 단계의 전립선암은 방사성 물질이 포함된 많은 작은 금속 씨앗을 전립선에 이식하는 '종자' 근접 치료로 치료할 수 있습니다. 이 씨앗은 건강한 조직의 방사선 노출을 제한할 수 있지만, 씨앗의 금속 케이스는 암세포를 죽이는 데 더 효과적인 알파 및 베타 방출체로 알려진 강력한 방사선 입자의 사용을 방지합니다. 또한 크기가 작기 때문에 전립선암 치료에는 일반적으로 약 100개의 씨앗이 필요합니다(각 개별 씨앗에는 주사가 필요함). 현재까지 근접치료 접근법은 췌장암 환자의 임상 결과를 개선하지 못했습니다.
현재 연구에서는 새로운 유형의 근접치료를 조사하고 있습니다. 금속 종자나 카테터를 사용하여 방사선을 전달하는 대신, 연구 저자들은 종양에 직접 주입되는 방사성 생체고분자의 사용을 조사하고 있습니다. 생분해성 외에도 생체고분자는 독특한 특성을 가지고 있습니다. 즉, 실온의 액체에서 체온으로 따뜻해지면 젤 같은 상태로 전환되도록 설계되었습니다. 생체고분자는 굳어지면서 종양 내에 머물며 주변의 건강한 조직으로 쉽게 퍼지지 않습니다.
듀크대학교에서 이 연구를 수행한 제1저자 Jeff Schaal 박사는 “우리의 생체고분자는 우리 몸 전체의 결합 조직에서 발견되는 풍부한 단백질인 엘라스틴에서 파생됩니다.”라고 설명했습니다. “이 바이오폴리머의 구성을 조정함으로써 우리는 액체에서 젤로 전환되는 정확한 온도를 제어할 수 있습니다. 그리고 방사성 폴리머를 보호용 금속 씨드 안에 넣지 않기 때문에 더 다양하고 더 강력한 동위원소를 사용할 수 있어 기존 씨드 근접 치료보다 더 높은 방사선량을 전달할 수 있습니다.”
이 개념 증명 처리에 사용되는 방사성 동위원소는 베타 입자로 알려진 고에너지 입자를 방출하는 요오드-131(또는 I-131)입니다. 베타 입자는 DNA 손상을 일으키고 조사된 세포를 죽이지만 매우 멀리 이동할 수는 없습니다. 단지 몇 밀리미터에 불과합니다(그래서 표적을 벗어난 독성은 제한됩니다). I-131은 수십 년 동안 갑상선암 치료에 사용되어 왔으며 안전성 프로필이 잘 확립되어 있다고 Schaal은 말했습니다.
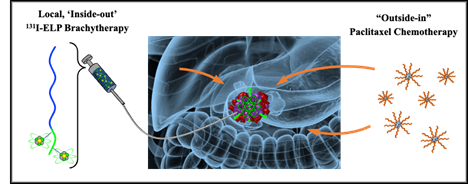
본 연구에서 평가된 전임상 치료 요법. 방사성 생체고분자(131I-ELP, 여기서 ELP는 엘라스틴 유사 폴리펩티드를 나타냄)를 췌장 종양에 주입하고 방사선 민감성 화학요법 약물인 파클리탁셀을 전신으로 전달합니다. 출처: 칠코티 연구소.
췌장암은 때때로 방사선과 방사선을 더욱 효과적으로 만드는 특정 화학요법제를 병용하여 치료합니다. 이러한 '방사선감작' 약물은 특히 DNA가 노출될 때 세포의 복제 과정을 연장함으로써 작용한다고 Schaal은 설명했습니다. 노출된 DNA는 방사선에 더 민감하고 방사선에 의해 회복 불가능하게 손상될 가능성이 더 높아 궁극적으로 세포 사멸을 초래합니다.
연구 저자들은 파클리탁셀로 알려진 방사선 민감성 화학요법제와 함께 췌장암의 다양한 측면(예: 일반적인 돌연변이, 종양 특성, 종양 밀도 또는 치료 저항성)을 반영하도록 신중하게 선택된 여러 가지 췌장암 모델에서 방사성 생체고분자를 평가했습니다. 테스트한 모든 모델 중에서 거의 모든 마우스가 반응했는데, 이는 종양이 줄어들거나 완전히 사라졌음을 의미합니다. Schaal은 "우리 모델에서 본 응답률은 전례가 없는 수준이었습니다."라고 말했습니다. "문헌을 철저히 검토한 후에도 우리는 유전적으로 다양한 췌장암 모델에서 강력한 반응을 보이는 또 다른 치료법을 아직 찾지 못했습니다." 또한 일부 쥐에서는 연구 기간 동안 종양이 재발하지 않았습니다.
연구 저자들이 현재의 임상 치료법인 파클리탁셀과 외부 빔 방사선을 평가했을 때 반응률은 그다지 인상적이지 않았습니다. 종양이 줄어들거나 사라지는 대신 종양 성장 속도만 억제되었습니다. Schaal은 “짧은 순간에 제공되는 외부 빔 방사선과 달리 우리의 근접 치료 접근 방식은 방사선을 지속적으로 전달합니다.”라고 설명했습니다. "우리는 이 지속적인 베타 입자 방사선이 종양의 미세 환경을 변경하고 파클리탁셀이 종양 핵심으로 더 잘 침투할 수 있게 하여 시너지적인 치료 효과를 가능하게 한다는 것을 발견했습니다."
중요한 것은 연구자들이 연구 과정에서 쥐의 중요한 기관에 무시할 만큼의 양의 방사능이 축적되는 등 어떠한 급성 독성 문제도 관찰하지 못했다는 것입니다. 그들은 가지고 있다 이전에보고 방사성 생체고분자는 I-95의 반감기(약 131일)보다 겔의 반감기(약 XNUMX일)가 훨씬 길기 때문에 안전하게 생분해됩니다.
저자는 전이성 질환에 대한 치료법을 평가하지 않았지만, 접근 방식의 특성상 다른 기관의 종양 덩어리와 같은 여러 위치에 생체고분자 주사를 허용할 것입니다. 이 연구가 전임상 단계에 있는 동안, 연구 저자들은 이 치료법을 발전시키기 위해 노력하고 있습니다. "우리 그룹은 더 큰 동물 모델에서 내시경 유도 전달을 위한 시스템을 개발하고 최적화하기 위해 임상 연구자들과 협력해 왔습니다."라고 듀크 대학교 생의학 공학과 교수이자 수석 저자인 Ashutosh Chilkoti 박사가 말했습니다. "그러나 이 치료법이나 새로운 치료법을 환자에게 적용할 때 어려운 점은 임상 시험을 통해 이를 뒷받침할 지원을 찾는 것입니다."
이 연구는 NIBIB(R01EB000188)의 보조금과 국립 암 연구소(NCI, 보조금 R35CA197616)의 보조금에 의해 지원되었습니다.
(다) NIH