Radiotherapie is een van de meest voorkomende kankerbehandelingen, waardoor de overlevingstijden effectief worden verlengd en de genezingspercentages voor kankerpatiënten toenemen. Door radiotherapie veroorzaakte botschade – waaronder verminderde botmassa, verhoogde botfragiliteit en een hoger risico op fracturen en osteonecrose – blijft echter een veel voorkomend probleem waarvoor momenteel geen effectieve tegenmaatregelen bestaan.
Straling veroorzaakt deze schade door de groei, overleving en rijping van botvormende cellen, osteoblasten genoemd, te onderdrukken, waardoor de botvorming wordt geremd. Eén mogelijke remedie zou blootstelling aan niet-invasieve elektromagnetische velden (EMF's) kunnen zijn, waarvan bekend is dat ze de groei en differentiatie van osteoblasten stimuleren, en de effecten van bestraling zouden kunnen verzachten. Nu heeft een onderzoeksteam in China de optimale EMF-golfvorm geïdentificeerd om de werkzaamheid van een dergelijke behandeling te maximaliseren, en rapporteert de bevindingen in Wetenschap Advances.
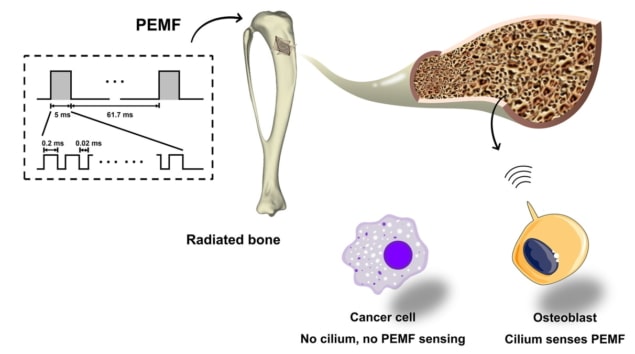
Da Jing, van Vierde Militaire Medische Universiteit, en collega's onderwierpen eerst botcellen aan EMF-stimulatie met behulp van verschillende golfvormen, waaronder sinusoïdale EMF, enkelgepulseerde EMF en gepulseerde burst-EMF (PEMF). Om de reactie van de cellen te beoordelen, volgden ze real-time intracellulaire calciumionen (Ca2+) signalering, een van de eerste cellulaire reacties op externe stimuli.
Het team ontdekte dat PEMF robuustere intracellulaire Ca induceerde2+ signalering in bestraalde osteoblasten dan de andere golfvormen, gekenmerkt door unieke Ca2+ oscillaties met meerdere Ca2+ stekels. Verdere analyses toonden aan dat een voorheen ongeïdentificeerde PEMF-golfvorm met een magnetische veldintensiteit van 2 mT en een frequentie van 15 Hz de sterkste respons in osteoblasten opwekte. Daarentegen had deze PEMF-golfvorm geen effect op andere typen bestraalde botcellen (osteoclasten en osteocyten).
Vervolgens onderzochten de onderzoekers of PEMF, toegediend met behulp van deze optimale parameters, door straling geïnduceerd botverlies kon verminderen in vivo. In onderzoeken met ratten stelden ze één achterbeen bloot aan twee doses van 8 Gy focale straling (met een tussenpoos van één dag) en gebruikten ze micro-CT om 45 dagen later de botstructuur te beoordelen. De bestraalde ledematen vertoonden aanzienlijk trabeculair botverlies, waaronder een afname van ongeveer 50% in de botvolumefractie en de botmineraaldichtheid vergeleken met de niet-bestraalde zijde.
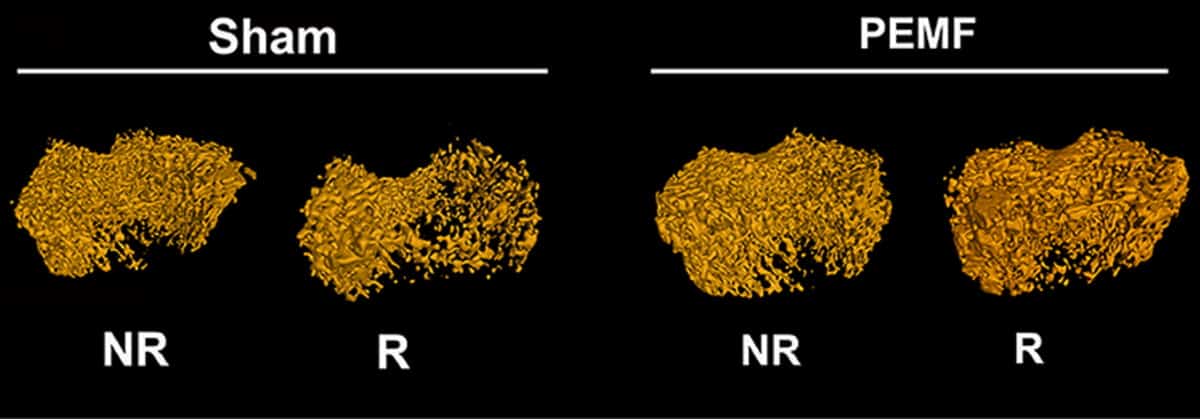
Een tweede groep ratten ontving gedurende de 2 dagen na de bestraling dagelijks PEMF voor het hele lichaam (45 uur/dag). Deze behandeling herstelde de botmassa en mechanische eigenschappen van bestraalde achterpoten tot het niveau van niet-bestraalde ledematen, door osteoblasten te redden. Het team merkt op dat PEMF geen effect had op het lichaamsgewicht of de voedselinname van de dieren.
Nu is aangetoond dat blootstelling aan PEMF door straling geïnduceerd botverlies kan verminderen, is het ook essentieel dat het PEMF geen nadelige invloed heeft op de tumorbehandeling. Met dit in gedachten vergeleken de onderzoekers de gevoeligheid van osteoblasten en verschillende tumorcellen (borstkanker, darmkanker, kwaadaardig melanoom en osteosarcoomcellen) voor PEMF.
Bestraling verminderde de levensvatbaarheid van de cellen en bevorderde apoptose in alle celtypen. Cruciaal is dat PEMF, hoewel het de levensvatbaarheid van osteoblasten verbeterde en apoptose van osteoblasten remde, op geen enkel tijdstip effect had op de levensvatbaarheid of apoptose in een van de tumorcellen.
Levende bio-inkt kan botreparatie en -regeneratie verbeteren
De onderzoekers schrijven deze selectiviteit toe aan de aanwezigheid van primaire cilia – sensorische organellen die extracellulaire mechanische signalen detecteren en vertalen – die fungeren als PEMF-sensoren. Deze primaire cilia zijn zeer overvloedig aanwezig in osteoblasten, maar ontbreken in de meeste tumorcellen. In een experiment waarbij de vorming van primaire cilia in bestraalde osteoblasten werd geblokkeerd, verdween de door PEMF gemedieerde toename in overleving en differentiatie van osteoblasten vrijwel volledig.
“Gezien het feit dat osteoblasten van alle botceltypen bijzonder gevoelig zijn voor straling, lijkt dit PEMF-regime, dat de specifieke activering van osteoblasten induceert, een veelbelovende en zeer efficiënte aanpak tegen door straling geïnduceerde botschade”, concluderen de onderzoekers.