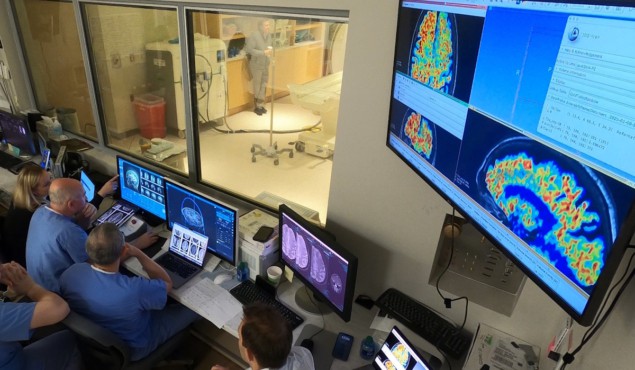
Niet-invasieve laagfrequente gerichte echografie (FUS), toegediend in combinatie met intraveneus toegediende microbellen, kan de bloed-hersenbarrière (BBB) tijdelijk openen en ervoor zorgen dat medicijnen die de ziekte van Alzheimer bestrijden de hersenen kunnen binnendringen en hun therapeutische doelen kunnen bereiken. De combinatie van een amyloïde-bèta-plaqueverminderend medicijn gevolgd door FUS blijkt veilig en effectiever te zijn in het verminderen van plaque-afzettingen in de hersenen dan alleen medicamenteuze behandeling. Hoewel de ziekte van Alzheimer niet kan worden genezen, kan het verminderen van tandplak de cognitieve impact van de ziekte verminderen en de progressie ervan vertragen.
Eerste bevindingen van een kleine, eerste klinische proef bij mensen, uitgevoerd in WVU Rockefeller Neuroscience Instituut en gerapporteerd in de New England Journal of Medicine (NEJM), stimuleert de hoop dat deze gecombineerde behandeling ooit de standaardzorg zal worden. In werkelijkheid, 60 Minuten, een populair CBS-televisienieuwsmagazine, zond een lange uitzending uit profiel van het baanbrekende onderzoek van neurochirurg Ali Rezai eerder deze maand, met onder meer een interview met een van de drie deelnemers aan dit klinische onderzoek naar de ziekte van Alzheimer.
Rezai en collega's gebruiken een gericht echografieapparaat (de Exableer Model 4000 Type 2) om de BBB bij patiënten te verstoren, te beginnen binnen twee uur na intraveneuze infusie van aducanumab. Aducanumab en lecanemab (die ook in de proef zullen worden getest) zijn door de Amerikaanse Food and Drug Administration (FDA) goedgekeurde monoklonale antilichaamtherapieën die amyloïde-bèta-plaques kunnen verminderen. De BBB verhindert echter dat de meeste van deze antilichamen de hersenen binnendringen.
Aan de proof-of-concept klinische proef namen drie deelnemers deel met een milde vorm van de ziekte van Alzheimer. Het doel was om de veiligheid en haalbaarheid te evalueren van het combineren van aducanumab met FUS om de BBB te openen en de medicijnafgifte en amyloïdverwijdering te verbeteren.
Voor de FUS-procedure werden patiënten uitgerust met een halfronde helm met daarin 1024 onafhankelijk regelbare ultrasone bronnen. Deze bronnen zenden ultrasone golven uit die op doelen worden gericht onder realtime MRI-begeleiding. Tijdens de sonificaties wordt een suspensie van in fosfolipiden ingekapselde perfluorpropaanbellen intraveneus toegediend. Het team gebruikte verspreide signalen van deze microbellen om de juiste akoestische vermogensniveaus te bepalen die de BBB veilig kunnen openen.
Na voltooiing van de FUS-procedure gebruikten de onderzoekers T1-gewogen MRI met gadoliniumcontrastverbetering om de opening van de BBB op de beoogde locaties te bepalen, 24 en 48 uur later herhaald om te bevestigen dat de BBB gesloten was. Ze voerden ook vervolg-MRI's uit 30 dagen en een jaar na voltooiing van de gecombineerde behandeling.
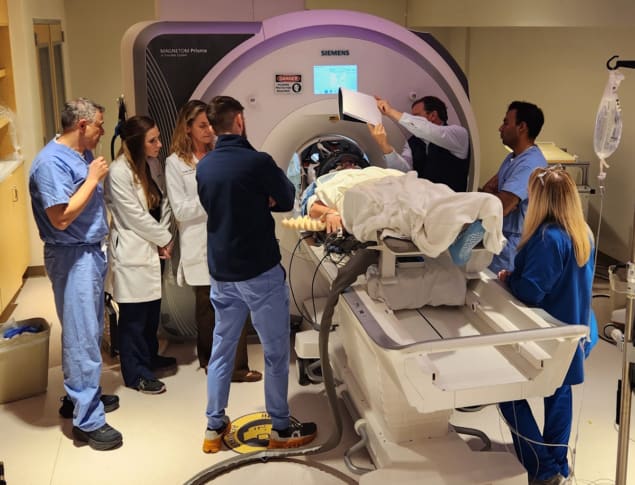
Deelnemers kregen zes maandelijkse behandelingen met intraveneus aducanumab met dosisescalatie (van 1 mg/kg lichaamsgewicht tot 6 mg/kg), gevolgd door FUS. De onderzoekers leggen uit dat ze in deze fase van de klinische proef de toepassing van FUS beperkten tot één hersenhelft, in gebieden van de frontale kwab, de temporale kwab of de hippocampus met hoge niveaus van amyloïde-bèta-plaque. Overeenkomstige hersengebieden in het contralaterale halfrond die niet waren blootgesteld aan FUS dienden als controles. Tijdens de follow-upfase kregen patiënten een maandelijkse infusie van 10 mg/kg aducanumab zonder FUS.
Om de amyloïde-bèta-niveaus te kwantificeren, voerde het team een prestatie uit 18F-florbetaben PET-scans bij baseline, na drie, elf en 11 weken tijdens de behandeling, en na 19 weken en één jaar in de follow-upfase. Rezai rapporteert dat voor alle drie de patiënten: 18F-florbetabin PET-scans toonden aan dat na 26 weken de amyloïde-bèta-plaques met gemiddeld 32% waren verminderd (gemeten via de gestandaardiseerde opnamewaardeverhouding) in hersengebieden waar de BBB was geopend, vergeleken met overeenkomstige gebieden in het onbehandelde halfrond .
De verlaging van de centiloïdwaarde, een schaal die wordt gebruikt om op PET gebaseerde metingen van de amyloïdbelasting te standaardiseren, bedroeg respectievelijk 48%, 49% en 63% voor de drie deelnemers. Rezai merkt op dat de klinische proef de penetratie van monoklonale antilichamen niet kwantificeerde, omdat deze niet voor dit doel was ontworpen.
Patiënten worden nu gerekruteerd voor de tweede fase van de klinische proef, waarbij lecanemab als monoklonale antilichaamtherapie zal worden gebruikt. “We zijn door de FDA beperkt tot de behandeling van maximaal 40 cc van de hersenen”, legt Rezai uit. “FUS zal gedurende zes maanden slechts één keer per maand worden toegediend, vergelijkbaar met de methoden voor aducanumab, met patiënt 1 BBB-opening van maximaal 10 cc; dan zullen de volgende patiënten een BBB-opening hebben van respectievelijk 20 en 40 cc.”

MR-geleide, gerichte echografie levert antilichaamtherapie rechtstreeks in de hersenen
In het 60 Minuten In een interview zei de 61-jarige patiënt Dan Miller, wiens vrouw vier jaar eerder voor het eerst gedragsveranderingen opmerkte, dat het bekijken van de laatste MRI-beelden van zijn hersenen waarop plaquereductie te zien was “onwerkelijk was”. Hij vertoont nog steeds af en toe ongewoon gedrag, maar er is geen verdere zichtbare progressie. Miller en zijn vrouw zijn hoopvol voor de toekomst.
In een begeleidend NEJM hoofdartikel, een andere pionier in het klinische gebruik van FUS, Kullervo Hynynen van het Sunnybrook Research Institute in Toronto merkt op dat “het uitbreiden van de behandeling naar klinisch significante volumes aan beide kanten van de hersenen cruciaal is voor het beoordelen van de werkzaamheid ervan bij het vertragen van de ziekteprogressie. Er zijn aanvullende onderzoeken nodig om de veiligheid en werkzaamheid op de lange termijn vast te stellen, en er moeten kosteneffectieve behandelingsapparaten worden ontwikkeld die niet afhankelijk zijn van online MRI-begeleiding.
Maar net als Miller is Hynynen optimistisch.
- Door SEO aangedreven content en PR-distributie. Word vandaag nog versterkt.
- PlatoData.Network Verticale generatieve AI. Versterk jezelf. Toegang hier.
- PlatoAiStream. Web3-intelligentie. Kennis versterkt. Toegang hier.
- PlatoESG. carbon, CleanTech, Energie, Milieu, Zonne, Afvalbeheer. Toegang hier.
- Plato Gezondheid. Intelligentie op het gebied van biotech en klinische proeven. Toegang hier.
- Bron: https://physicsworld.com/a/focused-ultrasound-plus-plaque-reducing-drugs-could-slow-alzheimers-progression/
- : heeft
- :is
- :niet
- :waar
- $UP
- 1
- 10
- 11
- 19
- 20
- 24
- 26%
- 30
- a
- de toegankelijkheid
- Extra
- toegediend
- administratie
- Na
- Alles
- alleen
- ook
- alzheimer
- Alzheimer
- an
- en
- Nog een
- Aanvraag
- passend
- ZIJN
- GEBIED
- AS
- Het beoordelen
- At
- gemiddelde
- barrière
- Baseline
- BE
- omdat
- worden
- geweest
- gedrag
- wezen
- lichaam
- zowel
- Beide kanten
- Hersenen
- bredere
- last
- maar
- by
- CAN
- verzorging
- centrum
- Wijzigingen
- Klik
- Klinisch
- CLOSED
- cognitieve
- collega's
- tegen te gaan
- combinatie van
- gecombineerde
- combineren
- vergelijkbaar
- vergeleken
- voltooiing
- Bevestigen
- contrast
- onder controle te houden
- controles
- Overeenkomend
- kostenefficient
- kon
- cruciaal
- dagen
- geleverd
- levert
- levering
- deposito's
- ontworpen
- Bepalen
- ontwikkelde
- apparaat
- systemen
- DEED
- gerichte
- direct
- Ziekte
- ontwrichten
- dosis
- drug
- Drugs
- gedurende
- Vroeger
- effectief
- werkzaamheid
- in staat stellen
- Engeland
- verhogen
- Enter
- het invoeren van
- escalatie
- oprichten
- schatten
- vertoont
- Verklaren
- Verklaart
- blootgestelde
- feit
- FDA
- haalbaarheid
- finale
- bevindingen
- Voornaam*
- gericht
- gevolgd
- volgend
- eten
- Voor
- vier
- oppompen van
- verder
- toekomst
- leiding
- HAD
- Hebben
- he
- Gezondheid
- Hoge
- zijn
- hoop
- hoopvol
- HOURS
- Echter
- HTTPS
- beeld
- afbeeldingen
- Impact
- in
- inclusief
- onafhankelijk
- informatie
- geïnfundeerd
- aftreksel
- Instituut
- Interview
- in
- intraveneus
- kwestie
- IT
- HAAR
- tijdschrift
- jpg
- later
- niveaus
- als
- Beperkt
- locaties
- langdurig
- magazine
- max-width
- Mei..
- maten
- methoden
- Molenaar
- model
- Maand
- maandelijks
- maanden
- meer
- meest
- mr
- MRI
- Dan moet je
- nodig
- Neurowetenschap leerprogramma
- nieuws
- geen
- Opmerkingen
- nu
- doel van de persoon
- occasionele
- of
- on
- eens
- EEN
- online.
- Slechts
- naar
- open
- geopend
- opening
- Optimistisch
- or
- deelnemers
- patiënt
- patiënten
- doordringen
- uitgevoerd
- fase
- Fysica
- Natuurkunde wereld
- pionier
- baanbrekende
- plan
- planning
- Plato
- Plato gegevensintelligentie
- PlatoData
- plus
- Populair
- energie
- die eerder
- procedures
- progressie
- bewijzen
- doel
- verhouding
- bereiken
- real-time
- ontvangen
- verminderen
- Gereduceerd
- vermindering
- reductie
- regio
- verwijdering
- herhaald
- gemeld
- Rapporten
- onderzoek
- onderzoekers
- respectievelijk
- begrensd
- s
- veilig
- veilig
- Veiligheid
- Zei
- Scale
- verspreid
- WETENSCHAPPEN
- Tweede
- geserveerd
- vertoonde
- getoond
- Sides
- signalen
- aanzienlijke
- ZES
- Zes maanden
- traag
- Vertragen
- Klein
- someday
- bronnen
- standaard
- Start
- Still
- stimuleren
- studies
- opschorting
- doelgerichte
- doelen
- team
- televisie
- getest
- neem contact
- dat
- De
- De toekomst
- Het Westen
- hun
- harte
- therapieën
- therapie
- Er.
- Deze
- ze
- dit
- drie
- thumbnail
- naar
- toronto
- behandelen
- behandeling
- behandelingen
- proces
- waar
- twee
- type dan:
- voor
- ondergaat
- universiteit-
- us
- Amerikaans eten
- .
- gebruikt
- gebruik
- waarde
- via
- viewing
- Virginia
- zichtbaar
- volumes
- was
- golven
- weken
- gewicht
- waren
- West
- welke
- en
- waarvan
- vrouw
- wil
- Met
- binnen
- zonder
- wereld
- jaar
- jaar
- zephyrnet