Radiotherapie van bewegende laesies is een uitdaging. De afgifte van de therapeutische straling aan een gepland doelvolume kan worden beïnvloed door orgaanbewegingen, terwijl anatomische vervormingen en onzekerheden bij de opstelling richtfouten kunnen veroorzaken. Als radiotherapeuten over een nauwkeurige, realtime 3D-verdelingskaart voor de stralingsdosis zouden beschikken, zouden ze het niveau of traject van de straling online kunnen wijzigen om effectievere en veiligere behandelingen te bereiken.
Akoestische beeldvorming met ioniserende straling (iRAI) is een niet-invasieve technologie die deze mogelijkheid zou kunnen bieden. Door de stralingsdosis te reconstrueren met behulp van akoestische golven, kan iRAI de dosisafzetting in tumoren en aangrenzende gezonde weefsels in kaart brengen en de dosisaccumulatie in realtime monitoren tijdens radiotherapie, zonder de noodzaak om extra stralingsbronnen te gebruiken.
Een multispeciaal onderzoeksteam bij de Universiteit van Michigan en Moffitt Cancer Center heeft nu een iRAI volumetrisch beeldvormingssysteem van klinische kwaliteit ontwikkeld. Het systeem, beschreven in Nature Biotechnology, bereikte 3D semikwantitatieve mapping van röntgenbundelafgifte diep in het lichaam tijdens radiotherapie van een patiënt met levermetastasen.
De iRAI-techniek werkt via het thermo-akoestische effect. Wanneer een hoogenergetische gepulseerde fotonenbundel, gegenereerd door een lineaire versneller, lichaamsweefsel raakt, wordt deze geabsorbeerd. Deze geabsorbeerde energie wordt omgezet in warmte, wat plaatselijke thermische uitzetting veroorzaakt en akoestische golven genereert. Deze golven zijn echter zwak en meestal niet waarneembaar met klinische ultrasone technologie.
Het nieuwe iRAI-systeem detecteert de akoestische signalen met een op maat ontworpen 2D-matrix-array-transducer en een bijpassend meerkanaals voorversterkerbord, aangedreven door een commercieel echografiesysteem voor onderzoek. Het versterkte signaal wordt vervolgens overgebracht naar een ultrasoonapparaat om in realtime dosisgerelateerde beelden te construeren.
De onderzoekers leggen uit dat hun systeem met twee modaliteiten, dat iRAI combineert met echografie, “een veelbelovende oplossing biedt om de behoefte aan real-time monitoring van de bundelpositie en online beoordeling van de toedieningsdosis tijdens radiotherapie op te lossen”. Het echografiebeeld presenteert de morfologische weefselstructuren en beweging in het lichaam, evenals functionele informatie zoals de bloedstroom en vasculaire dichtheid, terwijl het iRAI-beeld de ruimtelijk verdeelde dosisafzetting in verschillende biologische weefsels in kaart kan brengen en kwantificeren.
“Deze klinische proef was een pilotstudie om de haalbaarheid van het gebruik van iRAI te beoordelen bij patiënten die abdominale stereotactische lichaamsbestralingstherapie (SBRT) kregen”, legt klinisch hoofdonderzoeker uit. Kyle Cuneo van het Rogel Cancer Center in Michigan. “De bevindingen ervan stellen ons in staat het iRAI-systeem te optimaliseren.”
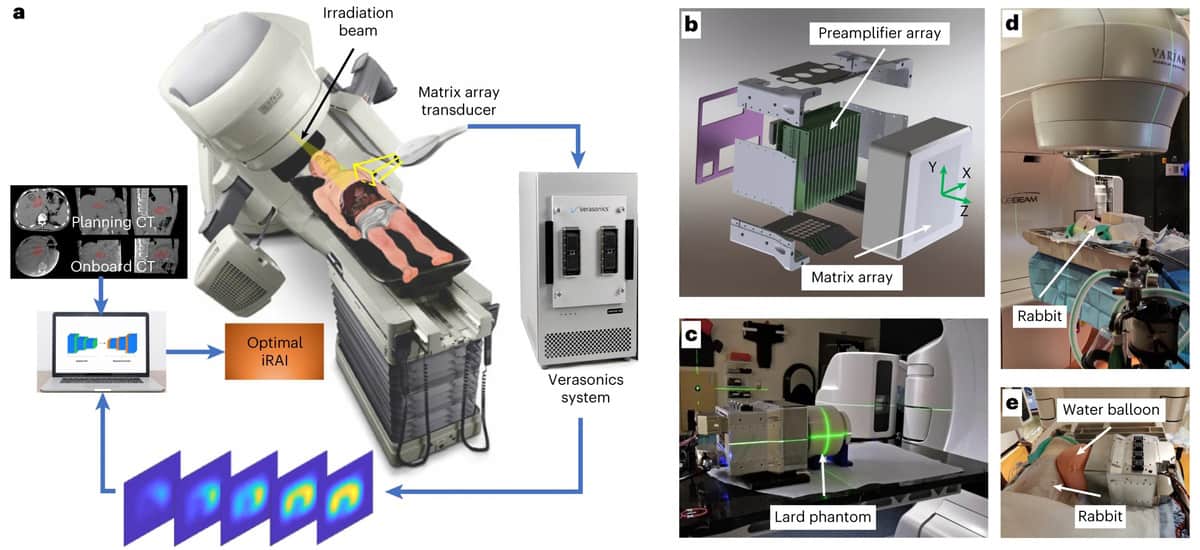
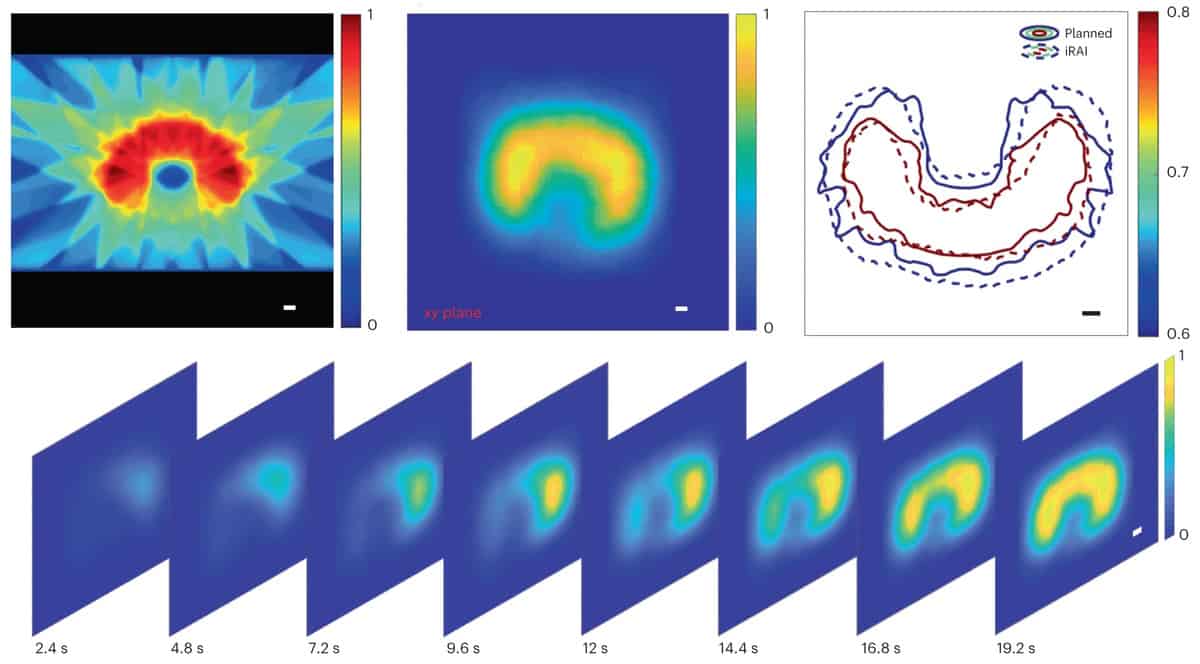
Voor hun proof-of-concept-studie valideerden de onderzoekers het systeem in een cilindrisch reuzelfantoom, een konijn en vervolgens een patiënt die abdominale SBRT onderging. Om de signaal-ruisverhouding (SNR) te verbeteren bij het detecteren van akoestische stralingssignalen, selecteerden ze een centrale frequentie van 0.35 MHz om overeen te komen met het vermogensspectrum van de akoestische signalen gegenereerd door de röntgenpuls van 4 µs. De SNR werd verder verbeterd door de 1024-kanaals voorversterker met een versterking van 46 dB, geïntegreerd in de 2D-matrixarray, en door de iRAI-beelden weer te geven met een gemiddelde van 25 keer.
Na het verifiëren van de systeemprestaties met behulp van het fantoom, creëerde en testte het team een klinisch behandelplan om de lever van een konijn te bestralen. De iRAI-metingen lieten een hoge consistentie zien tussen de gemeten dosisverdeling en die gegenereerd door het behandelplanningssysteem.
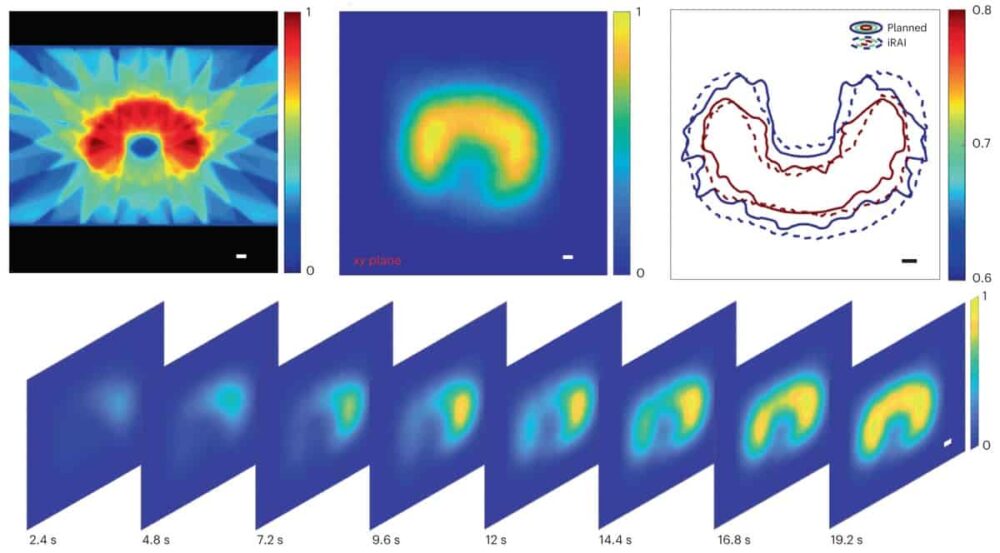
Het team stelde vervolgens radiotherapieplannen op voor de onderzoeksdeelnemer, waarbij het behandelplan voor elke fractie in twee delen werd verdeeld. Het eerste deel was bedoeld voor iRAI-beeldvorming en omvatte bundels van 2.087 en 0.877 Gy die respectievelijk in de superieure en inferieure anterieure richtingen werden afgeleverd. Dit werd gevolgd door een volumetrisch gemoduleerd boogtherapieplan (zonder iRAI-beeldvorming) om ervoor te zorgen dat de totale afgegeven stralingsdosis voldeed aan de klinische vereisten.
Zowel de dosislocaties als de algehele verdeling van iRAI-metingen kwamen goed overeen met het behandelplan. De volumetrische beeldvorming van iRAI kon het gebied met hoge dosis met hoge nauwkeurigheid in kaart brengen. De onderzoekers merken op dat ze de kaartnauwkeurigheid voor gebieden met een lagere dosisintensiteit moeten optimaliseren, de ruimtelijke resolutie moeten verbeteren en een uitgebreid kalibratieprotocol moeten ontwikkelen om absolute dosismetingen mogelijk te maken, met behulp van geavanceerde reconstructietechnieken die gebruik maken van kunstmatige intelligentie.
Grant hoofdonderzoeker Issam El Naqa van het Moffitt Cancer Center adviseert dat het huidige systeem zal worden uitgebreid met real-time echografie en ook zal worden geëvalueerd in de context van risicovolle bevallingsscenario's zoals FLASH-radiotherapie.
Akoestische beeldvorming belooft real-time dosismeting voor FLASH-radiotherapie
“Een mogelijke toepassing van deze technologie in de toekomst is real-time adaptieve behandeling. De huidige adaptieve behandeltechnieken zijn voornamelijk gebaseerd op anatomische veranderingen in de tumor en de risicoorganen (OAR's)”, legt Cuneo uit. “Met iRAI kunnen we zowel anatomische informatie als, nog belangrijker, dosimetrische informatie gebruiken om het bestralingsplan aan te passen. Dit zou dosisescalatie in het doel mogelijk kunnen maken, vooral in situaties waarin er sprake is van een aangrenzende OAR, en kunnen zorgen voor veiligere behandelingen door de werkelijke dosis die tijdens elke fractie aan het doel en de OAR wordt toegediend nauwkeurig te kwantificeren.”
"Het systeem heeft het unieke vermogen om de stralingsafzetting te visualiseren en tegelijkertijd de beweging van organen te monitoren, waardoor de straling beter op gerichte tumoren kan worden gericht, terwijl niet-betrokken weefsel op een kostenbesparende manier wordt gespaard", voegt El Naqa toe. “Dit kan op gelijke wijze worden toegepast in zowel ontwikkelde als ontwikkelingslanden waar financiële middelen schaars zijn, wat leidt tot verbeterde patiëntenzorg en betere resultaten op deze plaatsen.”
- Door SEO aangedreven content en PR-distributie. Word vandaag nog versterkt.
- Platoblockchain. Web3 Metaverse Intelligentie. Kennis versterkt. Toegang hier.
- Bron: https://physicsworld.com/a/dose-tracking-during-radiotherapy-could-enable-safer-cancer-treatments/
- 10
- 2D
- 3d
- a
- in staat
- absoluut
- versneller
- ophoping
- nauwkeurigheid
- accuraat
- nauwkeurig
- Bereiken
- bereikt
- aanpassen
- Extra
- Voegt
- vergevorderd
- Overeenkomst
- Het toestaan
- en
- Aanvraag
- toegepast
- Boog
- GEBIED
- gebieden
- reeks
- kunstmatig
- kunstmatige intelligentie
- beoordeling
- aangevuld
- middeling
- gebaseerde
- Balk
- Betere
- tussen
- bloed
- Blauw
- boord
- lichaam
- Onder
- CADXPERT / LANDXPERT
- Kanker
- verzorging
- Veroorzaken
- oorzaken
- Centreren
- centraal
- uitdagend
- Wijzigingen
- Klinisch
- combines
- commercieel
- uitgebreid
- bestaat uit
- bouwen
- verband
- Kosten
- kon
- landen
- aangemaakt
- Actueel
- deep
- geleverd
- het leveren van
- levering
- beschreven
- ontwikkelen
- ontwikkelde
- het ontwikkelen van
- Ontwikkelingslanden
- apparaat
- anders
- verdeeld
- distributie
- Uitkeringen
- Verdeeld
- gedreven
- gedurende
- elk
- effect
- effectief
- in staat stellen
- waardoor
- energie-niveau
- verbeterde
- verzekeren
- even
- fouten
- escalatie
- vooral
- geëvalueerd
- uitbreiding
- Verklaren
- Verklaart
- financieel
- Voornaam*
- flash
- stroom
- gevolgd
- fractie
- Frequentie
- oppompen van
- functioneel
- verder
- toekomst
- Krijgen
- gegenereerde
- genereert
- goed
- graad
- gezond
- Hoge
- hoog risico
- Echter
- HTTPS
- beeld
- afbeeldingen
- Imaging
- beïnvloed
- verbeteren
- verbeterd
- in
- informatie
- geïntegreerde
- Intelligentie
- kwestie
- IT
- leidend
- Niveau
- lijnen
- Lever
- locaties
- manier
- kaart
- in kaart brengen
- Match
- op elkaar afgestemd
- matching
- Matrix
- max-width
- maten
- monitor
- Grensverkeer
- meer
- beweging
- bewegend
- NATUUR
- Noodzaak
- New
- Aanbod
- online.
- open
- Optimaliseer
- totaal
- deel
- onderdelen
- patiënt
- patiënten
- prestatie
- spook
- piloot
- plaatsen
- plan
- gepland
- planning
- plannen
- Plato
- Plato gegevensintelligentie
- PlatoData
- positie
- potentieel
- energie
- bereid
- cadeautjes
- Principal
- Beloften
- veelbelovend
- protocol
- zorgen voor
- pols
- Konijn
- radiotherapie
- verhouding
- vast
- real-time
- ontvangende
- Voorwaarden
- onderzoek
- onderzoekers
- Resolutie
- Resources
- RIJ
- veiliger
- besparing
- Schaars
- scenario's
- gekozen
- Signaal
- signalen
- situaties
- oplossing
- OPLOSSEN
- bronnen
- ruimtelijke
- Spectrum
- Stakingen
- studies
- Studie
- dergelijk
- superieur
- system
- doelwit
- doelgerichte
- targeting
- team
- technieken
- Technologie
- De
- hun
- warmte-
- thumbnail
- niet de tijd of
- keer
- naar
- top
- Totaal
- Tracking
- traject
- overgedragen
- transfers
- behandeling
- proces
- waar
- onzekerheden
- unieke
- us
- .
- doorgaans
- gevalideerd
- het verifiëren
- via
- Bekijk
- volume
- golven
- welke
- en
- wil
- zonder
- Bedrijven
- zou
- röntgenstraal
- zephyrnet