Trippel-negativ brystkreft (TNBC) er en aggressiv subtype assosiert med tidlig metastatisk tilbakefall og verre pasientutfall. Svulsten uttrykker molekylære markører for den epiteliale-mesenkymale overgangen, men dens krav under spontan TNBC-metastase in vivo forblir ufullstendig forstått.
Forskere fra Johns Hopkins medisin har identifisert betydelige molekylære variasjoner mellom kreftceller som klamrer seg til en initial svulst og de som sprer seg for å danne fjerne svulster.
Andrew Ewald, Ph.D., Virginia DeAcetis-professor i grunnleggende vitenskapelig forskning og direktør, avdeling for cellebiologi ved Johns Hopkins University School of Medicine, sa: "Vi har lenge trengt nye behandlingsmål og alternativer for trippelnegative bryster kreft. Disse kreftformene kommer ofte tilbake innen tre år etter diagnose, og behandlinger som brukes for andre brystkreftformer fungerer vanligvis ikke for trippel-negative."
Forskere utførte studien på musemodeller og menneskelig vev. Denne formen for kreft er spesielt dødelig fordi den mangler molekylære signaler på overflaten som forbinder med hormonene progesteron og østrogen, samt det kreftfremmende proteinet Her2-neu. Mest brystkreft behandlinger i dag retter seg mot disse markørene, noe som gjør dem ineffektive for de med trippel-negative svulster.
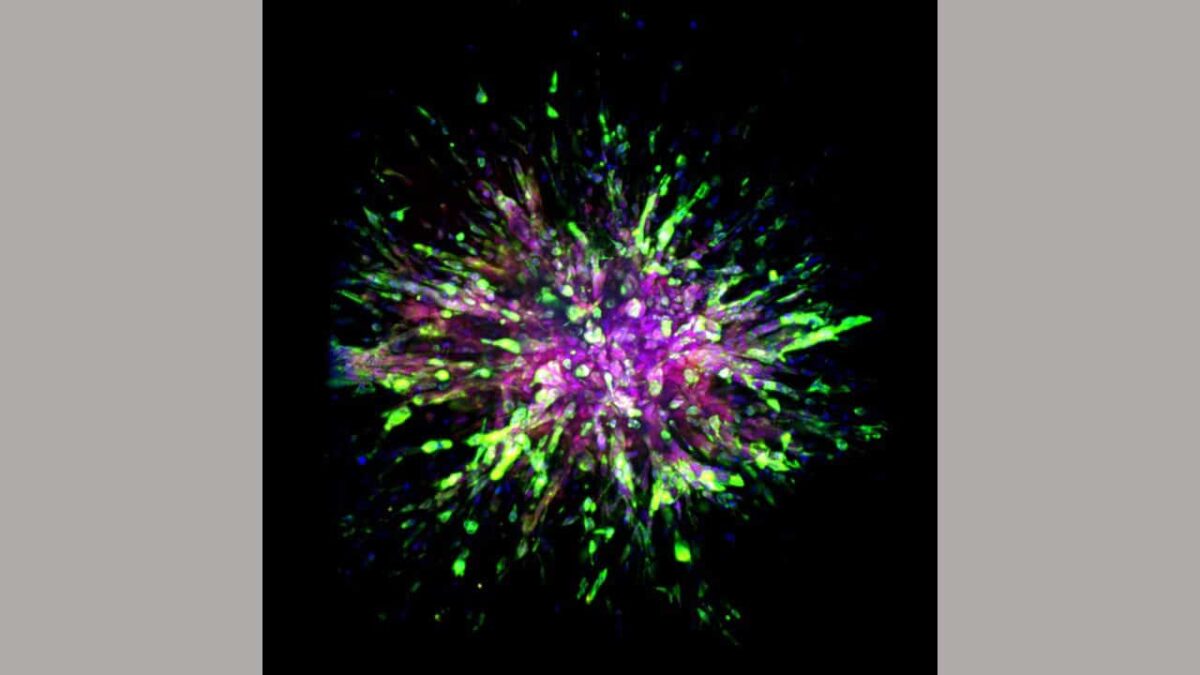
Forskere, i denne studien, observerte nøye molekylære forskjeller mellom innledende eller primære, trippel-negative brystkreftsteder og områder der den spredte seg, eller metastatiske steder, blant tre forskjellige typer celler: musemodeller, menneskelige kreftformer implantert i mus og prøver. av både primært og metastatisk vev tatt fra åtte pasienter.
Ved å bruke teknikker som f.eks maskinlæring, cellulær avbildning og biokjemisk analyse, identifiserte forskere forskjeller mellom de primære og metastatiske kreftenes genomiske uttrykksmønstre.
Ewald sa, "Den dårlige nyheten fra studien vår er at celler fra metastatiske steder er superoptimalisert for migrasjon og motstand mot behandling. Den gode nyheten er at vi identifiserte flere proteiner kalt transkripsjonsfaktorer som disse cellene krever for å håndtere utfordringene med å migrere og trives på metastatiske steder. Vi kan kanskje designe nye terapier som retter seg mot disse transkripsjonsfaktorene."
Forskere la merke til flere særegne egenskaper i cellene til mus implantert med trippel-negative brystkreftsvulster eller mus modifisert for å ha muse-versjonen av sykdommen. Det viktigste er at de fant at invasjon av trippel-negative brystkreftceller til andre vev i en annen del av kroppen, får cellene to cellulære egenskaper: bedre bevegelse og overlevelse.
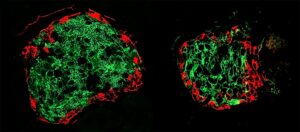
For å oppnå dette erverver brystkreftceller vimentin-celleskjelettproteinet, som forbedrer kapasiteten til såkalte mesenkymale celler til å migrere og generere nye celler. Mesenkymale celler er en type celle som vanligvis finnes i bein og beinmarg.
Produksjonen av et protein kalt cadherin gir overlevelsesfordeler til trippelnegative brystkreftceller. Proteinet finnes vanligvis i epitelceller som langs kanalene og dekkene til organer og ofte fornyer seg selv.
Forskere klassifiserer deres cellulære tilstand som såkalte hybride epiteliale-mesenkymale (EMT) celler når trippel-negative brystkreftceller får slike overlevelses- og migrerende egenskaper.
Med hjelp av Elana Fertig, Ph.D., divisjonsdirektør og assisterende direktør for kvantitative vitenskaper, og meddirektør for Convergence Institute ved Johns Hopkins Kimmel Cancer Center, observerte forskere nøye molekyler involvert i hybrid EMT-tilstander. De sporet også de molekylære mønstrene til individuelle celler i celleanalyser som modellerer invasjon ut av den primære svulsten og dannelsen av en koloni på et metastatisk sted.
Forskere brukte maskinlæringsteknikker for å identifisere mønstre i hver celles uttrykk for RNA, en slektning av DNA involvert i proteinsyntese. Flertallet av metastatiske celler, oppdaget forskerne, transformeres til hybrid EMT-tilstanden, som er mer migrerende og mer motstandsdyktig. Deretter undersøkte forskere primære svulster og vev fra de samme pasientenes metastatiske steder for å validere lignende tilstander i prøver fra åtte pasienter med trippel-negative maligniteter.
På molekylært nivå produserer de fleste metastatiske celler fem proteiner kalt transkripsjonsfaktorer (Grhl2, Foxc2, Zeb1, Zeb2 og Ovol1) som fremmer produksjonen av proteiner som er involvert i enten kreftcelleinvasjon eller kolonidannelse.
Ewald sa, "De molekylære forskjellene mellom metastatiske og primære svulster er sannsynligvis årsaken til at metastatiske tumorceller er så motstandsdyktige mot dagens behandlinger."
Forskere studerer nå måter å blokkere transkripsjonsfaktorenes gener eller deres resulterende proteiner for å stoppe metastatisk kreftvekst og om de samme molekylære og cellulære endringene skjer i andre kreftformer, for eksempel i tykktarm, binyrer, mage og tynntarm.
Tidsreferanse:
- Eloise M. Grasset, Matthew Dunworth, et al. Trippel-negativ brystkreftmetastase involverer kompleks epitel-mesenkymal overgangsdynamikk og krever vimentin. Science translasjonell medisin. GJØR JEG: 10.1126/scitranslmed.abn7571