Sluttstadium nyresykdom, når nyrene ikke lenger kan støtte kroppens behov, behandles best via nyretransplantasjon. Tilgangen på donororganer er imidlertid begrenset, og mange pasienter må stole på dialyse i stedet. Og mens en nyretransplantasjon gir utmerkede resultater, krever det at pasienten tar livslange immunsuppresjonsmedisiner, som forårsaker deres egne helsekomplikasjoner. For å løse disse problemene håper forskerne å utvikle en implanterbar biokunstig nyre for å behandle nyresvikt.
Forskere ved UC San Francisco (UCSF) jobber med å lage en slik enhet. I deres siste studie, rapportert i Nature Communications, de viser at nyreceller plassert i en implanterbar bioreaktor kan overleve inne i en gris og etterligne flere viktige nyrefunksjoner. Det er avgjørende at den implanterte enheten ikke provoserte en immunreaksjon. Forskningen er en del av Nyreprosjektet, i fellesskap ledet av UCSF Shuvo Roy og William Fissell ved Vanderbilt University Medical Center.
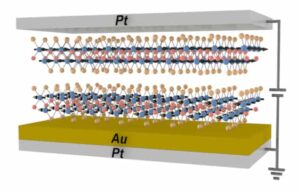
Som et første skritt mot en implanterbar biokunstig nyre, skapte Roy, Fissel og kollegene en celleholdig bioreaktor som replikerer nøkkelfunksjoner i nyretubuli, som inkluderer å levere oksygen og næringsstoffer til nyreceller samtidig som de beskyttes mot mottakerimmunceller som kan forårsake avstøting. . For å oppnå denne immunbeskyttelsen konstruerte teamet en tynn (mindre enn 1 μm) silisium nanopore-membran (SNM) fra silisiumskiver som inneholder spalteporer i nanoskala.
Forskerne bygde en prototype bioreaktor som huser en SNM med 10 nm brede porer, med humane nyreepitelceller (HRECs) dyrket på akrylinnsatser på hver side av SNM. For å teste om SNM gir en immunbeskyttende barriere vitro, eksponerte de den ene siden av SNM for det proinflammatoriske cytokinet TNF-α.
Seks timer etter eksponering var nivåene av TNF-α i avdelingen beskyttet av SNM ubetydelige, noe som viser at de 10 nm brede porene forhindrer passasje av store cytokiner (og dermed også større immunsystemkomponenter som T-celler og antistoffer) . Celler på siden direkte eksponert for TNF-α hadde mindre enn 50 % levedyktighet, mens de forseglet av SNM opprettholdt en høy levedyktighet på nesten 90 %.
Det er også viktig at et implantat ikke forårsaker blodpropp, som kan dannes på overflater i kontakt med blod og føre til enhetsfeil og alvorlige komplikasjoner for pasienten. For å unngå dette brukte forskerne beregningsvæskedynamikk for å optimalisere geometrien til den U-formede blodstrømningsbanen gjennom bioreaktoren.
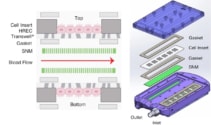
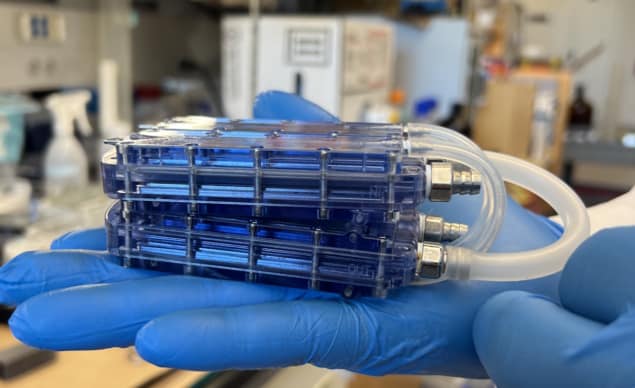
De brukte dette designet for å lage en implanterbar bioreaktor som inneholder fire SNM-er i et polykarbonathus, på linje med topp- og bunnflatene til blodkanalene. De plasserte akrylinnsatser frøet med konfluente HREC-er på motsatte sider av hver SNM, og brukte koblinger i rustfritt stål for å overføre blodet mellom SNM-ene og PTFE-vaskulære transplantater.
For å teste biokompatibiliteten til disse bioreaktorprototypene, satte teamet sammen og kirurgisk implanterte enheter i fem friske griser på dobbel antiplate-terapi (uten immunsuppresjon). Bioreaktorene koblet til dyrenes vaskulatur via PTFE-graftene. Ingen komplikasjoner relatert til enhetene eller operasjonen oppsto, og dyrene forble friske under de tre eller syv dager lange eksperimentene (tiden da hyperakutt avstøtning vanligvis vil oppstå), uten tegn til avvisning.
Forskerne evaluerte om implantering av bioreaktorer som inneholder xenogene menneskelige celler provoserte en immunreaksjon hos grisene. Undersøkelse av 13 vanlige inflammatoriske biomarkører avslørte en økning i enkelte cytokiner to dager etter implantasjon, som forventet på grunn av postoperativ betennelse. Men syv dager etter implantasjonen hadde alle cytokinnivåer sunket til en tilstand med minimal betennelse. Dette funnet er i motsetning til den kraftige responsen som forventes i en typisk xenograft-modell med en immunkompetent mottaker.
OCT kan bidra til å utvide nyredonorpoolen
Etter tre eller syv dager fjernet forskerne bioreaktorene fra dyrene for evaluering. De fant at den eksplanterte SNM var intakt, med minimal celle- og proteinfesting og ingen blodpropper dannet i enheten - et viktig skritt for å demonstrere sikkerheten. I tillegg forble de innkapslede HREC-cellene mer enn 90 % levedyktige, uten bevis for celleløsning og vedlikehold av tette intercellulære koblinger.
"Vi trengte å bevise at en funksjonell bioreaktor ikke vil kreve immunsuppressive medisiner, og det gjorde vi," sier Roy i en pressemelding. "Vi hadde ingen komplikasjoner og kan nå iterere opp og strekke oss etter hele panelet av nyrefunksjoner på menneskelig skala."
- SEO-drevet innhold og PR-distribusjon. Bli forsterket i dag.
- PlatoData.Network Vertical Generative Ai. Styrk deg selv. Tilgang her.
- PlatoAiStream. Web3 Intelligence. Kunnskap forsterket. Tilgang her.
- PlatoESG. Bil / elbiler, Karbon, CleanTech, Energi, Miljø, Solenergi, Avfallshåndtering. Tilgang her.
- PlatoHelse. Bioteknologisk og klinisk etterretning. Tilgang her.
- ChartPrime. Hev handelsspillet ditt med ChartPrime. Tilgang her.
- BlockOffsets. Modernisering av eierskap for miljøkompensasjon. Tilgang her.
- kilde: https://physicsworld.com/a/implantable-bioartificial-kidney-aims-to-free-patients-from-dialysis/
- :er
- :ikke
- $OPP
- 1
- 10
- 125
- 13
- a
- Oppnå
- tillegg
- adresse
- Etter
- mål
- justert
- Alle
- også
- an
- og
- dyr
- ER
- AS
- montert
- At
- unngå
- barriere
- BEST
- mellom
- blod
- Bunn
- bygget
- men
- by
- CAN
- Årsak
- Celler
- sentrum
- kanaler
- klikk
- kollegaer
- Felles
- fullføre
- komponenter
- består
- kryss
- tilkoblet
- kontakt
- inneholder
- kontrast
- kunne
- skape
- opprettet
- avgjørende
- Dager
- redusert
- levere
- demonstrere
- demonstrere
- utforming
- utvikle
- enhet
- Enheter
- dialyse
- gJORDE
- direkte
- direkte
- sykdom
- Doktor
- gjør
- Narkotika
- to
- under
- dynamikk
- hver enkelt
- enten
- ansatt
- innkapslet
- evaluert
- evaluering
- bevis
- undersøke
- utmerket
- Expand
- forventet
- eksperimenter
- utsatt
- Eksponering
- Failure
- finne
- fem
- flyten
- væske
- Væskedynamikk
- Til
- skjema
- dannet
- funnet
- fire
- Francisco
- Gratis
- fra
- funksjonelle
- funksjoner
- HAD
- ledet
- Helse
- sunt
- hjelpe
- Høy
- holder
- håper
- TIMER
- bolig
- Men
- HTTPS
- menneskelig
- bilde
- Immunsystem
- viktig
- in
- inkluderer
- Øke
- informasjon
- innledende
- Setter inn
- innsiden
- i stedet
- inn
- utstedelse
- saker
- IT
- DET ER
- jpg
- nøkkel
- nyre
- nyrer
- stor
- større
- siste
- føre
- venstre
- mindre
- nivåer
- Begrenset
- lenger
- vedlikehold
- mange
- max bredde
- medisinsk
- minimal
- modell
- mer
- må
- nanopore
- Natur
- nesten
- nødvendig
- behov
- Ny
- Nei.
- nå
- forekom
- of
- on
- ONE
- åpen
- motsatt
- Optimalisere
- or
- utfall
- egen
- Oksygen
- panel
- del
- passasje
- banen
- pasient
- pasienter
- Fysikk
- Fysikkens verden
- plato
- Platon Data Intelligence
- PlatonData
- trykk
- forebygge
- prosjekt
- beskyttet
- beskytte
- Protein
- prototype
- prototyper
- Bevis
- gir
- nå
- reaksjon
- i slekt
- avhengige
- forble
- fjernet
- nyre
- replikerer
- rapportert
- krever
- Krever
- forskning
- forskere
- svar
- Avslørt
- ikke sant
- roy
- Sikkerhet
- San
- San Fransisco
- sier
- Skala
- Seksjon
- seksjoner
- alvorlig
- syv
- flere
- side
- Tilbehør
- undertegne
- Silicon
- noen
- Tilstand
- Uttalelse
- Trinn
- Studer
- vellykket
- slik
- levere
- støtte
- Kirurgi
- overleve
- system
- T-celler
- Ta
- lag
- test
- testet
- enn
- Det
- De
- deres
- Dem
- Disse
- de
- denne
- De
- selv om?
- tre
- hele
- thumbnail
- Dermed
- tid
- til
- topp
- mot
- overgang
- transplantasjon
- behandle
- behandling
- behandling
- sant
- to
- typisk
- typisk
- universitet
- brukt
- av
- levedyktighet
- levedyktig
- var
- we
- var
- når
- om
- hvilken
- mens
- hele
- vil
- med
- uten
- arbeid
- verden
- ville
- zephyrnet