Radioterapia zmian ruchomych jest wyzwaniem. Na dostarczanie promieniowania terapeutycznego do zaplanowanej objętości docelowej może mieć wpływ ruch narządu, podczas gdy deformacje anatomiczne i niepewność ustawienia mogą powodować błędy celowania. Gdyby radioterapeuci dysponowali dokładną trójwymiarową mapą rozkładu dawek promieniowania w czasie rzeczywistym, byliby w stanie zmieniać poziom lub trajektorię promieniowania online, aby uzyskać bardziej skuteczne i bezpieczniejsze leczenie.
Obrazowanie akustyczne za pomocą promieniowania jonizującego (iRAI) to nieinwazyjna technologia, która może zapewnić taką możliwość. Rekonstruując dawkę promieniowania za pomocą fal akustycznych, iRAI może mapować depozycję dawki w guzach i sąsiadujących zdrowych tkankach oraz monitorować akumulację dawki w czasie rzeczywistym podczas radioterapii, bez konieczności stosowania dodatkowych źródeł promieniowania.
Wielospecjalistyczny zespół badawczy przy ul University of Michigan i Centrum Onkologiczne Moffitta opracowała system obrazowania wolumetrycznego iRAI klasy klinicznej. System opisany w Nature Biotechnology, uzyskali półilościowe mapowanie 3D dostarczania wiązki promieniowania rentgenowskiego w głąb ciała podczas radioterapii pacjenta z przerzutami do wątroby.
Technika iRAI działa poprzez efekt termoakustyczny. Kiedy impulsowa wiązka fotonów o wysokiej energii, generowana przez akcelerator liniowy, uderza w tkankę ciała, zostaje wchłonięta. Ta pochłonięta energia zamienia się w ciepło, które powoduje lokalną rozszerzalność cieplną i generuje fale akustyczne. Fale te są jednak słabe i zwykle niewykrywalne za pomocą ultrasonografii klinicznej.
Nowy system iRAI wykrywa sygnały akustyczne za pomocą specjalnie zaprojektowanego przetwornika matrycowego 2D i dopasowanej wielokanałowej płyty przedwzmacniacza, sterowanej przez komercyjny badawczy system ultradźwiękowy. Wzmocniony sygnał jest następnie przesyłany do urządzenia ultradźwiękowego w celu konstruowania obrazów zależnych od dawki w czasie rzeczywistym.
Naukowcy wyjaśniają, że ich dwumodalny system, który łączy iRAI z obrazowaniem ultrasonograficznym, oferuje „obiecujące rozwiązanie pozwalające rozwiązać potrzebę monitorowania położenia wiązki w czasie rzeczywistym i oceny online dostarczania dawki podczas radioterapii”. Obraz ultrasonograficzny przedstawia morfologiczne struktury tkanek i ruch w ciele, a także informacje funkcjonalne, takie jak przepływ krwi i gęstość naczyń, podczas gdy obraz iRAI może mapować i określać ilościowo przestrzennie rozłożoną depozycję dawki w różnych tkankach biologicznych.
„To badanie kliniczne było badaniem pilotażowym mającym na celu ocenę wykonalności zastosowania iRAI u pacjentów poddawanych stereotaktycznej radioterapii ciała (SBRT) jamy brzusznej” — wyjaśnia główny badacz kliniczny Kyle'a Cuneo z Rogel Cancer Center w Michigan. „Jego ustalenia umożliwiają nam optymalizację systemu iRAI”.
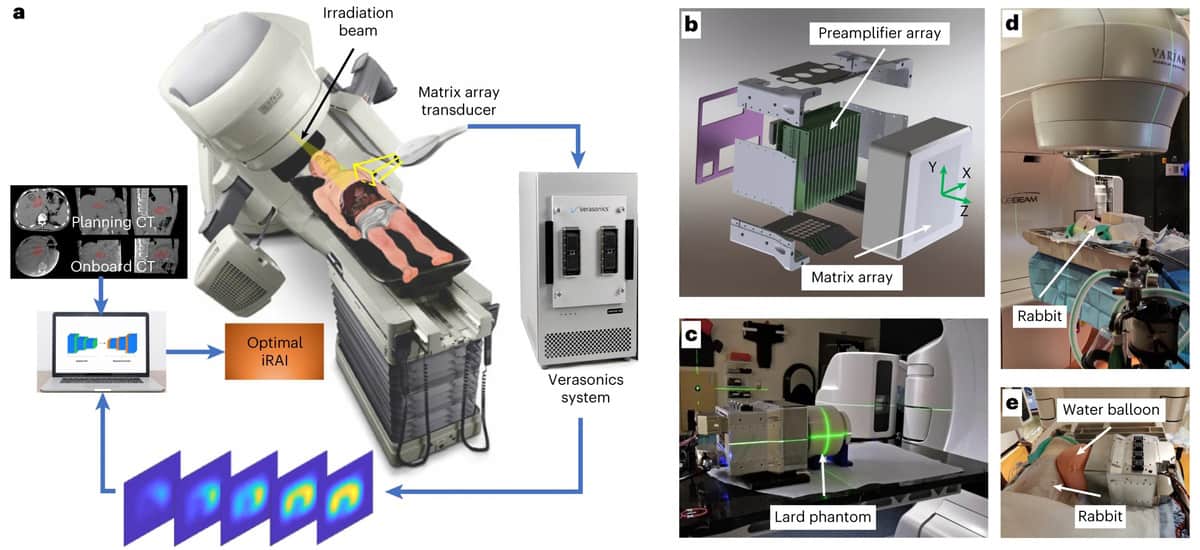
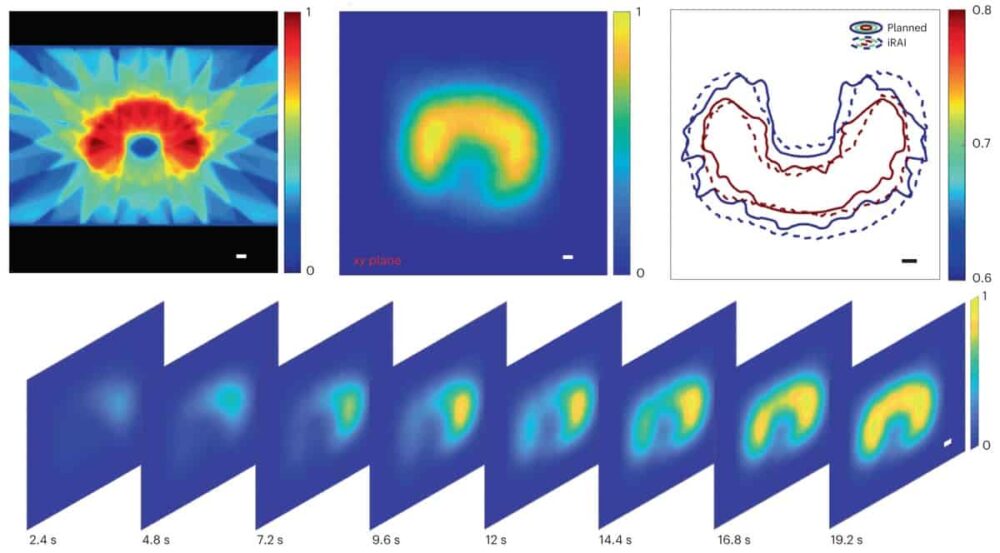
W ramach badania sprawdzającego słuszność koncepcji naukowcy zweryfikowali system w cylindrycznym fantomie ze smalcu, króliku, a następnie u pacjenta poddawanego SBRT jamy brzusznej. Aby poprawić stosunek sygnału do szumu (SNR) podczas wykrywania sygnałów akustycznych promieniowania, wybrali częstotliwość środkową 0.35 MHz, aby dopasować widmo mocy sygnałów akustycznych generowanych przez impuls rentgenowski 4 µs. SNR został dodatkowo wzmocniony przez 1024-kanałowy przedwzmacniacz o wzmocnieniu 46 dB zintegrowany z matrycą 2D matrix oraz wyświetlanie obrazów iRAI z 25-krotnym uśrednieniem.
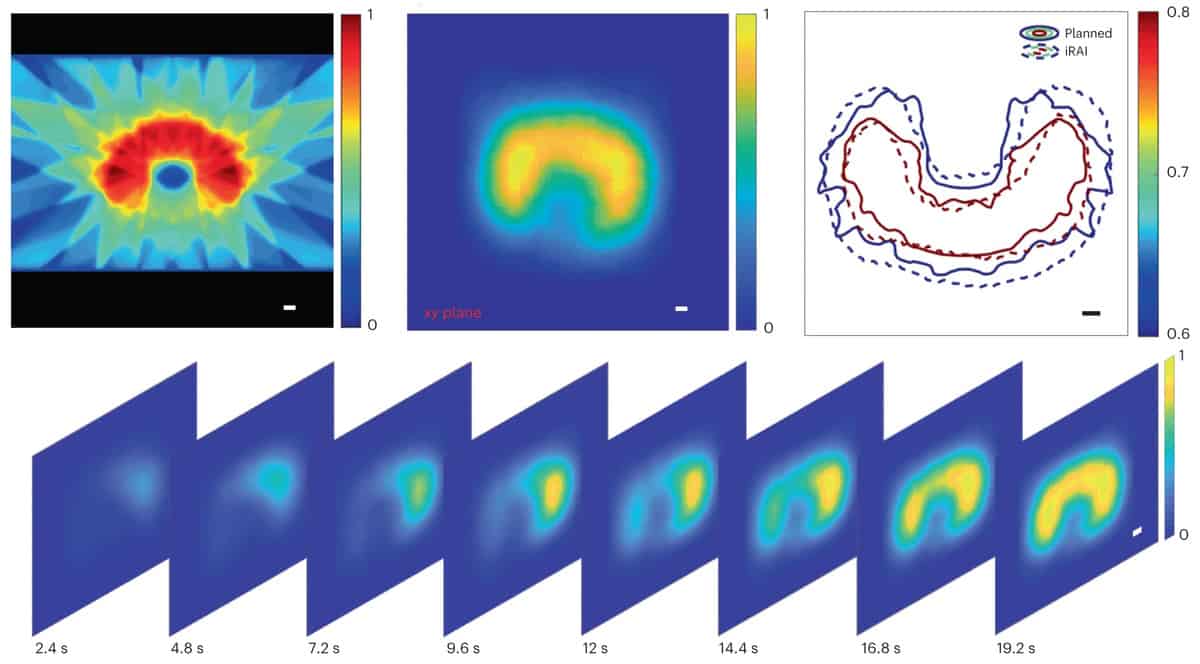
Po zweryfikowaniu działania systemu za pomocą fantomu zespół stworzył i przetestował kliniczny plan leczenia polegający na napromieniowaniu wątroby królika. Pomiary iRAI wykazały dużą spójność między zmierzonym rozkładem dawek a generowanym przez system planowania leczenia.
Następnie zespół przygotował plany radioterapii dla uczestnika badania, z planem leczenia dla każdej frakcji podzielonym na dwie części. Pierwsza część dotyczyła obrazowania iRAI i obejmowała wiązki o energii 2.087 i 0.877 Gy dostarczane odpowiednio w przednim i górnym kierunku. Następnie zastosowano plan terapii łukiem z modulacją wolumetryczną (bez obrazowania iRAI), aby upewnić się, że całkowita dostarczona dawka promieniowania spełnia wymagania kliniczne.
Zarówno umiejscowienie dawki, jak i ogólny rozkład pomiarów iRAI dobrze pasowały do planu leczenia. Obrazowanie wolumetryczne iRAI pozwoliło z dużą dokładnością odwzorować obszar o wysokiej dawce. Naukowcy zauważają, że muszą zoptymalizować dokładność mapowania dla obszarów o niższym natężeniu dawki, poprawić rozdzielczość przestrzenną i opracować kompleksowy protokół kalibracji, aby zapewnić pomiar dawki bezwzględnej, przy użyciu zaawansowanych technik rekonstrukcji wykorzystujących sztuczną inteligencję.
Główny badacz Granta Issama El Naqę z Moffitt Cancer Center informuje, że obecny system zostanie rozszerzony o obrazowanie ultrasonograficzne w czasie rzeczywistym, a także zostanie oceniony w kontekście scenariuszy porodu wysokiego ryzyka, takich jak radioterapia FLASH.
Obrazowanie akustyczne daje nadzieję na pomiar dawki w czasie rzeczywistym w radioterapii FLASH
„Jednym z potencjalnych zastosowań tej technologii w przyszłości jest adaptacyjne leczenie w czasie rzeczywistym. Obecne techniki leczenia adaptacyjnego opierają się głównie na zmianach anatomicznych w guzie i zagrożonych narządach (OAR)” — wyjaśnia Cuneo. „Dzięki iRAI możemy wykorzystać zarówno informacje anatomiczne, jak i, co ważniejsze, informacje dozymetryczne, aby dostosować plan naświetlania. Może to pozwolić na eskalację dawki w miejscu docelowym, zwłaszcza w sytuacjach, w których znajduje się sąsiedni OAR, i zapewnić bezpieczniejsze leczenie poprzez dokładne określenie ilościowe prawdziwej dawki dostarczonej do celu i OAR podczas każdej frakcji.
„System ma wyjątkową zdolność wizualizacji osadzania się promieniowania podczas monitorowania ruchu narządów, co pozwala na dokładniejsze określenie promieniowania do docelowych guzów przy jednoczesnym oszczędzaniu niezaangażowanej tkanki w sposób oszczędzający koszty” – dodaje El Naqa. „Można to w równym stopniu zastosować zarówno w krajach rozwiniętych, jak i rozwijających się, w których zasoby finansowe są ograniczone, prowadząc do poprawy opieki nad pacjentem i lepszych wyników w tych miejscach”.
- Dystrybucja treści i PR oparta na SEO. Uzyskaj wzmocnienie już dziś.
- Platoblockchain. Web3 Inteligencja Metaverse. Wzmocniona wiedza. Dostęp tutaj.
- Źródło: https://physicsworld.com/a/dose-tracking-during-radiotherapy-could-enable-safer-cancer-treatments/
- 10
- 2D
- 3d
- a
- Zdolny
- bezwzględny
- akcelerator
- akumulacja
- precyzja
- dokładny
- dokładnie
- Osiągać
- osiągnięty
- przystosować
- Dodatkowy
- Dodaje
- zaawansowany
- Umowa
- Pozwalać
- i
- Zastosowanie
- stosowany
- Łuk
- POWIERZCHNIA
- obszary
- Szyk
- sztuczny
- sztuczna inteligencja
- oszacowanie
- zwiększona
- średnio
- na podstawie
- Belka
- Ulepsz Swój
- pomiędzy
- krew
- Niebieski
- deska
- ciało
- Dolny
- CAD
- Rak
- który
- Spowodować
- Przyczyny
- Centrum
- centralny
- wyzwanie
- Zmiany
- Kliniczne
- kombajny
- handlowy
- wszechstronny
- Składa się
- skonstruować
- kontekst
- Koszty:
- mógłby
- kraje
- stworzony
- Aktualny
- głęboko
- dostarczona
- dostarczanie
- dostawa
- opisane
- rozwijać
- rozwinięty
- rozwijanie
- Kraje rozwijające się
- urządzenie
- różne
- dystrybuowane
- 分配
- Dystrybucje
- podzielony
- napędzany
- podczas
- każdy
- efekt
- Efektywne
- umożliwiać
- umożliwiając
- energia
- wzmocnione
- zapewnić
- Równie
- Błędy
- eskalacja
- szczególnie
- oceniane
- ekspansja
- Wyjaśniać
- Objaśnia
- budżetowy
- i terminów, a
- Migać
- pływ
- następnie
- frakcja
- Częstotliwość
- od
- funkcjonalny
- dalej
- przyszłość
- Wzrost
- wygenerowane
- generuje
- dobry
- stopień
- zdrowy
- Wysoki
- wysokie ryzyko
- Jednak
- HTTPS
- obraz
- zdjęcia
- Obrazowanie
- wpływ
- podnieść
- ulepszony
- in
- Informacja
- zintegrowany
- Inteligencja
- problem
- IT
- prowadzący
- poziom
- linie
- Wątroba
- lokalizacji
- sposób
- mapa
- mapowanie
- Mecz
- dopasowane
- dopasowywanie
- Matrix
- Maksymalna szerokość
- Pomiary
- monitor
- monitorowanie
- jeszcze
- ruch
- przeniesienie
- Natura
- Potrzebować
- Nowości
- Oferty
- Online
- koncepcja
- Optymalizacja
- ogólny
- część
- strony
- pacjent
- pacjenci
- jest gwarancją najlepszej jakości, które mogą dostarczyć Ci Twoje monitory,
- fantom
- pilot
- Miejsca
- krok po kroku
- planowany
- planowanie
- plany
- plato
- Analiza danych Platona
- PlatoDane
- position
- potencjał
- power
- przygotowany
- prezenty
- Główny
- obiecuje
- obiecujący
- protokół
- zapewniać
- puls
- królik
- Radioterapia
- stosunek
- real
- w czasie rzeczywistym
- odbieranie
- wymagania
- Badania naukowe
- Badacze
- Rozkład
- Zasoby
- RZĄD
- bezpieczniej
- oszczędność
- Rzadki
- scenariusze
- wybrany
- Signal
- Sygnały
- sytuacje
- rozwiązanie
- ROZWIĄZANIA
- Źródła
- Przestrzenne
- Widmo
- Strajki
- badania naukowe
- Badanie
- taki
- przełożony
- system
- cel
- ukierunkowane
- kierowania
- zespół
- Techniki
- Technologia
- Połączenia
- ich
- termiczny
- miniatur
- czas
- czasy
- do
- Top
- Kwota produktów:
- Śledzenie
- trajektoria
- przeniesione
- transfery
- leczenie
- próba
- prawdziwy
- niepewności
- wyjątkowy
- us
- posługiwać się
- zazwyczaj
- zatwierdzony
- weryfikacja
- przez
- Zobacz i wysłuchaj
- Tom
- fale
- który
- Podczas
- będzie
- bez
- działa
- by
- rentgenowski
- zefirnet