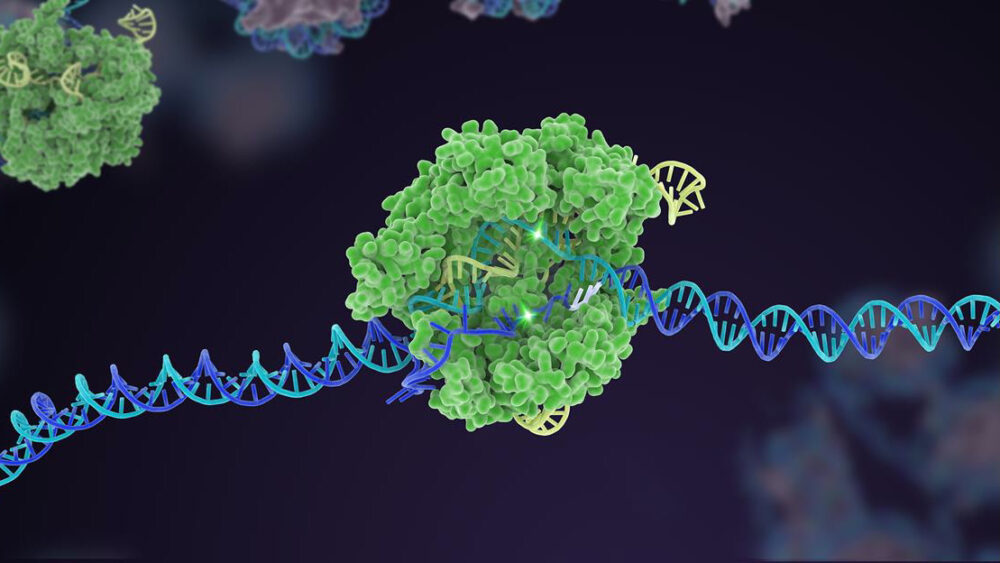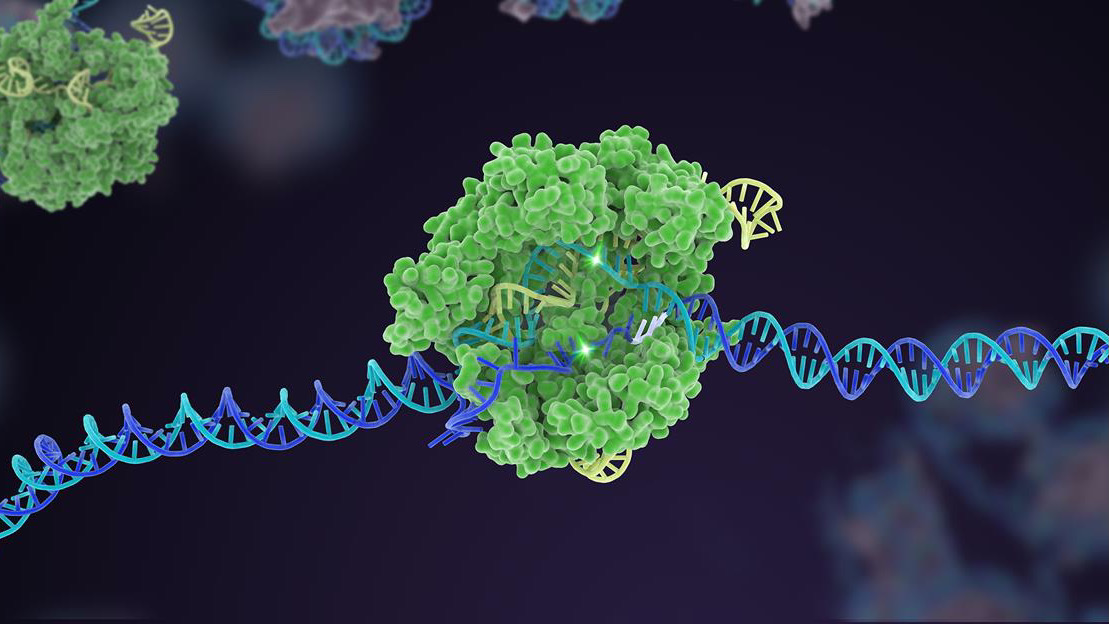
Dziesięć lat temu mało znany bakteryjny mechanizm obronny zyskał sławę jako potężny edytor genomu. W ciągu dekady CRISPR-Cas9 wyodrębnił wiele wariantów, rozszerzając się do wszechstronnego zestawu narzędzi, który może edytować kod genetyczny życia.
Daleki od pościgu za wieżą z kości słoniowej, jego praktyczne zastosowania w badaniach, opiece zdrowotnej i rolnictwie pojawiły się szybko i wściekle.
Widzieliście nagłówki. FDA zatwierdziła jego użycie w zwalczanie mutacji genetycznej leżącej u podstaw anemii sierpowatokrwinkowej. Niektórzy badacze edytowane komórki odpornościowe do walki z nieuleczalnymi nowotworami krwi u dzieci. Inni wzięli przeszczepy narządów od świni do człowieka od snu do rzeczywistości, próbując złagodzić niedobór narządów dawców. Ostatnie prace mają na celu pomóc milionom ludzi z wysokim poziomem cholesterolu - i potencjalnie udostępnić masom terapię genową opartą na CRISPR - poprzez zmniejszając ryzyko wystąpienia chorób serca z pojedynczym zastrzykiem.
Ale dla dr Jennifer Doudna, która zdobyła Nagrodę Nobla w 2020 roku za rolę w opracowaniu CRISPR, po prostu drapiemy powierzchnię jego potencjału. Wraz ze studentką Joy Wang, Doudna przedstawiła plan rozwoju technologii na następną dekadę w artykule in nauka.
Jeśli rok 2010 koncentrował się na stworzeniu zestawu narzędzi CRISPR i udowodnieniu jego skuteczności, to w tej dekadzie technologia osiąga swój pełny potencjał. Od terapii opartych na CRISPR i wielkoskalowych badań przesiewowych do diagnostyki chorób po inżynierię wysokowydajnych upraw i pożywnej żywności, technologia „i jej potencjalny wpływ są wciąż na wczesnym etapie” – napisali autorzy.
Dekada najważniejszych wydarzeń
Wylaliśmy mnóstwo atramentu na postępy CRISPR, ale opłaca się wrócić do przeszłości, aby przewidzieć przyszłość - i potencjalnie wykryć problemy po drodze.
Jednym z wczesnych osiągnięć była niesamowita zdolność CRISPR do szybkiego konstruowania zwierzęcych modeli chorób. Jego oryginalna forma z łatwością usuwa docelowy gen w bardzo wczesnym zarodku, który po przeszczepie do macicy może wygenerować genetycznie zmodyfikowane myszy w ciągu zaledwie miesiąca, w porównaniu do roku przy użyciu poprzednich metod. Dodatkowe wersje CRISPR, takie jak edycja zasad — zamiana jednej litery genetycznej na inną — oraz edycja podstawowa — która wycina DNA bez przecinania obu nici — jeszcze bardziej zwiększyły elastyczność zestawu narzędzi w inżynierii genetycznie zmienionych organoidów (myśl mini-mózgiem) i zwierzęta. CRISPR szybko stworzył dziesiątki modeli dla niektórych z naszych najbardziej wyniszczających i kłopotliwych chorób, w tym różnych nowotworów, choroby Alzheimera i dystrofii mięśniowej Duchenne'a - choroby zwyrodnieniowej, w której mięśnie powoli zanikają. Dziesiątki prób opartych na CRISPR są już dostępne w pracach.
CRISPR przyspieszył również genetyczne badania przesiewowe w erę dużych zbiorów danych. Zamiast celować w jeden gen naraz, można teraz wyciszyć lub aktywować tysiące genów równolegle, tworząc coś w rodzaju kamienia z Rosetty do tłumaczenia zaburzeń genetycznych na zmiany biologiczne. Jest to szczególnie ważne dla zrozumienia interakcji genetycznych, takich jak te w raku lub starzeniu się, do których wcześniej nie byliśmy wtajemniczeni, oraz dla zdobycia nowej amunicji do opracowywania leków.
Ale ukoronowaniem CRISPR była edycja multipleksowa. Podobnie jak jednoczesne stukanie w wiele klawiszy fortepianu, ten rodzaj inżynierii genetycznej jest ukierunkowany na wiele określonych obszarów DNA, szybko zmieniając skład genetyczny genomu za jednym zamachem.
Technologia działa na roślinach i zwierzętach. Od eonów ludzie pieczołowicie hodowali rośliny o pożądanych cechach — niezależnie od tego, czy chodzi o kolor, rozmiar, smak, odżywianie czy odporność na choroby. CRISPR może pomóc w selekcji wielu cech, a nawet udomowić nowe uprawy w ciągu zaledwie jednego pokolenia. Byki bez rogów generowane przez CRISPR, pomidory bogate w składniki odżywczei hiper-mięśniowe zwierzęta hodowlane i ryby są już rzeczywistością. Z populacją świata do 8 miliardów w 2022 roku i miliony cierpiące głód, CRISPRRed-uprawy mogą dać koło ratunkowe - to znaczy, jeśli ludzie są skłonni zaakceptować tę technologię.
Ścieżka naprzód
Dokąd zmierzamy?
Według autorów musimy dalej zwiększać skuteczność CRISPR i budować zaufanie. Oznacza to powrót do podstaw w celu zwiększenia dokładności i precyzji edycji narzędzia. Tutaj kluczowe znaczenie mają platformy do szybkiej ewolucji enzymów Cas, „nożycowego” elementu maszynerii CRISPR.
Były już sukcesy: jedna wersja Cas, na przykład, działa jako bariera dla elementu namierzającego — „ogara” sgRNA. W klasycznym CRISPR sgRNA działa samodzielnie, ale w tej zaktualizowanej wersji ma trudności z wiązaniem bez pomocy Cas. Ta sztuczka pomaga dostosować edycję do określonego miejsca DNA i zwiększa dokładność, dzięki czemu cięcie działa zgodnie z przewidywaniami.
Podobne strategie mogą również zwiększyć precyzję przy mniejszej liczbie skutków ubocznych lub wstawić nowe geny do komórek, takich jak neurony i inne, które już się nie dzielą. Chociaż jest to już możliwe przy pierwszej edycji, jej wydajność może być 30 razy niższy niż klasyczne mechanizmy CRISPR.
„Głównym celem pierwszorzędnej edycji w następnej dekadzie jest poprawa wydajności bez uszczerbku dla czystości produktu edycyjnego – wynik, który ma potencjał, aby zmienić najlepszą edycję w jedno z najbardziej wszechstronnych narzędzi do precyzyjnej edycji” – powiedzieli autorzy.
Ale być może ważniejsze jest dostarczanie, które pozostaje wąskim gardłem, zwłaszcza w przypadku leków. Obecnie CRISPR jest ogólnie stosowany na komórkach znajdujących się poza organizmem, które są podawane z powrotem – jak w przypadku CAR-T – lub w niektórych przypadkach przywiązane do nośnika wirusowego lub kapsułkowane w pęcherzykach tłuszczowych i wstrzykiwane do organizmu. Były sukcesy: w 2021, FDA zatwierdziła pierwszy strzał oparty na CRISPR do walki z genetyczną chorobą krwi, amyloidozą transtyretynową.
Jednak obie strategie są problematyczne: niewiele typów komórek może przetrwać leczenie CAR-T – umierając po ponownym wprowadzeniu do organizmu – a celowanie w określone tkanki i narządy pozostaje w większości poza zasięgiem terapii wstrzykiwanych.
Autorzy stwierdzili, że kluczowym postępem na następną dekadę jest przeniesienie ładunku CRISPR do docelowej tkanki bez szkody i uwolnienie edytora genów w zamierzonym miejscu. Każdy z tych kroków, choć pozornie prosty na papierze, przedstawia własny zestaw wyzwań, które będą wymagały zarówno bioinżynierii, jak i innowacji.
Wreszcie, CRISPR może współdziałać z innymi postępami technologicznymi, stwierdzili autorzy. Na przykład, korzystając z obrazowania komórek i uczenia maszynowego, moglibyśmy wkrótce opracować jeszcze wydajniejsze edytory genomu. Dzięki szybsze i tańsze sekwencjonowanie DNA, możemy wtedy łatwo monitorować konsekwencje edycji genów. Dane te mogą następnie zapewnić rodzaj mechanizmu sprzężenia zwrotnego, za pomocą którego można zaprojektować jeszcze potężniejsze edytory genomu w pozytywnej pętli.
Wpływ na świat rzeczywisty
Chociaż w planach jest dalsze rozszerzanie zestawu narzędzi CRISPR, technologia jest wystarczająco dojrzała, aby wpłynąć na rzeczywisty świat w drugiej dekadzie jej istnienia, stwierdzili autorzy.
W niedalekiej przyszłości powinniśmy zobaczyć „wzrost liczby terapii opartych na CRISPR przechodzących do późniejszych etapów badań klinicznych”. Patrząc dalej w przyszłość, technologia lub jej warianty mogą sprawić, że ksenoprzeszczepy narządów świni na człowieka będą rutynowe, a nie eksperymentalne. Wielkoskalowe badania przesiewowe genów, które prowadzą do starzenia się lub zwyrodnieniowych chorób mózgu lub serca – naszych dzisiejszych najlepszych zabójców – mogą przynieść profilaktyczne terapie oparte na CRISPR. Nie jest to łatwe zadanie: potrzebujemy zarówno wiedzy na temat genetyki leżącej u podstaw wieloaspektowych chorób genetycznych – to znaczy, gdy w grę wchodzi wiele genów – jak i sposobu dostarczenia narzędzi do edycji do celu. „Ale potencjalne korzyści mogą napędzać innowacje w tych obszarach znacznie wykraczające poza to, co jest obecnie możliwe” – stwierdzili autorzy.
Jednak z większą mocą wiąże się większa odpowiedzialność. CRISPR rozwija się w zawrotnym tempie, a agencje regulacyjne i opinia publiczna wciąż walczą o nadrobienie zaległości. Być może najbardziej znanym przykładem był ten z Dzieci CRISPR, gdzie przeprowadzano eksperymenty wbrew światowym wytycznym etycznym napędzany międzynarodowe konsorcjum, które wyznaczyło czerwoną linię dla edycji ludzkich komórek rozrodczych.
Podobnie organizmy modyfikowane genetycznie (GMO) pozostają kontrowersyjnym tematem. Chociaż CRISPR jest znacznie bardziej precyzyjny niż poprzednie narzędzia genetyczne, to konsumenci będą decydować, czy go powitać nowa generacja żywności wyewoluowanej przez człowieka— zarówno roślinnych, jak i zwierzęcych.
To są ważne rozmowy, które wymagają globalnego dyskursu gdy CRISPR wkracza w drugą dekadę. Ale dla autorów przyszłość rysuje się w jasnych barwach.
„Podobnie jak podczas nadejścia edycji genomu CRISPR, połączenie ciekawości naukowej i chęci przyniesienia korzyści społeczeństwu będzie napędzać następną dekadę innowacji w technologii CRISPR” – powiedzieli. „Kontynuując eksplorację świata przyrody, odkryjemy to, czego nie można sobie wyobrazić, i wykorzystamy to w prawdziwym świecie z korzyścią dla planety”.
Kredytowych Image: NIH
- Dystrybucja treści i PR oparta na SEO. Uzyskaj wzmocnienie już dziś.
- Platoblockchain. Web3 Inteligencja Metaverse. Wzmocniona wiedza. Dostęp tutaj.
- Źródło: https://singularityhub.com/2023/01/25/crisprs-wild-first-decade-only-scratches-the-surface-of-its-potential/
- 2020
- a
- zdolność
- przyśpieszony
- Akceptuj
- precyzja
- osiągnięcie
- Dzieje Apostolskie
- Dodatkowy
- awansować
- zaawansowany
- zaliczki
- nadejście
- przed
- agencje
- agenda
- Starzenie się
- rolnictwo
- przed
- Cele
- łagodzić
- sam
- już
- Chociaż
- Alzheimera
- amunicja
- i
- zwierzę
- zwierzęta
- zatwierdzony
- obszary
- Wsparcie
- Autorzy
- z powrotem
- baza
- Podstawy
- korzyści
- Korzyści
- Berkeley
- Poza
- Duży
- Big Data
- Miliard
- związania
- krew
- Bloomberg
- ciało
- podnieść
- Wzmocnione
- Mózg
- przynieść
- budować
- budować zaufanie
- Rak
- nie może
- walizka
- Etui
- zapasy
- Komórki
- wyzwania
- duża szansa,
- Zmiany
- wymiana pieniędzy
- tańsze
- klasyczny
- Kliniczne
- Badania kliniczne
- kod
- kolor
- połączenie
- jak
- w porównaniu
- składnik
- wszechstronny
- kompromis
- Konsekwencje
- konsorcjum
- Konsumenci
- kontynuując
- kontrowersyjny
- rozmowy
- mógłby
- kredyt
- CRISPR
- krytyczny
- Rośliny
- ciekawość
- Obecnie
- Ciąć
- tnący
- dane
- dekada
- Obrona
- dostarczyć
- dostawa
- rozwijanie
- oprogramowania
- odkryj
- choroba
- choroby
- DNA
- na dół
- dziesiątki
- marzenie
- napęd
- lek
- podczas
- każdy
- Wcześnie
- z łatwością
- redaktor
- skuteczność
- ruchomości
- efektywność
- wydajny
- obudowane
- inżynier
- Inżynieria
- Wchodzi
- szczególnie
- ustanowiony
- ustanowienie
- etyczny
- Parzyste
- ewoluuje
- przykład
- rozszerzenie
- odkryj
- SŁAWA
- gospodarstwo
- FAST
- FDA
- informacja zwrotna
- walka
- i terminów, a
- Elastyczność
- koncentruje
- żywność
- Nasz formularz
- od
- pełny
- dalej
- przyszłość
- zyskuje
- ogólnie
- Generować
- generacja
- inżynieria genetyczna
- Genetyka
- Globalne
- Go
- cel
- będzie
- absolwent
- większy
- wytyczne
- Nagłówki
- opieki zdrowotnej
- Serce
- pomoc
- pomaga
- tutaj
- Wysoki
- Atrakcja
- HTTPS
- człowiek
- Obrazowanie
- Rezultat
- ważny
- poprawy
- in
- Włącznie z
- Zwiększać
- wzrosła
- Zwiększenia
- niewiarygodny
- Innowacja
- Interakcje
- na świecie
- IT
- Jennifer
- tylko jeden
- Klawisz
- Klawisze
- zabójcy
- Uprzejmy
- wiedza
- na dużą skalę
- prowadzić
- nauka
- wypożyczać
- list
- życie
- Linia
- dłużej
- poszukuje
- WYGLĄD
- maszyna
- uczenie maszynowe
- maszyny
- Główny
- robić
- makijaż
- wiele
- dojrzały
- znaczy
- mechanizm
- metody
- miliony
- modele
- zmodyfikowano
- monitor
- Miesiąc
- jeszcze
- bardziej wydajny
- większość
- przeniesienie
- wieloaspektowy
- wielokrotność
- Naturalny
- Natura
- Blisko
- Potrzebować
- Neurony
- Nowości
- Następny
- NHS
- NIH
- nagroda Nobla
- notoryczny
- numer
- ONE
- oryginalny
- Inne
- Pozostałe
- zewnętrzne
- Przezwyciężać
- własny
- Papier
- Parallel
- Przeszłość
- ścieżka
- kraj
- Ludzie
- może
- planeta
- Rośliny
- Platformy
- plato
- Analiza danych Platona
- PlatoDane
- Volcano Plenty Vaporizer Storz & Bickel
- populacja
- możliwy
- potencjał
- potencjalnie
- power
- mocny
- Praktyczny
- Detaliczność
- przewidzieć
- Przewiduje
- prezenty
- poprzedni
- poprzednio
- premia
- nagroda
- problemy
- Produkt
- zapewniać
- publiczny
- położyć
- szybko
- dosięgnąć
- Osiąga
- real
- Prawdziwy świat
- Rzeczywistość
- niedawny
- Czerwony
- regulacyjne
- zwolnić
- pozostawać
- szczątki
- wymagać
- Badania naukowe
- Badacze
- sprężystość
- odpowiedzialność
- Bogaty
- mapa drogowa
- Rola
- Powiedział
- nauka
- Zwiadowca
- pokaz
- Ekrany
- druga
- zestaw
- niedobór
- powinien
- bok
- Cisza
- Prosty
- jednocześnie
- ponieważ
- pojedynczy
- witryna internetowa
- Rozmiar
- Powoli
- So
- Społeczeństwo
- kilka
- specyficzny
- prędkość
- Spot
- uprzedzony
- etapy
- Cel
- Nadal
- STONE
- strategie
- Zmagania
- Walka
- student
- taki
- cierpienie
- Powierzchnia
- przetrwać
- cel
- ukierunkowane
- kierowania
- cele
- Zadanie
- techniczny
- Technologia
- Połączenia
- Podstawy
- świat
- ich
- lecznictwo
- tysiące
- czas
- czasy
- do
- już dziś
- razem
- Toolbox
- narzędzia
- Top
- aktualny
- Wieża
- Próby
- Zaufaj
- SKRĘCAĆ
- typy
- UN
- zasadniczy
- zrozumienie
- zaktualizowane
- posługiwać się
- różnorodny
- wszechstronny
- wersja
- powitanie
- Co
- Co to jest
- czy
- który
- Podczas
- KIM
- Dziki
- będzie
- skłonny
- bez
- Wygrał
- Praca
- działa
- świat
- rok
- lat
- Wydajność
- zefirnet