Ricka Younga jest profesorem biologii na MIT, który bada RNA, które jest transkrybowane z części genomu, która nie koduje białek, znanej jako niekodujące DNA. Ta część genomu była kiedyś nazywana „śmieciowym DNA”, co daje poczucie tego, co wielu myślało o jej wartości. Naukowcy byli zaskoczeni odkryciem, że stanowi on 98% ludzkiego genomu, co zapoczątkowało poszukiwanie jego funkcji.
W tej rozmowie Rick Young rozmawia z Hanne Winarski od Bio Eats World i partnera generalnego a16z Jorge Konde, który prowadzi inwestycje na styku biologii, informatyki i inżynierii. Przed dołączeniem do a16z Conde był dyrektorem ds. strategii w Syros Pharmaceuticals i był współzałożycielem firmy zajmującej się interpretacją genomiki Knome.
Rozmowa dotyczy tego, czego dowiedzieliśmy się o 98% genomu, który uważaliśmy za śmieci. Okazuje się, że ma różne zadania, od ukrywania dowodów starożytnych infekcji wirusowych po sprawienie, by każda twarz wyglądała wyjątkowo. Dyskutują również o jego ogromnej, ale wciąż słabo poznanej roli w chorobie oraz o tym, jak badanie śmieciowego DNA doprowadziło do odkrycia przełącznika włączania/wyłączania genu, którego nikt się nie spodziewał.
Uwaga: ta rozmowa pierwotnie została opublikowana jako odcinek Bio zjada świat. Możesz posłuchać tego odcinka tutaj.
HANNE WINARSKY: Jesteśmy tutaj, aby porozmawiać o tym, co nazywa się śmieciowym DNA. Czy możemy zacząć od prostej definicji?
RICK YOUNG: To określenie sprzed około pół wieku. Naukowcy wiedzieli o częściach genomu, które nie kodują białek, i teoretyzowane że to śmieci. Wiedzieliśmy, że niektóre z nich to tylko pozostałości dawnych inwazji wirusowych genomu. Ale to zdanie, śmieciowe DNA, prześladowało nas.
HANNE: Jaki jest termin, którego próbujesz zamiast tego użyć? Ciemna materia DNA, o której coraz więcej rozumiemy każdego dnia?
RICK: Niekodujący DNA.
HANNE: Dlaczego uważali to za szczątki? Wspomniałeś, że niektóre z nich to pozostałości starych wirusów. Ale dlaczego od początku nie była to tylko tajemnica?
RICK: Ponieważ przez całą historię biologiczną toczyła się debata na temat tego, czym jest materiał genetyczny i początkowo uważano, że jest to białko. Ale kiedy stało się jasne, że białko jest maszynerią, a DNA jest planem maszynerii, ludzie zajęli się maszyną, ponieważ defekty w maszynerii powodują choroby. Ale potem okazało się, że tylko 2% genomu koduje aminokwasy dla białek. Zdecydowana większość, 98%, nie. A w 2000 roku, kiedy naukowcy z Projektu Ludzkiego Genomu przedstawione sekwencja ludzkiego genomu, te dane potwierdziły, że 98% naszych 3.2 miliarda zasad nie koduje białek.
Każdy gen ma tę niezwykłą zdolność do pobierania kawałków i kawałków segmentów białka, które będą kodować, i organizowania go tak, że produkt, który dostajesz w jednej komórce, może działać trochę szybciej, lub w innej komórce może w rzeczywistości trafić do innej komórki. komora do wykonywania innej pracy.
JORGE CONDE: Jakie były wstępne szacunki dotyczące liczby genów zakodowanych w tych 3.2 miliarda par zasad?
RICK: Ustaliliśmy około 100,000 XNUMX. Po prostu założyliśmy, że im bardziej jesteśmy skomplikowani, tym większy genom i większa liczba genów. Było trochę szoku, kiedy zdaliśmy sobie sprawę, że my i owady mamy mniej więcej taką samą liczbę genów.
JORGE: Mniej genów, niż się spodziewaliśmy, kodujących coś, co uważamy za niezwykle złożony organizm, prawda?
HANNE: To trochę szokujące.
Ten sam kod źródłowy, różne programy
JORGE: Wszyscy nauczyliśmy się w szkole średniej, że kody DNA dla RNA, kody RNA dla aminokwasów i aminokwasy dają nam białka, prawda? To centralny dogmat współczesnej biologii.
RICK: Tak. Jednym z głównych powodów, dla których ludzie szybko przypisywali tytuł „śmieciowego DNA” 98% genomu, który nie koduje białek, jest przekonanie, w dużej mierze, że biznesowym końcem genomu jest białka.
JORGE: Kiedy więc genetycy zaczęli domyślać się, że śmieciowe DNA może być czymś więcej niż śmieciowym?
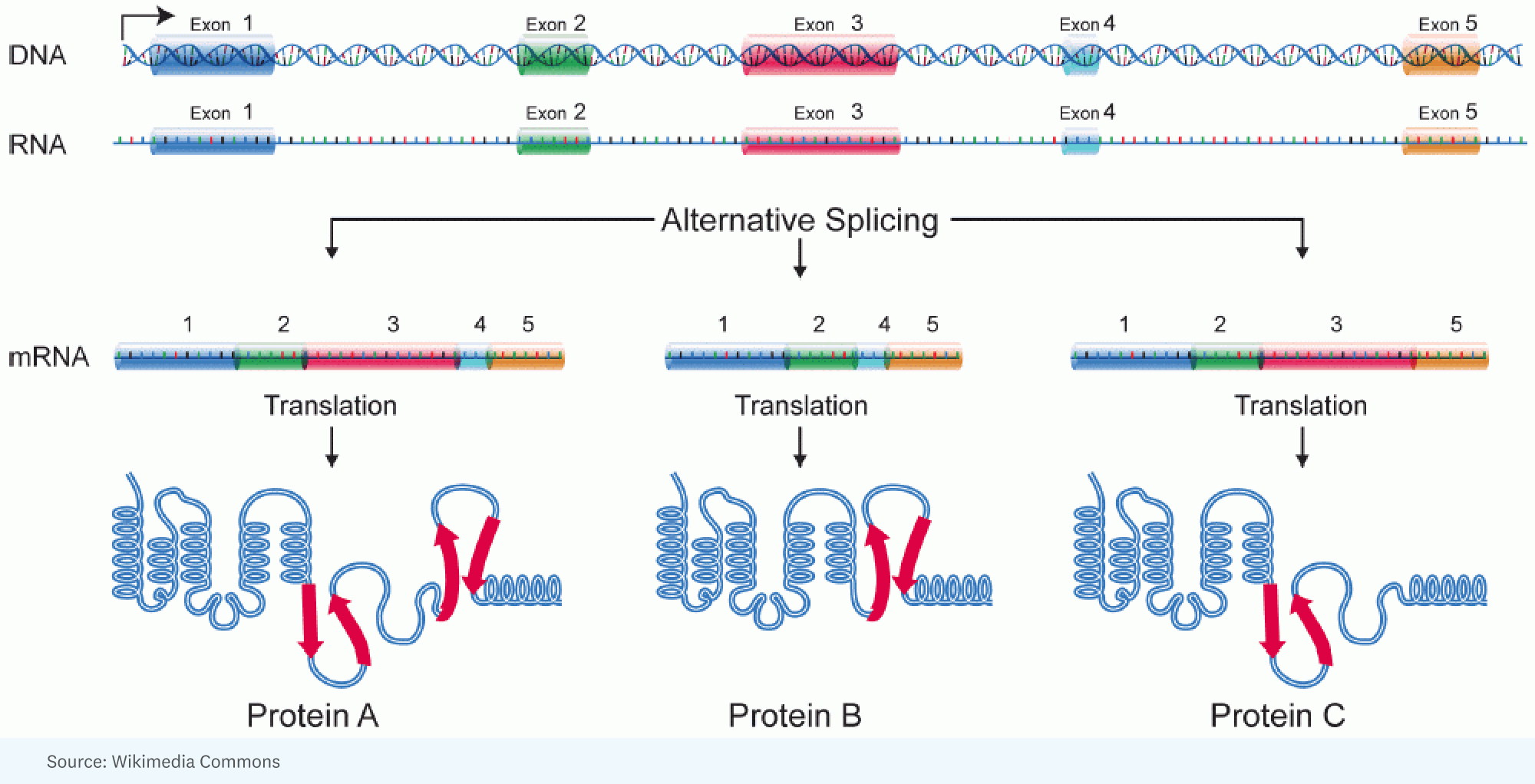
RICK: [Zaczęło się od] uświadomienia sobie, że dodatkową złożoność między istotami ludzkimi a owadami można wytłumaczyć ogromną ilością alternatywnego splicingu. To jest miejsce, w którym dla pojedynczego genu powstaje duży RNA, który jest składany inaczej w jednej komórce niż w innej. Innymi słowy, różne części genu kończą się w cząsteczce RNA, która będzie określać białko. Więc białko jest trochę inne.
HANNE: To brzmi trochę jak kalejdoskop, w którym światło pada inaczej, otrzymujesz różne kolory, różne kąty.
RICK: Cóż, to interesująca analogia. Myślę, że lepszą analogią jest to, że masz te klocki Lego i możesz stworzyć maszynę, ale możesz to zrobić na tak wiele różnych sposobów, tak wiele różnych struktur, kolorów. Każdy gen ma tę niezwykłą zdolność do pobierania kawałków i kawałków segmentów białka, które będą kodować, i organizowania go tak, że produkt, który dostajesz w jednej komórce, może działać trochę szybciej, lub w innej komórce może w rzeczywistości trafić do innej komórki. komora do wykonywania innej pracy.
JORGE: Każda komórka u danego człowieka ma w przybliżeniu taki sam genom. Jednak ten sam genom daje początek niewiarygodnie zróżnicowanej gamie różnych typów komórek. I tak, o ile zrobimy analogię, każdy typ komórki uruchamia inny program z tego samego kodu źródłowego.
RICK: Zgadza się.
Funkcje 98%
JORGE: Nie musisz być ekspertem, żeby przyjrzeć się różnym typom komórek i zobaczyć, jak bardzo mogą być, prawda? Neuron wygląda bardzo, bardzo inaczej i działa zupełnie inaczej niż, powiedzmy, komórka mięśniowa. Co determinuje program, program genetyczny, który komórka zdecyduje się uruchomić? Co sprawia, że komórka mięśniowa jest komórką mięśniową, a co sprawia, że neuron jest neuronem?
RICK: Zaczęliśmy więc od DNA, które tworzy RNA, a [RNA] tworzy białka. To jest centralny dogmat. Ale około pół wieku temu naukowcy zaczęli argumentować, że w rzeczywistości RNA zaczęło samodzielnie tworzyć różnego rodzaju funkcje. I okazuje się, że RNA faktycznie wykazuje pewną aktywność na najwcześniejszych etapach rozwoju.
Kiedy plemnik spotyka komórkę jajową, to RNA matki umieszcza w komórce jajowej. Robią to cząsteczki RNA. Okazuje się, że antybiotyki, których rutynowo używamy, wiążą się z RNA. Więc RNA ma tam kilka bardzo ważnych ról. To zmieniło sposób myślenia ludzi. Potem, kiedy zaczęliśmy myśleć o śmieciowym DNA, to ta część DNA, która nie koduje białka. A co, jeśli świat jest oparty na RNA, a nie na białkach, przynajmniej na początek? I teraz rozumiemy, że ogromna część tego, co nazywamy śmieciowym DNA, lub to, co zwykliśmy nazywać śmieciowym DNA, nie jest śmieciem. Jest bardzo funkcjonalny. A większość z nich tworzy RNA.
Więc twoim celem w programowaniu dowolnej komórki jest użycie tego konkretnego zestawu sekwencji, który dostroi każdy z tych wspólnych genów do pożądanego poziomu. . . .Naszym problemem jest to, że właściwie nie znamy programu.
HANNE: Wow. Czy możesz trochę pooglądać teren, na którym się znajdujemy, aby zrozumieć niekodującą część DNA? Wiesz, jakie jest nasze obecne rozumienie wszystkich różnych możliwości?
RICK: Tylko 2% naszego genomu koduje te sekwencje aminokwasowe, które wchodzą w skład białek. Więc co jest w księdze księgowej za to, co robi reszta?
Około połowa naszego genomu to tak zwana heterochromatyna. To tam otrzymujesz produkty starożytnych inwazji wirusowych. Starożytne retrowirusy zaatakowały, a następnie zostały przekształcone w DNA i zostały wstawione do genomu. Tak naprawdę jest to sposób, który mieliśmy przez całą naszą ewolucyjną historię, aby ukryć sekwencje, z którymi nie chcemy mieć do czynienia. I milczy w naszym genomie, z ważnym wyjątkiem.
Druga połowa to miejsce, w którym znajdują się wszystkie aktywne geny kodujące białka i gdzie znajdują się wszystkie aktywne geny niekodujące. Więc co to robi? Ma długą listę funkcji regulacyjnych, ale uprościmy ją do trzech.
Jedną z jego funkcji jest utrzymanie chromosomów. To są miejsca, w których zachodzi replikacja DNA. To miejsca w naszym genomie są odpowiedzialne za jego zwijanie, ponieważ jest to polimer o długości 2 metrów. Musi zostać złożony w jądro o średnicy kilku mikronów.
Drugim regionem regulacyjnym są wszystkie te rzeczy, które są odpowiedzialne za regulację genów. Prawdopodobnie znacznie więcej genomu określa cechy regulacyjne dla ekspresji genów niż określa same geny. A to dlatego, że każda komórka wykorzystuje inny region regulatorowy dla każdego genu.
HANNE: To takie interesujące, brzmi dla mnie trochę tak, jakby była szafa z półkami na rzeczy, które musimy na chwilę włożyć do szafy, a potem jest szafa z infrastrukturą.
Dlaczego tak ważne jest skupienie się na tym? Ponieważ to właśnie tam występuje ponad 75% wszystkich zmienności genetycznej związanej z chorobami.
RICK: Tak. Zasadniczo masz wspólny zestaw genów w każdej komórce, zarówno kodujących, jak i niekodujących. I masz elementy, masz rzeczywiste sekwencje, które działają tylko w określonych typach komórek. Więc twoim celem w programowaniu dowolnej komórki jest użycie tego konkretnego zestawu sekwencji, który dostroi każdy z tych wspólnych zestawów genów do pożądanego poziomu. Grasz więc na niesamowitym instrumencie muzycznym z 20,000 XNUMX kodującymi białka genami i mniej więcej taką samą liczbą genów niekodujących. Robisz to poprzez określone sekwencje. Naszym problemem jest to, że tak naprawdę nie znamy programu.
Wydobywanie programu regulacyjnego
HANNE: Jak więc zaczynasz to wymyślać? Jakie wskazówki stosujesz, gdy zaczynasz rozumieć ten program?
RICK: Podpowiedzi są takie, że regiony regulacyjne dla każdego genu w komórce same się ujawniają. Mówią ci. I możesz użyć różne technologiektóre bardzo szybko mówią ci w całym genomie, w konkretnym typie komórki, powiedzmy w monenerze, jakie są wszystkie regiony regulatorowe, które znajdują się w tej komórce. Możesz nawet zobaczyć, gdzie ustawiony jest reostat dla każdego z tych genów. Właśnie tam szybkie sekwencjonowanie dało nam te możliwości jednoczesnego wnioskowania o wszystkich aktywnych elementach genów, zarówno kodujących, jak i niekodujących w genomie konkretnego typu komórki.
Naszym problemem w tej chwili jest to, że musisz robić to po jednym typie komórek na raz, a mamy wiele, wiele setek typów komórek. Czasami trudno jest zobaczyć konkretną komórkę bez zanieczyszczenia innymi komórkami, ponieważ wszystkie nasze tkanki są naprawdę kombinacją wielu typów komórek.
JORGE: Czy warto argumentować przez analogię, gdybyśmy powiedzieli, że biorąc pod uwagę, że każda komórka ma cały genom, każda komórka ma cały śpiewnik, określone typy komórek decydują się grać określone symfonie, a mechanizm, który pomaga regulować genom, jest zasadniczo dyrygentem Orkiestra? Ta maszyneria jest dyrygentem, który określa, jakie piosenki zagrać, jakie nuty uderzyć, z jaką głośnością, w jakim tempie itd. Czy jest to rozsądna analogia do zrozumienia regulacyjnej funkcji genomu?
RICK: To w tym sensie, że łatwo zobaczyć, jaki będzie wynik. Ale trudniejsze jest to, kto pisze wszystkie notatki? Kim jest kompozytor, który umieścił tam te wszystkie nuty i wszystko w porządku? Kompozytor okazuje się, dla większości naszych komórek i większości naszych genów, tymi cząsteczkami białka zwanymi czynnikami transkrypcyjnymi, których zadaniem jest wiązanie się z elementami regulatorowymi genów i nadawanie im ustawienia reostatu.
Jest w tym ciekawa zmarszczka, ponieważ w miejscach, w których wiążą się te czynniki transkrypcyjne, nazywamy je wzmacniaczem. W tych miejscach wzmacniacza zawsze powstaje RNA z miejsca, w którym są one związane. Dopiero niedawno zrozumieliśmy, że RNA odgrywa ważną rolę w regulacji. Aby to wzmocnić: sposób, w jaki Twój iPhone rozpoznaje Twoją twarz, polega na tym, że wzmacniacze kontrolujące geny budowy czaszki różnią się u każdego człowieka.
Masz teraz ten triumwirat. Masz sekwencję DNA. Jest rozpoznawany specyficznie przez cząsteczkę tworzącą, czynnik transkrypcyjny, ale potrzebuje tego trzeciego kawałka, cząsteczki RNA. Zatem DNA, RNA i białko faktycznie współpracują ze sobą w tych regionach regulatorowych. I dlaczego tak ważne jest skupienie się na tym? Ponieważ to właśnie tam występuje ponad 75% wszystkich zmienności genetycznej związanej z chorobami.
HANNE: Nie żeby być muzycznie nerdowatym, ale brzmi to prawie jak akord, prawda? Trzydźwiękowa struktura grająca razem, aby stworzyć coś większego.
RICK: Zgadza się.
Programiści
JORGE: Jedną z najbardziej nowatorskich dziedzin biologii jest nasza rosnąca zdolność do prób zrozumienia niektórych praw rządzących tym, jak określane są programy komórkowe, jak określa się los komórki. Dla mnie jednym z fascynujących postępów w naszym rozumieniu była praca, którą wykonał Yamanaka, za którą został nagrodzony Nagroda Nobla, pokazując, że można przeprogramować typy komórek, po prostu wystawiając komórki na działanie bardzo małej garstki określonych czynników transkrypcyjnych.
HANNE: Czy możesz opisać, dlaczego dokładnie to był taki przełom dla branży?
RICK: Miałem niewielką rolę w tym filmie. Okazuje się, że chociaż jest to bardzo duża liczba, niewielka liczba czynników transkrypcyjnych może zidentyfikować wszystkie elementy regulacyjne, które są niezbędne dla tożsamości tej komórki. Yamanaka udowodnił nam to, pokazując, że tylko cztery z tych czynników można wykorzystać do zaprogramowania dowolnej komórki ludzkiej lub dowolnej komórki męskiej w odpowiednik embrionalnej komórki macierzystej.
Jednym ze sposobów myślenia o tym jest to, że jeśli piosenka jest zbyt zła, organizm nie żyje. Ale jeśli jest trochę nie tak, dorastasz, stajesz się dorosły, a potem z wiekiem zapadasz na te wszystkie różne choroby.
JORGE: I to jest niesamowite, prawda? Bo to by sugerowało, że system jest w jakiś sposób zaprojektowany tak, by z tego, co brzmi jak prostota, czerpie się niesamowitą złożoność. Cztery czynniki transkrypcyjne determinujące całą złożoną kaskadę zdarzeń rządzących różnymi typami komórek.
Część pracy, którą wykonałeś, wykazała, że te główne czynniki transkrypcyjne zasadniczo tworzą ekwiwalent obwodów kontrolujących geny niezbędne do ustanowienia i utrzymania stanu komórki. Czy możesz opisać, co masz na myśli przez obwody kontroli genów?
RICK: W obwodach kontroli genów są dwa fajne elementy. Po pierwsze, kiedy główny regulator znajduje te wzmacniacze i powoduje ekspresję swoich docelowych genów, to jest część obwodu, to jest wyjście. Innym elementem, który jest tak fajny, jest to, że główne czynniki transkrypcyjne również regulują swoją własną ekspresję. Więc istnieje pętla sprzężenia zwrotnego. Na przykład miałbyś schemat elektryczny, na którym mistrzowie kontrolują własną ekspresję z własnych genów, a następnie wiążą się i kontrolują ekspresję docelowego zestawu genów.
JORGE: To dość dzikie. To prawie jak cykliczne odniesienie, gdzie czynnikami transkrypcyjnymi są białka, to białko jest zrobione z DNA zakodowanego w genie. Czynniki transkrypcyjne są częścią maszynerii, która pomaga w ekspresji w transkrypcji genów. Dlatego mówisz, że czynniki transkrypcyjne – białko – pomagają regulować ekspresję genów, które tworzą czynniki transkrypcyjne.
HANNE: Tak. Jest mentalny obraz tej całej symfonii wszystkich tych małych komórek, no wiesz, śpiewających te wszystkie różne tekstury.
Genom regulacyjny i choroba
HANNE: Co się zmienia, kiedy zaczynamy rozumieć, jak to wszystko działa? Co możemy zrobić z tą wiedzą?
RICK: W tych miejscach, w których te główne czynniki transkrypcyjne decydują o tożsamości każdej komórki, większość ludzkich zmienności powoduje choroby. Ponad 75% zmienności związanej z chorobą występuje w tych elementach wzmacniających, które kierują kluczowymi genami.
JORGE: Dobra. Więc to jest dzikie, prawda? Kiedy myślimy o mutacjach powodujących lub przyczyniających się do choroby, zwykle myślimy o mutacji, która występuje w genie, która wpływa na białko, w jakiś sposób uszkadza białko, co powoduje chorobę.
HANNE: Tak.
JORGE: Ale mówisz, że w 75% przypadków ta mutacja faktycznie zachodzi poza genami, dzieje się w tym niekodującym regionie genomu. Jeśli gen jest piosenką, to nie chodzi o to, że piosenka jest niewłaściwie odtwarzana, ale że może być odtwarzana za głośno, za cicho, za wolno lub za szybko, ale to jest przyczyną wielu chorób.
RICK: Jednym ze sposobów myślenia o tym jest to, że jeśli piosenka jest zbyt zła, organizm nie żyje. Ale jeśli jest trochę nie tak, dorastasz, stajesz się dorosły, a potem z wiekiem zapadasz na te wszystkie różne choroby.
Po raz pierwszy mamy wszystkie te modele, jak skonfigurować urządzenie i sprawić, by działał.
JORGE: Nie zrobienie złej wersji genu, ale otrzymanie złej dawki genu. Za dużo lub za mało.
RICK: Zgadza się. Jak znaleźć terapie, które sobie z tym poradzą? Jak selektywnie podkręcać lub obniżać gen? W zasadzie możemy to zrobić na wiele sposobów i możemy to zrobić za pomocą terapii genowej. Możemy to zrobić dzięki edycji genów CRISPR. Ale najważniejszą rzeczą, którą, jak sądzę, odkryliśmy w ciągu ostatnich kilku lat, jest to, że każdy z tych elementów regulujących geny ma RNA. RNA jest funkcjonalne. To reostat, który pomaga dostroić wyjście tego genu. Teraz możesz na wiele sposobów RNA leków. Mamy ASO (oligonukleotydy antysensowne), takie jak Spinraza na rdzeniowy zanik mięśni. Mamy interferencję RNA. Na horyzoncie mamy kilka nowych leków drobnocząsteczkowych. Gdybyś mógł pomyśleć o sposobach programowania leku, syntetycznego RNA, do regulowania regulatorowego RNA, regulatorowego RNA, to masz główny sposób dostrojenia dowolnego genu w dowolnej komórce, gdzie ta komórka może uzyskać dostęp do tego leku.
HANNE: Więc nie chodzi tylko o zupełnie inne rozumienie tego, jak pojawia się choroba. Ale to zupełnie inne zrozumienie tego, w jaki sposób możemy potencjalnie leczyć choroby.
RICK: Dokładnie. W zasadzie mamy teraz programowalny sposób opracowywania leku, który dostraja dowolny interesujący gen. W tej chwili ludzie po prostu programują syntetyczne cząsteczki RNA, aby wyprodukować szczepionkę na tę pandemię. Taki, który jest tak dobrym wynikiem, jak można by się spodziewać po szczepionce.
JORGE: Kiedy myślimy o zastosowaniach technologia w biologii, zwykle próbujemy zrobić jedną z dwóch rzeczy. Albo próbujemy zbadać biologię bardzo głęboko i zrozumieć ją, zwiększając poziom jej złożoności, albo próbujemy interweniować. Coraz częściej jesteśmy w stanie badać biologię na bardzo, bardzo głębokim poziomie, dzięki czemu rozumiemy rządzące prawa lub zasady dzięki temu, jak regulowane są komórki. I mamy to, mamy coraz bardziej wyrafinowane narzędzia, takie jak te programowalne modalności medycyny, gdzie możemy celować w RNA, bardzo, bardzo konkretnie. Będzie to w pewnym sensie ten cnotliwy cykl między naszą zdolnością do przesłuchiwania biologii, a następnie interweniowania na coraz bardziej wyrafinowane sposoby. I myślę, że jest to jeden z najbardziej ekscytujących aspektów tego, gdzie obecnie się znajdujemy w tej dziedzinie.
RICK: Zgadzam się z tobą. Obecnie rozwijamy tak głębokie zrozumienie wielu warstw złożoności, że możemy postawić hipotezy terapeutyczne, których wcześniej nie widzieliśmy. Możemy je wykonywać z szybkością, jakiej jeszcze nie wyobrażaliśmy sobie jeszcze kilka lat temu. Ta czasowa odległość między podstawowym odkryciem a terapią, która trafiła do ludzi 10 lat temu, wynosiła średnio 14 lat. Teraz można sobie wyobrazić opracowanie hipotezy terapeutycznej opartej na podstawach naukowych i terapii, która dociera do pacjenta w ciągu dziewięciu miesięcy. Byli widząc to z tą nową szczepionką.
HANNE: Zmieniamy więc nie tylko to, jak rozumiemy pojawiające się choroby, jak je leczymy, ale także jak zajmujemy się samą nauką, a następnie jak szybko nauka może się wydarzyć i przekształcić w kliniczną rzeczywistość dla pacjentów.
RNA jako kompartmentalizator
RICK: Dokładnie. Ale teraz jest wisienka na torcie, ponieważ klasycznie myśleliśmy o farmakologii na dwa sposoby. Jednym z nich był wpływ leku na jednostkę. Drugi to wpływ jednostki na lek. A w tym ostatnim segmencie martwisz się dystrybucją leku, do jakich tkanek trafia, do jakich tkanek nie jest dostępny. Ponieważ zakładamy, że gdy lek dostanie się do komórki, dyfunduje przez komórkę i znajduje swój cel. Mamy przegródki z błoną, o których wiemy od stulecia.
JORGE: Co zawsze było kwestią przepuszczalności komórek, prawda? Czy może przejść przez błonę?
RICK: Tak. Czy może przejść przez błonę i dostać się do jądra, czy nie? Ale dopiero w ostatniej dekadzie zrozumieliśmy, że w komórkach istnieje również wiele ciał niebłonowych zwanych kondensaty biomolekularne ponieważ uważa się, że jednym z powodów, dla których te ciała się tworzą, jest to, że kondensują się podobnie jak woda kondensuje się w kroplę rosy. Ale to, co było tak głębokie w tym zrozumieniu, to to, że te kondensaty dzielą białka, DNA, RNA dla określonych funkcji. I tak teraz zrozumieliśmy, że można oddzielić od 5 do 10 miliardów cząsteczek białka i RNA w komórce na różne przedziały, w których funkcjonują razem ze swoimi kumplami.
HANNA: Hm.
JORGE: Czy opuszczamy królestwo biologii i wkraczamy w królestwo fizyki?
RICK: Zrobiliśmy dokładnie to, ponieważ uważa się, że separacja faz jest siłą napędową. To jest zjawisko fizyczne opisane przez matematykę.
HANNA: Wow.
RICK: Teraz dowiedzieliśmy się, że najskuteczniejsze leki chemioterapeutyczne to: koncentrując wewnątrz przedziałów, w których żyją ich cele. Koncentrują się 600-krotnie w porównaniu z resztą komórki, więc ich aktywność na onkogenach jest 600 razy większa niż oczekiwaliśmy. To nie tylko mówi nam, że istnieją zupełnie nowe spostrzeżenia, które są ważne w odkrywaniu i opracowywaniu leków na przyszłość, ale także sprawia, że chcemy lepiej zrozumieć, co robią te kondensaty.
Oto co mam na myśli przez wisienkę na torcie. Zdaliśmy sobie sprawę, że te przedziały kondensatu, które w tak ważny sposób działają na komórkę, są regulowane przez RNA. Ich powstawanie może być stymulowane przez RNA. Jeśli wyprodukujesz za dużo RNA, podniesiesz reostat do 11, rozpuści kondensat. Tak więc nagle zdajemy sobie sprawę, że wyjście RNA w dowolnym miejscu wewnątrz komórki może dostroić funkcję czegokolwiek poprzez wzmocnienie lub rozpuszczenie tych kondensatów, w których zachodzi ta funkcja. I to jest, jak sądzę, głębokie, ponieważ jest to kolejny sposób, w jaki programowalny RNA, syntetyczna cząsteczka RNA, może zostać wykorzystana do dostrojenia funkcji komórki, która stała się dysfunkcyjna. Po raz pierwszy mamy wszystkie te modele, jak skonfigurować urządzenie i sprawić, by działał.
HANNE: Kolejne pokrętło do wybierania.
RICK: Ale jak to wyłączyć? Okazuje się, że kiedy robisz tak długie RNA, to tylko duży łańcuch ładunków ujemnych, który rozpuszcza kondensat i wyłącza gen. W ten sposób geny są regulowane. Dostrajasz kondensat za pomocą RNA, a następnie wyłączasz go produktem RNA, który powstaje, gdy gen zostaje w pełni przepisany.
HANNE: Super fajnie. A więc wyłącznik, naprawdę.
RICK: To wyłącznik, którego nikt nie przewidział. Oznacza to, po raz kolejny, że jeśli masz programowalny lek, masz nowy sposób na celowanie w funkcje komórkowe, które są dysfunkcyjne, nowe rozwiązanie problemu terapeutycznego.
JORGE: Śmieciowe DNA jednego człowieka jest wyrafinowaną maszynerią regulującą genom innego człowieka.
HANNE: Albo każdego.
Opublikowano 15 lipca 2022
Technologia, innowacyjność i przyszłość, jak mówią ci, którzy ją budują.
- Andreessen Horowitz
- Bio i nauka
- Bitcoin
- blockchain
- zgodność z technologią blockchain
- konferencja blockchain
- coinbase
- pomysłowość
- Zgoda
- konferencja kryptograficzna
- wydobycie kryptograficzne
- kryptowaluta
- Zdecentralizowane
- DeFi
- Zasoby cyfrowe
- ethereum
- uczenie maszynowe
- niezamienny żeton
- plato
- Platon Ai
- Analiza danych Platona
- Platoblockchain
- PlatoDane
- platogaming
- Wielokąt
- dowód stawki
- W3
- zefirnet