Czerniak skóry jest najbardziej śmiertelnym ze wszystkich nowotworów skóry, zwłaszcza ze względu na tendencję do naciekania i tworzenia przerzutów w odległych miejscach. Jest to trzeci pierwotny nowotwór złośliwy po rakach płuc i piersi, który preferencyjnie kolonizuje mózg, z występowaniem przerzutów do mózgu.
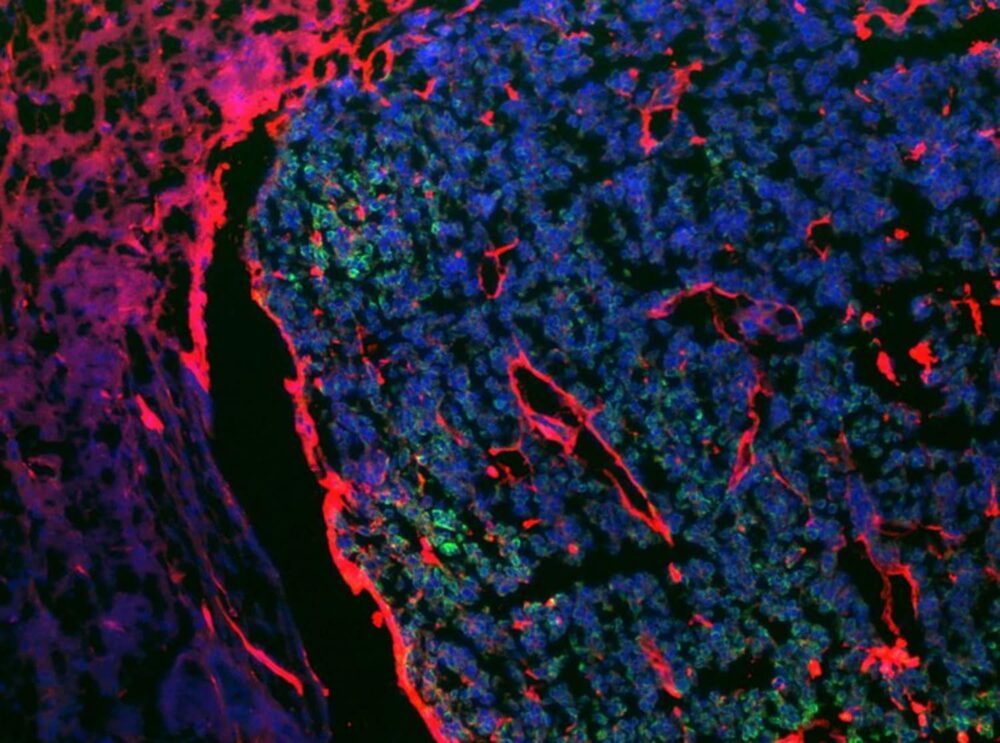
Po raz pierwszy naukowcy z Uniwersytet w Tel Awiwie odkryli mechanizm, który umożliwia przerzuty raka skóry do mózgu i zdołali opóźnić rozprzestrzenianie się choroby o 60% do 80% przy użyciu istniejących metod leczenia. Odkryli, że komórki rakowe „rekrutują” astrocyty, komórki w kształcie gwiazdy znajdujące się w rdzeniu kręgowym i mózgu, które są odpowiedzialne za utrzymanie homeostazy lub stabilnych warunków w mózg, u pacjentów z czerniakiem z przerzutami do mózgu.
Prof. Ronit Satchi-Fainaro powiedział: „W zaawansowanym stadium u 90% pacjentów z czerniakiem (rakiem skóry) rozwiną się przerzuty do mózgu. To zagadkowa statystyka. Spodziewamy się przerzutów w płucach i wątrobie, ale mózg ma być chronionym narządem. Bariera krew-mózg zapobiega przedostawaniu się szkodliwych substancji do mózgu, a tutaj podobno nie działa – komórki rakowe ze skóry krążą we krwi i docierają do mózgu. Zadaliśmy sobie pytanie „z kim” komórki rakowe rozmawiają” w mózgu, aby go infiltrować”.
Prof. Satchi-Fainaro powiedział: „Astrocyty są pierwszymi, które przychodzą, aby poprawić sytuację na przykład w przypadku udaru lub urazu i to z nimi komórki nowotworowe wchodzić w interakcje, wymieniając cząsteczki i uszkadzając je. Ponadto komórki rakowe rekrutują astrocyty, aby nie hamowały rozprzestrzeniania się przerzutów. W związku z tym tworzą miejscowy stan zapalny w obszarach interakcji komórek czerniaka z astrocytami, co zwiększa przepuszczalność przez barierę krew-mózg oraz podział i migrację komórek rakowych”.
„Komunikacja między nimi znajduje odzwierciedlenie w tym, że astrocyty zaczynają wydzielać białko promujące stan zapalny o nazwie MCP-1 (znane również jako CCL2), a w odpowiedzi na to komórki nowotworowe zaczynają wyrażać swoje receptory CCR2 i CCR4. które podejrzewaliśmy, że są odpowiedzialne za destrukcyjną komunikację z astrocytami”.
Naukowcy przetestowali swoją hipotezę, hamując ekspresję białka i jego receptorów w genetycznie zmodyfikowanych modelach laboratoryjnych i trójwymiarowych modelach czerniaka pierwotnego i przerzutów do mózgu. Wykorzystali zarówno przeciwciało (cząsteczka biologiczna), jak i małą cząsteczkę (syntetyczną) zaprojektowaną do blokowania białka MCP-3.
Wykorzystali również technologię CRISPR do genetycznej edycji komórek rakowych i wycięcia dwóch genów, które wyrażają dwa odpowiednie receptory, CCR2 i CCR4. Dzięki każdej metodzie naukowcy mogli opóźnić rozprzestrzenianie się przerzutów.
prof. Satchi-Fainaro powiedziany, „Te terapie odniosły sukces w opóźnieniu przenikania komórek rakowych do mózgu i ich późniejszego rozprzestrzeniania się w mózgu. Należy zauważyć, że przerzuty czerniaka do mózgu są bardzo agresywne, ze złym rokowaniem na 15 miesięcy po zabiegu chirurgicznym, radioterapii i chemoterapia. W zależności od etapu interwencji osiągnęliśmy opóźnienie od 60% do 80%”.
„Najlepsze wyniki osiągnęliśmy dzięki leczeniu przeprowadzonemu bezpośrednio po operacji usunięcia czerniaka pierwotnego i udało nam się zapobiec przedostawaniu się przerzutów do mózgu; dlatego uważam, że leczenie jest odpowiednie dla kliniki jako środek zapobiegawczy.”
„Zarówno przeciwciało, jak i mała cząsteczka, której używaliśmy – przeznaczone głównie do leczenia miażdżycy, cukrzycy, zwłóknienia wątroby i chorób sercowo-naczyniowych, a także służące jako biomarker dla innych rodzajów raka – zostały już przetestowane na ludziach w ramach badań klinicznych . Dlatego te zabiegi są bezpieczne i możemy spróbować zmienić je na czerniaka”.
Referencje czasopisma:
- Sabina Pozzi, Anna Scomparin i in. Hamowanie osi MCP-1/CCR2 uwrażliwia mikrośrodowisko mózgu na progresję przerzutów czerniaka do mózgu. JCI Insight, DOI: 10.1172 / jci.insight.154804