As bactérias podem parecer um estranho aliado na batalha contra o câncer.
Mas num novo estudo, bactérias geneticamente modificadas faziam parte de uma terapia de equipa para reduzir tumores. Em camundongos com câncer de sangue, mama ou cólon, as bactérias atuaram como faróis para seus parceiros – células T modificadas – enquanto os dois procuravam e destruíam células tumorais.
CAR T – o nome das terapias que utilizam essas células T destruidoras do câncer – é uma abordagem transformadora. Aprovado pela primeira vez pela Food and Drug Administration (FDA) dos EUA para um tipo de leucemia mortal em 2017, agora existem seis tratamentos disponível para vários tipos de câncer no sangue.
Apelidado de “droga viva”pelo pesquisador pioneiro Dr. Carl June, da Universidade da Pensilvânia, o CAR T está começando a assumir doenças autoimunes, lesões cardíacas e problemas de fígado. Também está preparado para eliminar “células zumbis” senescentes ligadas a doenças relacionadas à idade e combater o VIH e outras infecções virais.
Apesar da sua promessa, no entanto, o CAR T vacila quando confrontado com tumores sólidos – que constituem cerca de 90% de todos os cancros.
“Cada tipo de tumor tem suas próprias maneiras de escapar do sistema imunológico”, dito Junho anteriormente em Medicina Penn NovaS. “Portanto, não haverá uma terapia CAR T mágica que atinja todos os tipos de tumores.”
Surpreendentemente, as bactérias podem fazer com que June reconsidere – a nova abordagem tem potencial como tratamento universal para todos os tipos de tumores sólidos. Quando administrados a ratos, os insetos projetados cavaram profundamente nos núcleos dos tumores e prontamente secretaram uma “etiqueta” sintética para atrair soldados CAR T próximos. A etiqueta molecular adere apenas às regiões imediatamente adjacentes ao tumor e poupa as células saudáveis dos ataques CAR T.
As bactérias modificadas também poderiam, em teoria, infiltrar-se noutros tipos de tumores sólidos, incluindo os “sorrateiros”, difíceis de atingir com terapias convencionais. Juntos, o novo método chamado ProCAR – células T CAR guiadas por probióticos – combina bactérias e células T em uma potência no combate ao câncer.
Ele mostra “a utilidade das bactérias projetadas como um novo aprimoramento da terapia com células T CAR”, dito Eric Bressler e Dr. Wilson Wong, da Universidade de Boston, que não estiveram envolvidos no estudo.
Double Tap
Espere aí, o que é CAR T mesmo?
Em suma, as terapias CAR T utilizam células T que foram geneticamente modificadas para aumentar as suas capacidades existentes. As células T já são assassinas naturais que caçam e destroem vírus, bactérias e cânceres dentro do nosso corpo. Eles usam “garras” celulares para agarrar proteínas especiais na superfície das células-alvo – chamadas antígenos – sem danificar as células saudáveis próximas.
Mas as células cancerígenas são inimigas complicadas. Seus antígenos sofrem mutações rapidamente para evitar a vigilância e os ataques das células T. A terapia CAR T substitui essa defesa ao manipular células T para melhor procurar e destruir seus alvos.
O processo geralmente é assim. As células T são extraídas em uma coleta de sangue. Os cientistas então inserem genes nas células para formar uma nova “garra” de proteína para agarrar um antígeno específico. Essas células projetadas são infundidas de volta no corpo do paciente, onde caçam o antígeno e destroem a célula-alvo. Trabalho recente também está explorando a edição direta de células T dentro do corpo.
CAR T fez maravilhas para cânceres do sangue anteriormente intratáveis. Mas os tumores sólidos são uma história diferente.
Um grande problema é a segmentação. Muitos tipos de câncer no sangue têm um antígeno universal que sinaliza “Sou canceroso”, tornando relativamente fácil a engenharia de células T CAR para encontrá-los.
Os tumores sólidos, por outro lado, têm uma grande variedade de antígenos – muitos dos quais também estão presentes em tecidos normais – diminuindo a eficiência das células T CAR e aumentando as chances de efeitos colaterais mortais. Pior ainda, as células cancerígenas produzem proteínas semelhantes a cola que constroem um escudo protetor em torno dos cancros. Chamada de microambiente tumoral, a barreira é altamente tóxica para as células T CAR. Seus baixos níveis de oxigênio destroem prontamente as membranas das células T CAR. Como balões estourados, as células espalham seu conteúdo nas áreas circundantes, causando inflamação.
O que pode sobreviver a este deserto de tumores? Bactérias.
Um antígeno universal
O novo estudo transformou bactérias em cavalos de Tróia que podem, em teoria, infiltrar-se em qualquer tumor sólido. A bactéria escolhida, uma cepa de E. coli, já é usado para aliviar problemas gastrointestinais e metabólicos. Eles são fáceis de reprogramar geneticamente e podem liberar cargas biológicas nos núcleos dos tumores, tornando-os candidatos perfeitos para “marcar” cânceres no CAR T.
Para projetar as etiquetas, a equipe desenvolveu um antígeno proteico que pode se ancorar aos componentes do tumor e brilhar em verde fluorescente. Os tumores revestidos com este antígeno projetado os tornam fáceis de detectar e vulneráveis às células T CAR projetadas para destruí-los.
A equipe então reprogramou geneticamente as bactérias para liberar sua carga útil de antígeno assim que atingissem o microambiente do tumor.
Numa prova de conceito, o sistema tag-team reduziu o crescimento do cancro e aumentou a sobrevivência em ratos com um cancro sanguíneo agressivo. Os tratamentos com probióticos com etiqueta não funcional não ajudaram. Os ratos tratados passaram o dia alegremente e mantiveram um peso corporal saudável enquanto seus tumores diminuíam. As bactérias modificadas permaneceram perto dos tumores por pelo menos duas semanas.
Outros testes em ratos com cancro do cólon mostraram resultados igualmente positivos. Uma dose de bactérias seguida por duas doses de células T CAR reduziu o tamanho do tumor em quatro vezes 22 dias após o tratamento.
Outra perna para cima
O sistema funcionou, mas a equipe não ficou satisfeita. A quantidade de antígeno produzido depende do crescimento bacteriano, fazendo com que a eficiência da etiqueta diminua e diminua com a população bacteriana.
Para impulsionar o sistema, a equipe adicionou outro circuito genético às bactérias, permitindo-lhes liberar uma substância química que atrai as células T CAR. O método melhorado reduziu tumores em ratos com câncer de mama após duas injeções na corrente sanguínea.
“Combinar as vantagens das bactérias que direcionam tumores e das células CAR-T fornece uma nova estratégia para o reconhecimento de tumores, e isso constrói a base para comunidades projetadas de terapias vivas”, dito a autora do estudo, Rosa Vincent, na Universidade de Columbia.
A estratégia poderia ser especialmente poderosa em tumores sem antígenos óbvios. No entanto, ampliar a estratégia exigirá algum esforço. Os cânceres em humanos têm aproximadamente 0.8 polegadas de diâmetro – cerca de três quartos de um quarto.
Embora seja uma estimativa baixa para vários tipos de cancro, ainda é “20 a 40 vezes maior do que os tumores de ratos neste estudo”, disseram Bressier e Wong. Mais estudos terão de explorar quão bem o antigénio sintético se difunde em cancros cada vez maiores.
A segurança é outra preocupação. Em comparação com os ratos, os humanos são mais sensíveis a potenciais toxinas produzidas por bactérias. Baseado em ensaios clínicos anteriores com bactérias modificadas, a solução pode ser mais engenharia genética para atenuar os genes relacionados às toxinas.
“Embora ainda estejamos na fase de investigação”, os resultados “poderão abrir novos caminhos para a terapia do cancro”, dito autor do estudo, Dr. Tal Danino.
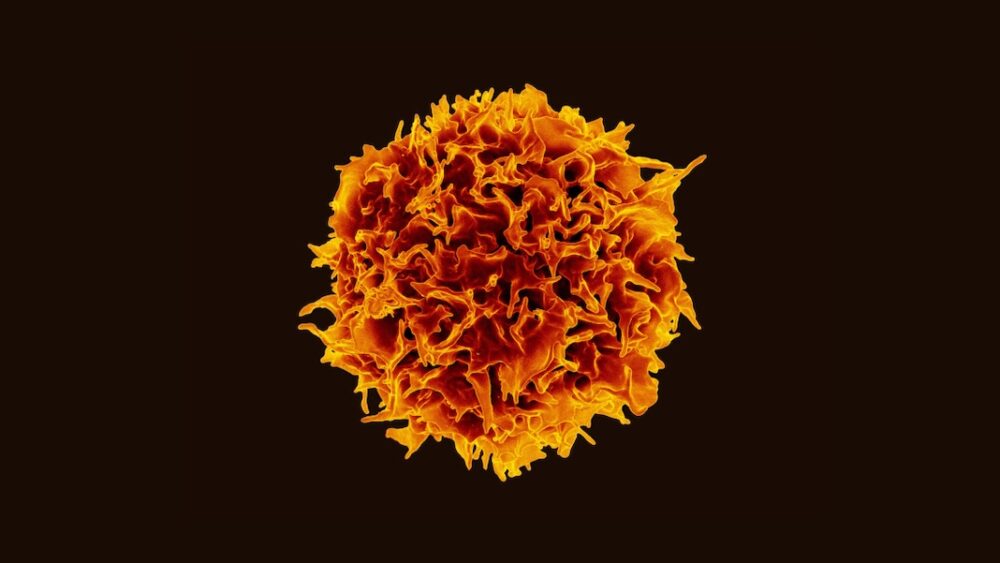
Crédito da imagem: Imagem colorida de microscópio eletrônico de varredura de uma célula T / NIAID
- Conteúdo com tecnologia de SEO e distribuição de relações públicas. Seja amplificado hoje.
- PlatoData.Network Gerativa Vertical Ai. Capacite-se. Acesse aqui.
- PlatoAiStream. Inteligência Web3. Conhecimento Amplificado. Acesse aqui.
- PlatãoESG. Carbono Tecnologia Limpa, Energia, Ambiente, Solar, Gestão de resíduos. Acesse aqui.
- PlatoHealth. Inteligência em Biotecnologia e Ensaios Clínicos. Acesse aqui.
- Fonte: https://singularityhub.com/2023/10/17/cancer-killing-duo-hunts-down-and-destroys-tumors-with-surprising-alacrity/
- :tem
- :é
- :não
- :onde
- $UP
- 2017
- 22
- 8
- a
- habilidades
- Sobre
- adicionado
- administração
- vantagens
- Depois de
- novamente
- contra
- agressivo
- Todos os Produtos
- Permitindo
- Aliado
- já
- tb
- quantidade
- an
- Apresentadora
- e
- Outro
- qualquer
- abordagem
- aprovou
- SOMOS
- áreas
- por aí
- AS
- At
- Ataques
- Atrai
- autor
- disponível
- avenidas
- evitar
- em caminho duplo
- Bactérias
- barreira
- baseado
- Batalha
- BE
- sido
- Começo
- Melhor
- Grande
- sangue
- corpo
- impulsionar
- nascido
- Boston
- Câncer de mama
- erros
- construir
- Constrói
- mas a
- by
- chamado
- CAN
- Câncer
- Células cancerosas
- terapia de câncer
- candidatos
- carro
- Carl
- Causar
- causando
- Células
- chances
- químico
- escolhido
- Clínico
- COLÔMBIA
- Comunidades
- comparado
- componentes
- conceito
- Interesse
- conteúdo
- contraste
- convencional
- poderia
- crédito
- danificar
- dia
- dias
- profundo
- Defesa
- depende
- Design
- projetado
- Designer
- destruir
- destruído
- diferente
- difícil
- diretamente
- doenças
- feito
- dosar
- down
- dr
- desenhar
- condução
- droga
- duo
- e
- facilidade
- fácil
- efeitos
- eficiência
- esforço
- engenheiro
- engenharia
- Engenharia
- eric
- especialmente
- estimativa
- Mesmo
- existente
- explorar
- Explorando
- Vacila
- fda
- Encontre
- Primeiro nome
- fluxo
- seguido
- comida
- Escolha
- Foundation
- da
- mais distante
- genético
- engenharia genética
- OFERTE
- dado
- vai
- agarrar
- Verde
- Growth
- Ter
- saudável
- ajudar
- altamente
- Como funciona o dobrador de carta de canal
- Contudo
- HTTPS
- Humanos
- caça
- imagem
- imediatamente
- Sistema imunológico
- melhorado
- in
- Incluindo
- aumentou
- aumentando
- cada vez mais
- infecções
- dentro
- para dentro
- envolvido
- IT
- ESTÁ
- se
- Junho
- assassinos
- grande
- Maior
- mínimo
- níveis
- como
- ligado
- pequeno
- vida
- Baixo
- fazer
- Fazendo
- muitos
- Posso..
- medicina
- método
- Microscópio
- molecular
- mais
- múltiplo
- nome
- natural
- Perto
- Novo
- NIH
- normal
- agora
- Casca de noz
- óbvio
- of
- WOW!
- on
- uma vez
- ONE
- queridos
- só
- para
- aberto
- or
- Outros
- A Nossa
- Fora
- resultados
- próprio
- Oxygen
- parte
- Pennsylvania
- por cento
- perfeita
- fase
- pioneiro
- sem caroço
- platão
- Inteligência de Dados Platão
- PlatãoData
- equilibrado
- população
- positivo
- potencial
- poderoso
- presente
- anteriormente
- Problema
- processo
- Produzido
- promessa
- prova
- prova de conceito
- protetor
- Proteína
- Proteínas
- fornece
- bomba
- Trimestre
- rapidamente
- alcançado
- prontamente
- reconhecimento
- Reduzido
- regiões
- relativamente
- liberar
- pesquisa
- investigador
- Resultados
- ROSA
- grosseiramente
- Dito
- satisfeito
- dimensionamento
- exploração
- Ciência
- cientistas
- Buscar
- parecem
- sensível
- Proteger
- tiros
- mostrou
- lado
- sinais
- Similarmente
- Tamanho
- sólido
- solução
- alguns
- solicitado
- especial
- específico
- Spot
- Ainda
- História
- estranho
- Estratégia
- caso
- Estudo
- surpreendente
- Em torno da
- vigilância
- sobrevivência
- sobreviver
- sintético
- .
- As células T
- TAG
- Tire
- Target
- alvejando
- tem como alvo
- Profissionais
- testes
- do que
- que
- A
- deles
- Eles
- então
- teoria
- Lá.
- Este
- deles
- isto
- para
- juntos
- transformadora
- transformado
- tratamento
- tratamentos
- troiano
- VIRAR
- dois
- tipo
- tipos
- Universal
- universidade
- us
- Comida dos EUA
- usar
- usava
- utilização
- geralmente
- utilidade
- variedade
- vincent
- viral
- vírus
- Vulnerável
- maneiras
- semanas
- peso
- BEM
- fui
- foram
- quando
- qual
- QUEM
- Largo
- precisarão
- Wilson
- Limpar
- de
- sem
- Wong
- trabalhou
- pior
- zefirnet