A degeneração macular relacionada à idade (DMRI) é uma das principais causas de cegueira. Inicia-se na barreira sanguínea externa da retina (oBRB) formada pelo epitélio pigmentar da retina (EPR), membrana de Bruch e coriocapilar. Os mecanismos de iniciação e progressão da DMRI ainda precisam ser melhor compreendidos devido à falta de modelos oBRB humanos fisiologicamente relevantes.
A equipe de pesquisa do National Eye Institute (NEI), parte do National Institutes of Health, utilizou pacientes células-tronco e bioimpressão 3D para produzir tecido ocular que avançará na compreensão dos mecanismos das doenças que causam cegueira. Os cientistas imprimiram uma combinação de células que formam a barreira externa da retina do sangue.
O epitélio pigmentar da retina (EPR), separado da coriocapilar rica em vasos sanguíneos por Membrana de Bruch, constitui a barreira externa sangue-retina. Os coriocapilares e o EPR trocam nutrientes e resíduos sob o controle da membrana de Bruch. Drusas, que são acúmulos de lipoproteínas, desenvolvem-se fora da membrana de Bruch na DMRI e obstruem sua função. A degradação do EPR ao longo do tempo causa deterioração dos fotorreceptores e perda de visão.
Os cientistas combinaram três tipos de células coróides imaturas em um hidrogel: pericitos, células endoteliais e fibroblastos. Eles então imprimiram o gel em uma estrutura biodegradável. Em poucos dias, as células começaram a amadurecer em uma densa rede capilar.
No nono dia, os cientistas semearam células epiteliais pigmentares da retina no outro lado da estrutura. O tecido impresso atingiu a maturidade total no dia 42. As análises dos tecidos e os testes genéticos e funcionais mostraram que o tecido impresso parecia e se comportava de forma semelhante à barreira sangue-retina externa nativa.
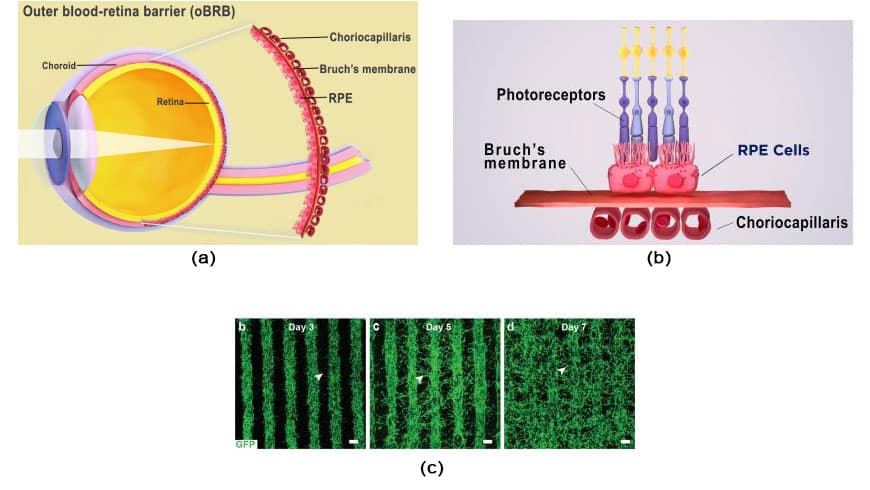
b. A barreira hemato-retiniana externa do olho compreende o epitélio pigmentar da retina, a membrana de Bruch e a coriocapilar. Crédito da imagem: National Eye Institute.
c. Crescimento de vasos sanguíneos através de linhas impressas de uma mistura de células endoteliais-pericito-fibroblastos. No sétimo dia, os vasos sanguíneos preenchem o espaço entre as fileiras, formando uma rede de capilares. Crédito da imagem: Kapil Bharti.
Quando submetido ao estresse, o tecido impresso exibiu características de DMRI em estágio inicial, como depósitos de drusas sob o EPR, e progrediu para DMRI em estágio seco e tardio, onde foi observada ruptura do tecido. Os baixos níveis de oxigênio causaram uma aparência úmida semelhante à DMRI com hiperproliferação vascular coroidal que se moveu para a zona sub-EPR. Quando usados para tratar a DMRI, os medicamentos anti-VEGF retardaram a formação e migração dos vasos sanguíneos, ao mesmo tempo que melhoraram a forma do tecido.
Kapil Bharti, Ph.D., que dirige a Seção NEI de Pesquisa Translacional Ocular e de Células-Tronco, disse: “Ao imprimir células, facilitamos a troca de sinais celulares necessários para a anatomia normal da barreira sangue-retina externa. Por exemplo, a presença de células RPE induz a expressão do gene mudanças nos fibroblastos que contribuem para a formação da membrana de Bruch – algo que foi sugerido há muitos anos, mas não foi comprovado até o nosso modelo.”
Os cientistas abordaram duas questões tecnológicas: criar uma estrutura biodegradável apropriada e alcançar um padrão de impressão consistente. Eles desenvolveram um hidrogel sensível à temperatura que produzia fileiras distintas enquanto o gel estava frio, mas se dissolvia quando o gel aquecia. Um sistema mais exato de avaliação da arquitetura tecidual foi possível graças à boa consistência das fileiras. Além disso, otimizaram a proporção de fibroblastos, células endoteliais e pericitos na combinação celular.
O coautor Marc Ferrer, Ph.D., diretor do Laboratório de Bioimpressão de Tecidos 3D do Centro Nacional para o Avanço das Ciências Translacionais do NIH, e sua equipe forneceram experiência para a biofabricação dos tecidos externos da barreira sangue-retina “em um poço, ”Juntamente com medições analíticas para permitir a triagem de drogas.
[Conteúdo incorporado]
“Nossos esforços colaborativos resultaram em modelos de tecido retiniano muito relevantes para doenças oculares degenerativas”, disse Ferrer. dito. “Tais modelos de tecidos têm muitos usos potenciais em aplicações translacionais, incluindo o desenvolvimento terapêutico.”
Jornal de referência:
- Min Jae Song, Russ Quinn e outros. A barreira externa da retina 3D bioimpressa revela o fenótipo coroidal dependente do EPR na degeneração macular avançada. Nature Methods, 2022, DOI: 10.1038/s41592-022-01701-1