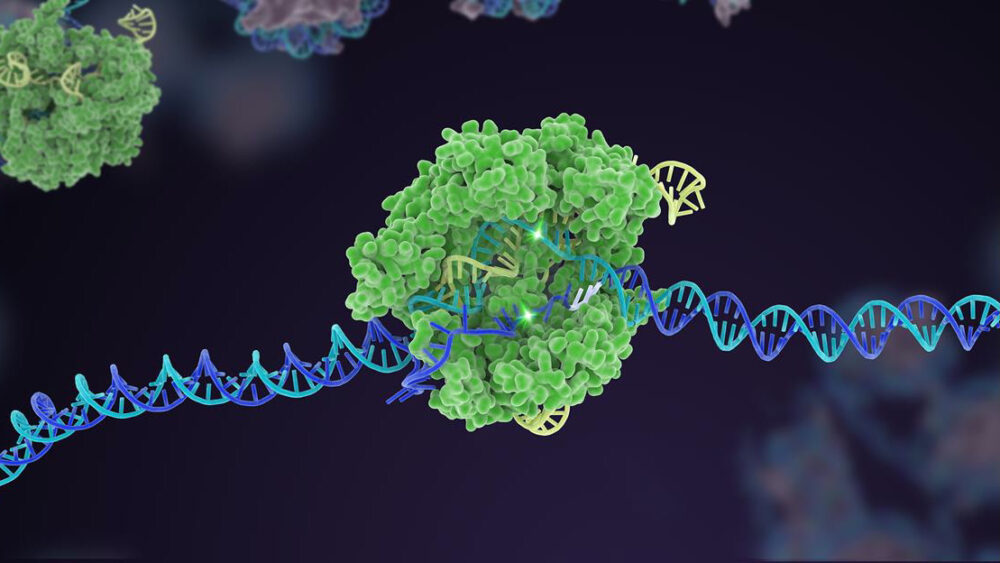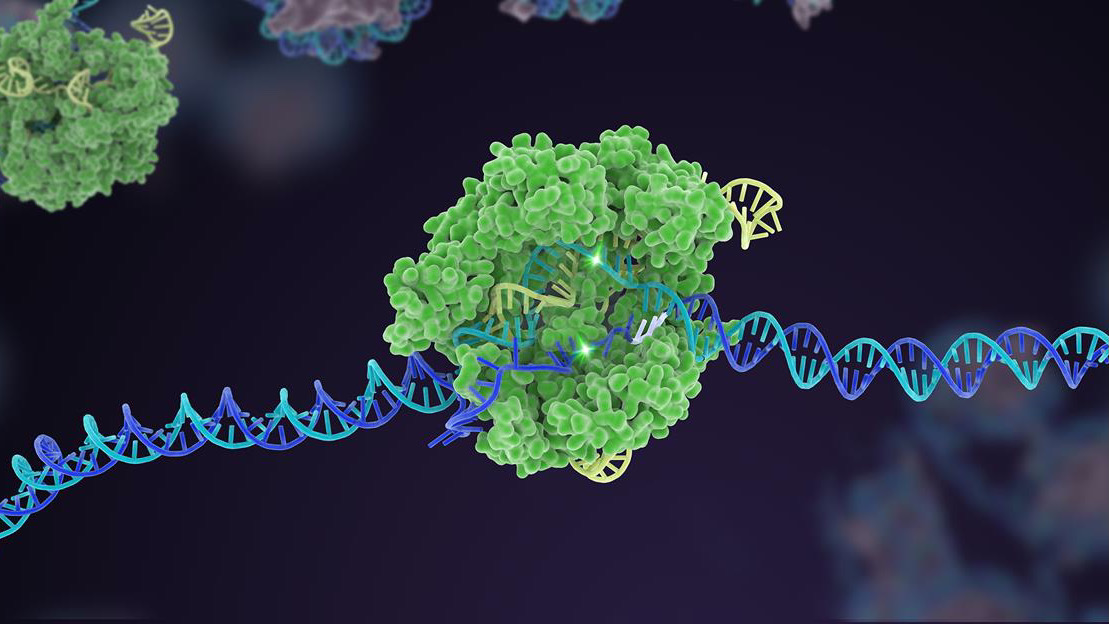
Dez anos atrás, um mecanismo de defesa bacteriano pouco conhecido disparou para a fama como um poderoso editor de genoma. Na década seguinte, o CRISPR-Cas9 gerou várias variantes, expandindo-se em uma caixa de ferramentas abrangente que pode editar o código genético da vida.
Longe de ser uma busca de torre de marfim, seus usos práticos em pesquisa, saúde e agricultura vieram rápido e furiosos.
Você viu as manchetes. A FDA aprovou seu uso em combatendo a mutação genética subjacente para a doença falciforme. Alguns pesquisadores Células imunológicas editadas para combater câncer de sangue intratável em crianças. outros levaram transplantes de órgãos de porco para humano do sonho à realidade na tentativa de amenizar a escassez de doadores de órgãos. Trabalhos recentes visam ajudar milhões de pessoas com colesterol alto - e potencialmente levar a terapia genética baseada em CRISPR para as massas - por diminuindo suas chances de doenças cardíacas com uma única injeção.
Mas para a Dra. Jennifer Doudna, que ganhou o Prêmio Nobel em 2020 por seu papel no desenvolvimento do CRISPR, estamos apenas arranhando a superfície de seu potencial. Juntamente com a estudante de pós-graduação Joy Wang, Doudna traçou um roteiro para a próxima década da tecnologia em um artigo in Ciência.
Se os anos 2010 foram focados em estabelecer a caixa de ferramentas CRISPR e provar sua eficácia, esta década é quando a tecnologia atinge todo o seu potencial. Desde terapias baseadas em CRISPR e telas em larga escala para diagnóstico de doenças até a engenharia de culturas de alto rendimento e alimentos nutritivos, a tecnologia “e seu impacto potencial ainda estão em seus estágios iniciais”, escreveram os autores.
Uma década de destaques
Nós gastamos muita tinta nos avanços do CRISPR, mas vale a pena revisitar o passado para prever o futuro - e potencialmente detectar problemas ao longo do caminho.
Um destaque inicial foi a incrível capacidade do CRISPR de projetar rapidamente modelos animais de doenças. Sua forma original elimina facilmente um gene alvo em um embrião muito jovem, que quando transplantado para um útero pode gerar camundongos geneticamente modificados em apenas um mês, em comparação com um ano usando métodos anteriores. Versões CRISPR adicionais, como edição de base - troca de uma letra genética por outra - e edição primária - que corta o DNA sem cortar as duas fitas - aumentaram ainda mais a flexibilidade do kit de ferramentas na engenharia de organoides geneticamente alterados (pense em mini-cérebros) e animais. O CRISPR rapidamente estabeleceu dezenas de modelos para algumas de nossas doenças mais devastadoras e desconcertantes, incluindo vários tipos de câncer, Alzheimer e distrofia muscular de Duchenne – um distúrbio degenerativo no qual o músculo lentamente se desgasta. Dezenas de ensaios baseados em CRISPR estão agora nas obras.
O CRISPR também acelerou a triagem genética na era do big data. Em vez de atingir um gene de cada vez, agora é possível silenciar ou ativar milhares de genes em paralelo, formando uma espécie de pedra de Roseta para traduzir perturbações genéticas em mudanças biológicas. Isso é especialmente importante para entender as interações genéticas, como as do câncer ou envelhecimento das quais não tínhamos conhecimento anteriormente, e ganhar nova munição para o desenvolvimento de medicamentos.
Mas uma conquista importante para o CRISPR foi a edição multiplexada. Como tocar simultaneamente em várias teclas de piano, esse tipo de engenharia genética atinge várias áreas específicas do DNA, mudando rapidamente a composição genética de um genoma de uma só vez.
A tecnologia funciona em plantas e animais. Por eras, as pessoas cultivaram meticulosamente colheitas com características desejáveis - seja cor, tamanho, sabor, nutrição ou resistência a doenças. O CRISPR pode ajudar a selecionar várias características ou até mesmo domesticar novas culturas em apenas uma geração. Touros sem chifres gerados por CRISPR, tomate rico em nutrientese animais de fazenda hipermusculosos e peixes já são realidade. Com a população mundial atingindo 8 bilhões em 2022 e milhões que sofrem de fome, CRISPRed-crops pode oferecer uma tábua de salvação - isto é, se as pessoas estiverem dispostas a aceitar a tecnologia.
O caminho a seguir
Para onde vamos a partir daqui?
Para os autores, precisamos aumentar ainda mais a eficácia do CRISPR e construir confiança. Isso significa voltar ao básico para aumentar a exatidão e a precisão de edição da ferramenta. Aqui, as plataformas para desenvolver rapidamente as enzimas Cas, o componente “tesoura” do maquinário CRISPR, são críticas.
Já houve sucessos: uma versão Cas, por exemplo, atua como uma proteção para o componente de direcionamento - o sgRNA “bloodhound”. No CRISPR clássico, o sgRNA funciona sozinho, mas nesta versão atualizada, ele luta para se ligar sem a ajuda do Cas. Esse truque ajuda a adaptar a edição a um local de DNA específico e aumenta a precisão para que o corte funcione conforme previsto.
Estratégias semelhantes também podem aumentar a precisão com menos efeitos colaterais ou inserir novos genes em células como neurônios e outras que não se dividem mais. Embora já seja possível com a edição principal, sua eficiência pode ser 30 vezes menor do que os mecanismos CRISPR clássicos.
“O principal objetivo da edição prime na próxima década é melhorar a eficiência sem comprometer a pureza do produto de edição – um resultado que tem o potencial de transformar a edição prime em uma das ferramentas mais versáteis para edição de precisão”, disseram os autores.
Mas talvez mais importante seja a entrega, que continua sendo um gargalo especialmente para a terapêutica. Atualmente, o CRISPR é geralmente usado em células fora do corpo que são infundidas de volta – como no caso do CAR-T – ou, em alguns casos, amarradas a um portador viral ou encapsuladas em bolhas de gordura e injetadas no corpo. Houve sucessos: em 2021, a FDA aprovou o primeira injeção baseada em CRISPR para enfrentar uma doença genética do sangue, a amiloidose por transtirretina.
No entanto, ambas as estratégias são problemáticas: poucos tipos de células podem sobreviver ao tratamento CAR-T – morrendo quando reintroduzidos no corpo – e o direcionamento de tecidos e órgãos específicos permanece fora do alcance das terapias injetáveis.
Um avanço importante para a próxima década, disseram os autores, é transportar a carga CRISPR para o tecido alvo sem causar danos e liberar o editor de genes no local pretendido. Cada uma dessas etapas, embora aparentemente simples no papel, apresenta seu próprio conjunto de desafios que exigirão tanto a bioengenharia quanto a inovação para superar.
Finalmente, o CRISPR pode criar sinergia com outros avanços tecnológicos, disseram os autores. Por exemplo, ao explorar imagens de células e aprendizado de máquina, em breve poderíamos projetar editores de genoma ainda mais eficientes. Graças a sequenciamento de DNA mais rápido e barato, podemos monitorar facilmente as consequências da edição de genes. Esses dados podem fornecer um tipo de mecanismo de feedback com o qual projetar editores de genoma ainda mais poderosos em um loop virtuoso.
Impacto no mundo real
Embora expandir ainda mais a caixa de ferramentas CRISPR esteja na agenda, a tecnologia está suficientemente madura para impactar o mundo real em sua segunda década, disseram os autores.
Em um futuro próximo, devemos ver “um número crescente de tratamentos baseados em CRISPR passando para estágios posteriores de ensaios clínicos”. Olhando para o futuro, a tecnologia, ou suas variantes, poderia tornar os xenotransplantes de órgãos de porco para humanos uma rotina, em vez de experimentais. Telas em larga escala para genes que levam ao envelhecimento ou doenças cerebrais ou cardíacas degenerativas - nossos principais assassinos hoje - podem render tratamentos profiláticos baseados em CRISPR. Não é uma tarefa fácil: precisamos tanto do conhecimento da genética por trás das doenças genéticas multifacetadas — ou seja, quando vários genes entram em ação — quanto de uma maneira de entregar as ferramentas de edição ao seu alvo. “Mas os benefícios potenciais podem impulsionar a inovação nessas áreas muito além do que é possível hoje”, disseram os autores.
No entanto, com maior poder vem maior responsabilidade. O CRISPR avançou a uma velocidade vertiginosa, e as agências reguladoras e o público ainda estão lutando para alcançá-lo. Talvez o exemplo mais notório tenha sido o da Bebês CRISPR, onde experimentos realizados contra as diretrizes éticas globais impulsionado um consórcio internacional para estabelecer uma linha vermelha para a edição de células germinativas humanas.
Da mesma forma, os organismos geneticamente modificados (OGMs) continuam sendo um tema controverso. Embora o CRISPR seja muito mais preciso do que as ferramentas genéticas anteriores, caberá aos consumidores decidir se aceitam ou não uma nova geração de alimentos desenvolvidos pelo homem-tanto vegetal quanto animal.
Esses são conversas importantes que precisam de um discurso global já que o CRISPR entra em sua segunda década. Mas para os autores, o futuro parece brilhante.
“Assim como durante o advento da edição do genoma CRISPR, uma combinação de curiosidade científica e o desejo de beneficiar a sociedade impulsionará a próxima década de inovação na tecnologia CRISPR”, disseram eles. “Ao continuar a explorar o mundo natural, vamos descobrir o que não pode ser imaginado e colocá-lo em uso no mundo real para o benefício do planeta.”
Crédito de imagem: NIH
- Conteúdo com tecnologia de SEO e distribuição de relações públicas. Seja amplificado hoje.
- Platoblockchain. Inteligência Metaverso Web3. Conhecimento Ampliado. Acesse aqui.
- Fonte: https://singularityhub.com/2023/01/25/crisprs-wild-first-decade-only-scratches-the-surface-of-its-potential/
- 2020
- a
- habilidade
- acelerado
- ACEITAR
- precisão
- realização
- atos
- Adicional
- avançar
- avançado
- avanços
- advento
- contra
- agências
- agenda
- Envelhecendo
- agricultura
- à frente
- visa
- aliviar
- sozinho
- já
- Apesar
- A doença de Alzheimer
- munição
- e
- animal
- animais
- aprovou
- áreas
- Assistência
- autores
- em caminho duplo
- base
- fundamentos básicos
- beneficiar
- Benefícios
- Berkeley
- Pós
- Grande
- Big Data
- bilhão
- vincular
- sangue
- Bloomberg
- corpo
- impulsionar
- Impulsionado
- Cérebro
- trazer
- construir
- ganhar confiança
- Câncer
- não podes
- casas
- casos
- luta
- Células
- desafios
- chances
- Alterações
- mudança
- mais barato
- clássico
- Clínico
- ensaios clínicos
- código
- cor
- combinação
- como
- comparado
- componente
- compreensivo
- comprometendo
- Consequências
- consórcio
- Consumidores
- continuar
- controverso
- conversas
- poderia
- crédito
- CRISPR
- crítico
- culturas
- curiosidade
- Atualmente
- Cortar
- corte
- dados,
- década
- Defesa
- entregar
- Entrega
- em desenvolvimento
- Desenvolvimento
- descobrir
- Doença
- doenças
- dna
- down
- dezenas
- seu "Sonho"
- distância
- droga
- durante
- cada
- Cedo
- facilmente
- editor
- eficácia
- efeitos
- eficiência
- eficiente
- encapsulado
- engenheiro
- Engenharia
- Entra
- especialmente
- estabelecido
- estabelecendo
- considerações éticas
- Mesmo
- evolui
- exemplo
- expansão
- explorar
- FAME
- fazenda
- RÁPIDO
- fda
- retornos
- lutar
- Primeiro nome
- Flexibilidade
- focado
- alimentos
- formulário
- da
- cheio
- mais distante
- futuro
- ganhando
- geralmente
- gerar
- geração
- engenharia genética
- Genética
- Global
- Go
- meta
- vai
- pós-graduação
- maior
- orientações
- headlines
- saúde
- Coração
- ajudar
- ajuda
- SUA PARTICIPAÇÃO FAZ A DIFERENÇA
- Alta
- Destaques
- HTTPS
- humano
- Imagiologia
- Impacto
- importante
- melhorar
- in
- Incluindo
- Crescimento
- aumentou
- Aumenta
- incrível
- Inovação
- interações
- Internacionais
- IT
- Jennifer
- apenas um
- Chave
- chaves
- assassinos
- Tipo
- Conhecimento
- em grande escala
- conduzir
- aprendizagem
- emprestar
- carta
- vida
- Line
- mais
- procurando
- OLHARES
- máquina
- aprendizado de máquina
- maquinaria
- a Principal
- fazer
- maquiagem
- muitos
- maduro
- significa
- mecanismo
- métodos
- milhões
- modelos
- modificada
- Monitore
- Mês
- mais
- mais eficiente
- a maioria
- em movimento
- multifacetado
- múltiplo
- natural
- Natureza
- Perto
- você merece...
- Neurônios
- Novo
- Próximo
- NHS
- NIH
- premio Nobel
- notório
- número
- ONE
- original
- Outros
- Outros
- lado de fora
- Superar
- próprio
- Papel
- Paralelo
- passado
- caminho
- país
- Pessoas
- possivelmente
- avião
- Plants
- Plataformas
- platão
- Inteligência de Dados Platão
- PlatãoData
- Abundância
- população
- possível
- potencial
- potencialmente
- poder
- poderoso
- Prática
- Precisão
- predizer
- previsto
- presentes
- anterior
- anteriormente
- Prime
- prêmio
- problemas
- Produto
- fornecer
- público
- colocar
- rapidamente
- alcançar
- Chega
- reais
- mundo real
- Realidade
- recentemente
- Vermelho
- reguladores
- liberar
- permanecem
- permanece
- requerer
- pesquisa
- pesquisadores
- resiliência
- responsabilidade
- Rico
- roadmap
- Tipo
- Dito
- Ciência
- batedor
- peneiramento
- telas
- Segundo
- conjunto
- escassez
- rede de apoio social
- lado
- Silêncio
- simples
- simultaneamente
- desde
- solteiro
- local
- Tamanho
- Lentamente
- So
- Sociedade
- alguns
- específico
- velocidade
- Spot
- girou
- Estágio
- Passos
- Ainda
- PEDRA
- estratégias
- Lutas
- Lutando
- estudante
- tal
- sofrimento
- superfície
- sobreviver
- Target
- visadas
- alvejando
- tem como alvo
- Tarefa
- tecnológica
- Equipar
- A
- O Básico
- o mundo
- deles
- terapêutica
- milhares
- tempo
- vezes
- para
- hoje
- juntos
- Caixa de ferramentas
- ferramentas
- topo
- tópico
- Torre
- ensaios
- Confiança
- VIRAR
- tipos
- UN
- subjacente
- compreensão
- Atualizada
- usar
- vário
- versátil
- versão
- boas-vindas
- O Quê
- O que é a
- se
- qual
- enquanto
- QUEM
- Selvagem
- precisarão
- disposto
- sem
- Ganhou
- Atividades:
- trabalho
- mundo
- ano
- anos
- Produção
- zefirnet