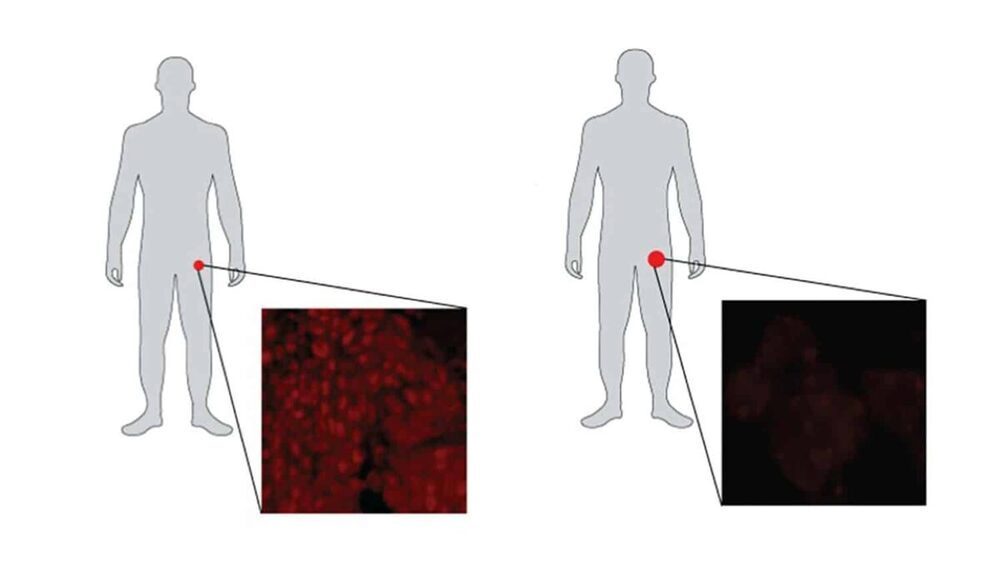
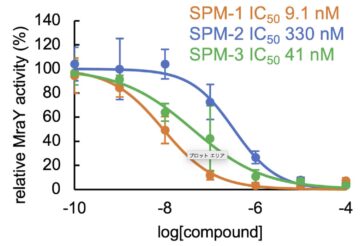
Андроген-депривационная терапия (АДТ) является основным методом лечения метастатического рака предстательной железы, но прогрессирование до кастрационно-резистентного рака предстательной железы (КРРПЖ) почти повсеместно. В последние годы были разработаны мощные ингибиторы андрогенных рецепторов (АР), в том числе антагонист АР энзалутамид.
Несмотря на то, что в большинстве случаев эти препараты эффективны, в конечном итоге они могут перестать работать, однако понимание того, как происходит это изменение, ограничено. Новое исследование от Мичиганский университет Онкологический центр Рогеля предполагает, что ингибиторы рецепторов андрогенов могут коренным образом перестраивать и изменять функцию опухолей предстательной железы, а в некоторых случаях даже делать их более агрессивными.
Джоши Алумкал, доктор медицинских наук, профессор семейной онкологии Вича и профессор внутренней медицины, чья команда провела это исследование в сотрудничестве с лабораторией Чжэн Ся в Институте рака Рыцаря Университета здоровья и наук Орегона, сказал: «Самой большой неудовлетворенной потребностью в клинике сейчас является понимание обходных путей в опухоли, которая становится устойчивой к препаратам, нацеленным на андрогенные рецепторы, чтобы мы могли определить, как лучше всего лечить пациента, чья опухоль начала расти».
«Как только энзалутамид перестанет работать, возможности будут ограничены. Мы не знаем, как и почему большинство опухолей становятся резистентными».
Ученые хотели понять, что было в этих опухолях для начала, и что произошло после того, как опухоли начали расти при лечении энзалутамидом. Пациенты были включены в долгосрочное исследование по сбору метастатических биопсий до и после того, как опухоль развила резистентность к терапии. Ученые получили повторные образцы от 21 пациента, что позволило им понять механизмы, действующие в опухоли каждого пациента.
Алумкал говорит, «Это самая большая коллекция соответствующих метастатических биопсий до и после применения энзалутамида. Чтобы понять устойчивость к лекарствам, исследователи часто собирают образцы у некоторых пациентов до лечения и у другой группы, чьи опухоли устойчивы к лечению. Однако этот подход гораздо менее точен, поскольку между этими пациентами могут быть и другие существенные различия. Вы не можете точно определить, имеют ли различия какое-либо отношение к воздействию наркотиков или больше связаны с тем, что опухоли просто разные».
Метод последовательного отбора образцов дает более четкое представление о том, как может возникнуть устойчивость к энзалутамиду.
После сравнения исходного образца с образцом прогрессирования от того же пациента ученые не обнаружили значительных изменений экспрессии генов в большинстве опухолей.
Алумкал говорит, «То, что программа генной экспрессии опухоли до лечения выглядела очень похожей на прогрессирование при лечении энзалутамидом, весьма примечательно. Это говорит о том, насколько хорошо большинство опухолей могут адаптироваться и поддерживать двигатель рецептора андрогена, несмотря на лечение энзалутамидом».
Но это был не единственный сюрприз.
В трех из 21 случая Алумкал и его команда увидели глубокий сдвиг в проводке опухолей или программе экспрессии генов.
Алумкал сказал, «Мы знали, что иногда опухоли становятся независимыми от топлива и больше не зависят от рецептора андрогена. Вместо этого эти опухоли включают программу экспрессии генов, более распространенную в нервных клетках, а не в клетках простаты, и переходят в агрессивную форму, называемую нейроэндокринным раком простаты».
«В 15 процентах случаев опухоли также стали независимыми от топлива по другой причине. Эти опухоли были связаны уникальным образом и наиболее соответствовали подтипу рака простаты, называемому двойным негативным раком простаты, что означает, что опухоли больше не имели рецептора андрогена в качестве двигателя. Но они также не стали нейроэндокринным раком простаты».
«Изначально почти все опухоли предстательной железы являются пожирателями газа: очень зависимы от топлива и питаются от рецептора андрогена в качестве двигателя. При лечении гормональными препаратами большинство опухолей остаются зависимыми от топлива, но становятся более экономичными, способными двигаться дальше с меньшим количеством бензина».
«Наша работа показала, что большинство опухолей — даже после приема энзалутамида — остаются очень зависимыми от топлива, что говорит о том, что продолжение воздействия на рецептор андрогена может иметь огромное значение для этих опухолей».
Алумкал обнаружил, что три опухоли превратились в двойной негативный рак простаты, что сродни электромобилю. Бензиновый двигатель был заменен совершенно другим набором механизмов, которые позволяли опухолям расти и выживать. «Мутации ДНК, обнаруженные в исходной и прогрессирующей биопсии этих конверторных опухолей, были одинаковыми, что убедительно свидетельствует о том, что энзалутамид полностью перепрограммировал двигатель исходной топливно-зависимой опухоли, чтобы он стал независимым от топлива при прогрессировании заболевания. Это драматический сдвиг, чтобы обернуть голову ».
Команда Алумкала обнаружила определенные гены, которые были высоко экспрессированы в исходных опухолях, которые в конечном итоге развились в дважды негативный рак простаты, несмотря на то, что исходные опухоли имели схожий вид под микроскопом. Это открытие подразумевает, что некоторые опухоли существуют в гибридном состоянии, изначально зависящем от топлива, но подверженном развитию в дважды негативный рак простаты после терапии энзалутамидом.
Квасцы говорит, «Результаты метода последовательного отбора проб показывают, что энзалутамид вызывает адаптацию опухолей, в некоторых случаях резко».
Алумкал отмечает, что «Сигнатура гена, которую он определил, является предварительной, и команде предстоит еще много работы. Тем не менее тот факт, что ДНК похожий вид в конвертерах убедительно указывает на то, что энзалутамид перепрограммирует опухоли. У нас есть еще много работы, но, возможно, удастся заранее выявить пациентов с наибольшим риском того, что их опухоль станет независимой от топлива после лечения такими препаратами, как энзалутамид».
Справочник журнала:
- Вестбрук Т.С., Гуан X., Роданский Э. и соавт. Транскрипционное профилирование совпадающих биопсий пациентов проясняет молекулярные детерминанты индуцированной энзалутамидом клональной пластичности. Nat Commun 13, 5345 (2022). ДОИ: 10.1038/s41467-022-32701-6