Inovacije v protonski terapiji so bile v ospredju letnega srečanja ASTRO, skupaj z napredkom v drugih najsodobnejših modalitetah – med njimi z MR vodeno adaptivno radioterapijo, kombiniranimi pristopi imunoterapije in radioterapije ter stereotaktičnimi zdravljenji oligometastatske bolezni. Joe McEntee poročila.
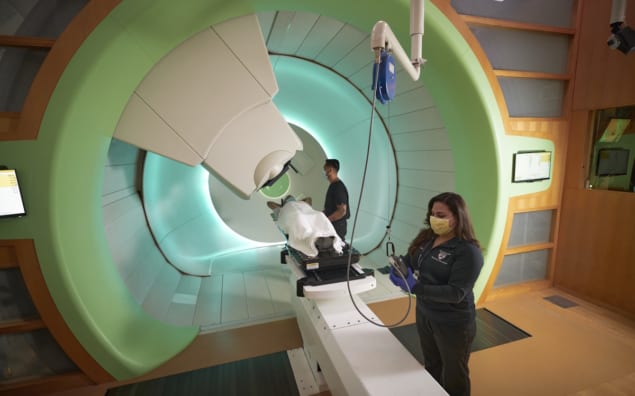
Medtem ko je protonska terapija resnično prispela kot glavna možnost zdravljenja v onkologiji z obsevanjem – trenutno je v ZDA 42 delujočih protonskih objektov in nadaljnjih 13 centrov v izgradnji – je očitno, da se klinična inovacija šele začenja, ko gre za obsežna uporaba protonov za zdravljenje raka. To je eden od ključnih zaključkov, ki izhajajo iz posebnega konferenčnega zasedanja – Inovativni pristopi radioterapije: koristi, izzivi, globalna perspektiva – na Letno srečanje ASTRO v San Diegu, CA, v začetku tega meseca.
Kar zadeva natančno ciljanje, je primer protonske terapije v primerjavi s konvencionalno radioterapijo dovolj jasen. Pomislite na podobne lastnosti ubijanja tumorjev kot fotoni, vendar z izrazito zmanjšanim odmerkom za normalno tkivo. Vse to pomaga ekipi radiološke onkologije pri zdravljenju tumorjev v bližini ogroženih organov (OAR), s potencialom zmanjšanja stranskih učinkov in zapletov na poti.
"Protoni sprostijo vso svojo energijo na točki in se nato ustavijo," je pojasnil James Metz, predsednik radiacijske onkologije na Univerzi v Pensilvaniji (UPenn) in izvršni direktor OncoLink storitev izobraževanja o raku. To pomeni, da ni doze sevanja preko tarče, kot tudi veliko manjša doza, ki je odložena pred tarčo v primerjavi s fotonskim in elektronskim obsevanjem.

Kot taki lahko kliniki ciljajo na tumor plast za plastjo z dovajanjem protonov, skeniranim s snopom svinčnika. »Vzamemo tumor, ga voksel za vokselom razdelimo na 5 mm3 volumne in vzemite ta žarek svinčnika ter obdelajte [kompleksne strukture] točko za točko brez absolutno nobenega izhodnega odmerka,« je opozoril Metz. "Protoni nam dajejo priložnost, da zmanjšamo odmerek na normalne strukture, združimo s kemoterapijo in imunoterapijo ter povečamo odmerke [sevanja] v prihodnje."
Ne glede na trenutno uvajanje sistemov protonske terapije v razvitem svetu – klinično sprejemanje je podobno za ZDA, Evropo in Azijo, čeprav trenutno obstaja le en center za protonsko zdravljenje v podsaharski Afriki – je očitno, da dokazi »zlatega standarda« za klinično učinkovitost protonov je še vedno v teku. "Moramo sistematično ovrednotiti klinični potencial in ga opredeliti s pomočjo stroge znanosti – s kvantificiranjem koristi v primerjavi z naložbo," je trdil Metz. "Navsezadnje so potrebni znatni viri in infrastruktura za podporo centra za protonsko terapijo."
Dokazi prihajajo – in to prej kot slej. Številna randomizirana klinična preskušanja faze III zbirajo podatke ali so bila pred kratkim zaključena za različne znake raka (vključno z rakom pljuč, požiralnika, jeter, glave in vratu ter možganov). Medtem se tudi pragmatična preskušanja dobro razvijajo in ocenjujejo protonsko zdravljenje v rutinski klinični praksi za bolnike z rakom dojke in rakom prostate.
FLASH disruptor
Metz je eden od kliničnih pionirjev protonske terapije, saj je vodil razvojni program za Robertsov center za protonsko terapijo v Philadelphiji – ustanova, ki je zdravila na tisoče bolnikov z rakom z uporabo protonov, odkar je odprla svoja vrata leta 2010. Klinična inovacija je to, kar je, vendar se pozornost že obrača na to, kar se oglašuje kot "naslednja velika stvar" v terapiji z delci: FLASH protonska terapija.
Za kontekst je FLASH eksperimentalni način zdravljenja, ki vključuje dovajanje ultravisokih odmerkov (nad 60–80 Gy/s) ionizirajočega sevanja (elektronov, fotonov ali protonov) v zelo kratkem času (manj kot 1 s). Predklinične študije so pokazale, da je radioterapija FLASH manj toksična za normalna tkiva in enako učinkovita kot običajna radioterapija pri uničevanju tumorjev. Če so sheme zdravljenja FLASH široko potrjene, lahko torej spremenijo radioterapijo – tako da bi lahko večje odmerke varno dostavili tumorjem ali pa dali uveljavljene odmerke z zmanjšano toksičnostjo za OAR.
Skratka, protonska terapija FLASH se oblikuje kot prihodnji motilec v radiološki onkologiji, je trdil Metz, "združuje biologijo in tehnologijo na nove načine ... in radiobiologijo nekoliko obrača na glavo". Prednosti se že kažejo. Za začetek bi lahko protonska terapija FLASH znatno skrajšala čas zdravljenja z obsevanjem, tako da postane radioterapija bolj podobna kirurškemu posegu.

Bodo ultravisoke hitrosti odmerka v hipu spremenile radioterapijo?
To je dobra novica za pacienta na več koordinatah – odpiranje poti do izboljšane kakovosti življenja, zmanjšane toksičnosti in stranskih učinkov ter veliko manj časa, preživetega na kliniki. Na bolj temeljni ravni lahko obsevanje FLASH sproži tudi različne imunske poti in izražanje genov, kar ustvarja nove priložnosti za kombinacije zdravil in sevanja.
Kljub temu, da ima FLASH potencial, da spremeni paradigme zdravljenja in številne trenutne predpostavke o izvajanju sevanja, je Metz sklenil s previdnostjo: »Rekel bi, da protonska terapija FLASH še ni pripravljena za najboljšo uporabo ... [in] ni pripravljena za nadaljnjo uporabo kot nekaj centrov z velikimi sredstvi, ki lahko dokončajo ustrezne raziskave in klinična preskušanja.«
Klinične inovacije: vse je odvisno od rezultatov
Poleg kliničnih priložnosti, ki jih ponuja protonska terapija, je seja ASTRO o inovativnih pristopih radioterapije pokrivala številne druge podlage. Tamer Refaat, profesor radiacijske onkologije na univerzi Loyola v Chicagu, Illinois, začelo s poročilom o statusu radioterapije, vodene z MR (MRgRT).
»Velika stvar [z MRgRT] je prilagajanje v realnem času,« je Refaat dejal delegatom. Z drugimi besedami, personalizirana, dnevno prilagojena radioterapija, ki temelji na anatomiji pacienta v realnem času in na mizi, kar kliničnemu timu omogoča maksimiranje odmerka do ciljnega volumna in minimiziranje odmerka za OAR.
Kar zadeva inovacije MRgRT, ki si jih je treba ogledati, je Refaat poudaril komercialno in klinično uvedbo funkcije cine-gating za izboljšanje zdravljenja tumorjev zgornjega dela trebuha v eni sami fazi dihanja. "Žarek sevanja se vklopi vedno, ko je tarča znotraj meje sledenja, in se izklopi, ko je zunaj," je pojasnil (dodal, da je slaba stran daljši čas na mizi za zdravljenje pacienta).

V središču pozornosti je bila tudi vključitev funkcionalnega MRgRT v potek dela MR-Linac, pri čemer je Refaat navedel raziskovalce na Center za raka MD Anderson (Houston, Teksas) med zgodnjimi uporabniki, ki želijo identificirati radiorezistentne subvolume tumorja in ustrezno povečati odmerek za te subvolume.
Druga vroča tema je bila osredotočena na sinergije kombiniranega načina vključevanja zdravljenja raka z imunoterapijo in radioterapijo. Govorka Silvia Formenti, radiološka onkologinja pri Weill Cornell Medicine v New Yorku, je eden od glavnih nosilcev spremembe paradigme v radiobiologiji, njena prizadevanja pojasnjujejo vlogo ionizirajočega sevanja na imunski sistem, hkrati pa dokazujejo učinkovitost kombiniranih režimov radioterapije in imunoterapije pri solidnih tumorjih.
Formenti je poudaril ključno vlogo, ki jo ima v zvezi s tem ImmunoRad Radiation Oncology-Biology Integration Network (ROBIN). Multidisciplinarno sodelovanje pri raziskavah in razvoju med ameriškimi in evropskimi centri za raka, ROBIN si prizadeva bolje razumeti medsebojno delovanje radioterapije in imunskega odziva – kot tudi negovanje nabora talentov znanstvenikov na začetku kariere na tem področju. Prav zdaj, je opozoril Formenti, je širša slika zamegljena zaradi "finančne toksičnosti", pri čemer so se stroški imunoterapije izkazali za previsoke za večino držav z nizkimi in srednjimi dohodki - pa tudi za številne Američane.
Osredotočenost na skupne klinične raziskave je ponovil Stephen Harrow, svetovalec klinični onkolog pri Edinburški center za raka na Škotskem. V zadnjem govoru seje je razpravljal o uporabi stereotaktične radioterapije telesa (SBRT) za oligometastatsko bolezen.
Harrow je po pandemiji poudaril, kako je škotska mreža Oligomet SABR (SOSN), ki jo podpira 1 milijon funtov škotskega državnega financiranja, petim škotskim centrom za raka omogočila, da ponudijo združeno storitev zdravljenja SBRT bolnikom po vsej državi (ne samo zelo poseljen osrednji pas, ki obsega Glasgow in Edinburgh).
Cilj SOSN, je pojasnil, je "zgraditi mrežo zdravnikov, fizikov in radiografov, tako da se vsi strinjamo glede izbire pacientov [merila za SBRT] in da imamo enakost za paciente po vsej državi". Še več, je dodal, "dokazi vsekakor gradijo, da lahko vplivate na rezultate bolnikov s SBRT za oligometno bolezen."
- Distribucija vsebine in PR s pomočjo SEO. Okrepite se še danes.
- PlatoData.Network Vertical Generative Ai. Opolnomočite se. Dostopite tukaj.
- PlatoAiStream. Web3 Intelligence. Razširjeno znanje. Dostopite tukaj.
- PlatoESG. Ogljik, CleanTech, Energija, Okolje, sončna energija, Ravnanje z odpadki. Dostopite tukaj.
- PlatoHealth. Obveščanje o biotehnologiji in kliničnih preskušanjih. Dostopite tukaj.
- vir: https://physicsworld.com/a/proton-therapy-on-an-upward-trajectory-while-flash-treatment-schemes-get-ready-to-shine/
- :ima
- : je
- :ne
- $GOR
- 1
- 100
- 13
- a
- Sposobna
- O meni
- nad
- absolutno
- ustrezno
- čez
- prilagoditev
- prilagodljivo
- dodano
- dodajanje
- napredek
- privoščiti
- Afrika
- dogovorjene
- vsi
- Dovoli
- skupaj
- že
- Prav tako
- Čeprav
- Američani
- med
- an
- anatomija
- in
- in infrastrukturo
- anderson
- letno
- očitno
- uporaba
- pristopi
- primerno
- SE
- trdili
- prispeli
- AS
- asia
- predpostavke
- At
- pozornosti
- temeljijo
- BE
- Širina
- postane
- zadaj
- počutje
- Prednosti
- Boljše
- med
- Poleg
- Big
- večji
- biologija
- telo
- Meja
- Brain
- Rak na dojki
- dihanje
- splošno
- Building
- vendar
- by
- CA
- prišel
- CAN
- rak
- primeru
- center
- Osrednji
- center
- centri
- Stol
- izzivi
- Chicago
- jasno
- klik
- Ambulanta
- klinični
- klinične inovacije
- kliničnih preskušanj
- kliniki
- Zapri
- zaprto
- sodelovanje
- sodelovanje
- kombinacije
- združujejo
- kombinirani
- prihaja
- prihajajo
- komercialna
- v primerjavi z letom
- dokončanje
- kompleksna
- sklenjene
- Konferenca
- Gradbeništvo
- svetovalec
- ozadje
- konvencionalne
- Cornell
- strošek
- bi
- država
- zajeti
- Ustvarjanje
- Merila
- Trenutna
- Trenutno
- vrhunsko
- datum
- dan
- ponudba
- zmanjšala
- namenjen
- opredeliti
- vsekakor
- dostop delegat
- dostavi
- dostava
- dokazuje
- razporejeni
- uvajanje
- deponiran
- razvili
- Razvoj
- Diego
- drugačen
- Direktor
- razpravljali
- bolezen
- motil
- razne
- razdeli
- vrata
- Odmerek
- slaba stran
- drog
- vsak
- prej
- odmevala
- Izobraževanje
- Učinkovito
- učinkovitost
- prizadevanja
- pojavljajo
- omogočena
- obsežno
- energija
- okrepi
- dovolj
- pravičnost
- stopnjevati
- ustanovljena
- Evropa
- Evropski
- oceniti
- ocenjevanje
- dokazi
- očitno
- izvršni
- Izvršni direktor
- Izhod
- eksperimentalni
- razložiti
- izraz
- objekti
- Sklad
- daleč
- Nekaj
- Polje
- končna
- pet
- Flash
- Osredotočite
- za
- iz
- spredaj
- funkcionalno
- funkcionalnost
- temeljna
- Financiranje
- nadalje
- Prihodnost
- dobili
- pridobivanje
- Daj
- dana
- Globalno
- Cilj
- dogaja
- dobro
- vlada
- Imajo
- ob
- he
- Glava
- Pomaga
- jo
- več
- Poudarjeno
- zelo
- njegov
- HOT
- houston
- Kako
- Vendar
- HTTPS
- identificirati
- if
- iii
- Illinois
- slika
- Imunski sistem
- imunoterapija
- izboljšalo
- in
- V drugi
- Vključno
- Povečajte
- indikacije
- vplivajo
- Podatki
- Infrastruktura
- Inovacije
- novosti
- inovativne
- Povezovanje
- integracija
- interakcije
- v
- naložbe
- vprašanje
- IT
- ITS
- james
- jpg
- samo
- Ključne
- pozneje
- Led
- manj
- Stopnja
- kot
- Jetra
- več
- Mainstream
- več
- max širine
- Povečajte
- pomeni
- Medtem
- srečanja
- milijonov
- mesec
- več
- Najbolj
- veliko
- multidisciplinarno
- narodov
- Nimate
- potrebna
- mreža
- Novo
- NY
- novice
- NZS
- št
- normalno
- opozoriti
- roman
- zdaj
- Številka
- negovati
- of
- off
- ponudba
- on
- ONE
- v teku
- samo
- odprite
- odprt
- o odprtju
- operativno
- Priložnosti
- Priložnost
- Možnost
- or
- Ostalo
- rezultatov
- zunaj
- več
- paradigma
- paradigme
- del
- Terapija z delci
- pot
- poti
- Bolnik
- bolniki
- Prilagojene
- perspektiva
- faza
- Philadelphia
- Fotoni
- Fizika
- Svet fizike
- slika
- pionirji
- plinovod
- ključno
- platon
- Platonova podatkovna inteligenca
- PlatoData
- igral
- Veliko
- Točka
- naseljeno
- potencial
- praksa
- pragmatično
- Precision
- postopek
- Učitelj
- Učni načrt
- Lastnosti
- protoni
- dokazovanje
- R & D
- Radioterapija
- Naključno
- Oceniti
- Cene
- pripravljen
- v realnem času
- Pred kratkim
- zmanjša
- Zmanjšana
- obravnavajo
- režimi
- sprostitev
- poročilo
- Poročila
- Raziskave
- raziskovalci
- vir
- Odgovor
- revolucijo
- Richard
- Pravica
- strog
- Robin
- vloga
- soba
- Sobe
- rutinsko
- s
- varno
- San
- San Diego
- pravijo,
- sheme
- Znanost
- Znanstveniki
- škot
- iskanju
- izbor
- Storitev
- Zasedanje
- več
- oblikovanje
- Šarma
- premik
- sijaj
- Kratke Hlače
- pokazale
- bistveno
- silvia
- Podoben
- saj
- sam
- So
- trdna
- Zvočniki
- porabljen
- Spotlight
- začel
- Status
- Stephen
- Še vedno
- stop
- strukture
- Študije
- PODSAHARSKA
- precejšen
- taka
- podpora
- kirurški
- sistem
- sistemi
- miza
- Bodite
- talent
- Pogovor
- ciljna
- ciljanje
- skupina
- Tehnologija
- Pogoji
- texas
- kot
- da
- O
- njihove
- Njih
- POTEM
- Tukaj.
- zato
- jih
- mislim
- ta
- tisti,
- tisoče
- skozi
- thumbnail
- čas
- krat
- do
- skupaj
- Rekel
- temo
- Touted
- Sledenje
- usmeritev
- Transform
- zdravljenje
- Zdravljenje
- tretmaji
- poskusi
- sprožijo
- Res
- resnično
- Obračalni
- zavoji
- pod
- razumeli
- univerza
- navzgor
- us
- uporabo
- potrjeno
- Proti
- zelo
- Poglej
- Obseg
- prostornine
- je
- Watch
- način..
- we
- Dobro
- Kaj
- kdaj
- kadar koli
- ki
- medtem
- z
- v
- besede
- potek dela
- svet
- bi
- še
- york
- Vi
- zefirnet