Stereotaktisk kroppsstrålningsterapi (SBRT) är en precisionsbehandling av cancer som ger färre strålningsfraktioner med högre doser än traditionell strålbehandling. SBRT kan ge utmärkt lokal tumörkontroll, men för vissa tumörplatser riskerar den att exponera närliggande organ-at-risk (OAR) för oacceptabla strålningsnivåer. Protonbaserad SBRT ger bättre OAR-sparande, men kräver fortfarande vissa behandlingsmarginaler som kan begränsa dess kliniska tillämpbarhet.
FLASH-strålbehandling, där strålning levereras med ultrahöga doshastigheter, skulle kunna möjliggöra ytterligare sparande av OAR. För att undersöka dess potential begav sig ett forskarteam upp kl Emory University utvecklar ett ramverk för att optimera protonterapileverans för att möta kraven från FLASH-strålbehandling.
De flesta moderna protonterapisystem kan uppnå FLASH-doshastigheter med hjälp av en högenergitransmissionsstråle som passerar genom patienten och avsätter dos genom hela dess väg. Detta tillvägagångssätt eliminerar emellertid den stora fördelen med protonterapi: dess förmåga att leverera dos i en utbredd Bragg-topp. För att förbättra överensstämmelse vid FLASH-doshastigheter, Ruirui Liu och kollegor föreslår att patientspecifika åsfilter skulle kunna ge en liknande dosfördelning som den för konventionell intensitetsmodulerad protonterapi (IMPT).
För FLASH-behandlingar, dos, dos-genomsnittlig doshastighet (DADR) och dos-medelvärd linjär energiöverföring (LETd) alla påverkar det biologiska svaret. Således utvecklade forskarna ett integrerat ramverk för fysisk optimering (IPO) som samtidigt optimerar dessa tre parametrar för att maximera OAR-sparande i en patients behandlingsplan. Ramverket, som beskrivs i International Journal of Radiation Oncology, Biology, Physics, använder IPO-IMPT objektivfunktionen för att tillhandahålla flera lösningar för design av patientspecifika åsfilter och protonfläckkartor.
Åsfiltren, som används i kombination med en räckviddskompensator, består av en rad zigguratformade stift som sprider Bragg-toppen från en 250 MeV-stråle för att täcka en strålspecifik planeringsvolym. Teamet utvecklade omvänd planeringsprogramvara för att definiera stiftplatserna för ett patientspecifikt filter, och använde Geant4-baserade Monte Carlo-simuleringar för att tillhandahålla dos- och LET-påverkansmatriser.

Patientplaner
För att demonstrera IPO-IMPT-ramverket utvecklade forskarna behandlingsplaner för tre patienter med lungcancer. De ordinerade en dos på 50 Gy (fem 10 Gy-fraktioner) till den kliniska målvolymen, med en maximal hotspot-dos på 62.5 Gy. Beroende på vilken parameter som prioriteras syftar planerna till att öka FLASH-täckningen och/eller minska LETdsamtidigt som måldosen bibehålls.
För patient 1, som hade en central lungtumör nära hjärtat, var OAR:s hjärtat och lungan. För det här fallet genererade forskarna en enkelstråle IPO-IMPT-plan med syfte att minska LETd till hjärtat samtidigt som måltäckningen bibehålls. IPO-IMPT-planen uppfyllde detta mål, uppvisade liknande måltäckning som en konventionell IMPT-plan men minskade markant LETd till hjärtat.
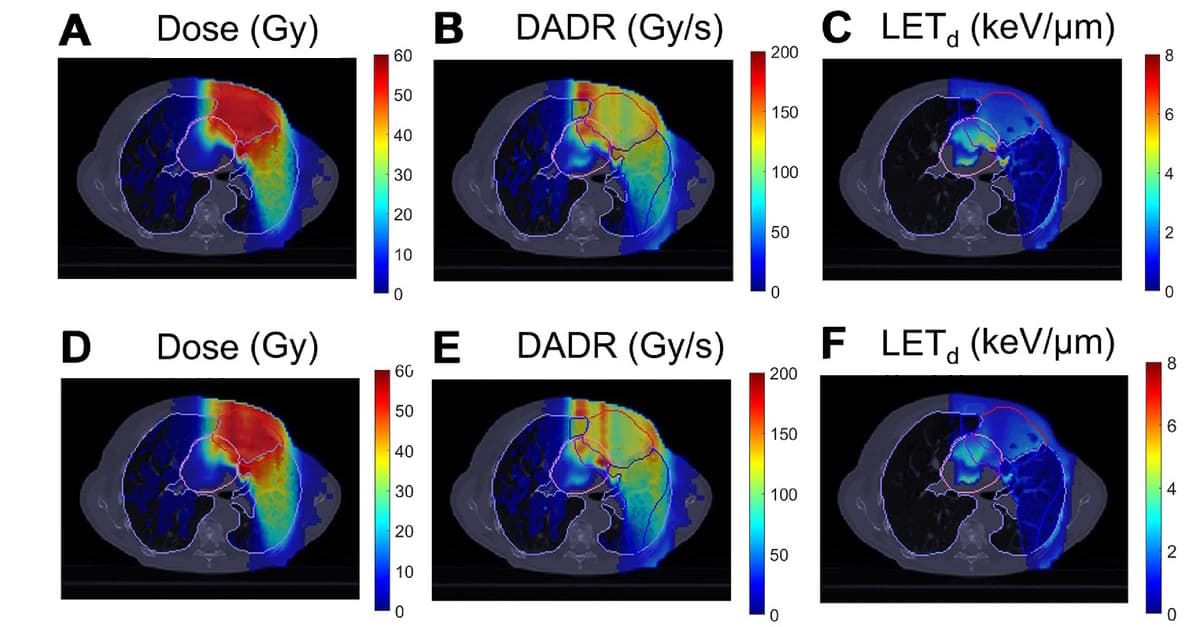
Patient 2 hade en metastaserande tumör i höger nedre lob och patient 3 hade en tumör i den subkarinala lymfkörteln. I dessa fall var matstrupen också en OAR och huvudmålet var matstrupssparande. För både IPO-IMPT och IMPT uppfyllde nästan 100 % av matstrupsutvärderingsvolymen 40 Gy/s FLASH-tröskeln. För patient 2 minskade IPO-IMPT något LETd för hjärtat och matstrupen och ökad FLASH-täckning för hjärtat.
Gles stiftdesign
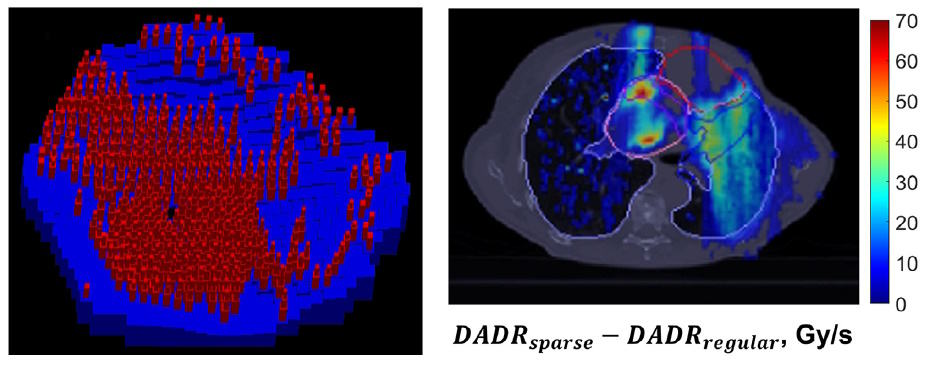
Vanliga åsfilter designade med IPO-IMPT-ramverket sparade selektivt OARs genom att minska LET och öka FLASH-täckningen. Men glesa åsfilter, från vilka vissa stift har utelämnats, erbjuder potential att ytterligare öka OAR-sparandet. Att ta bort filterstift på specifika platser ger ett högre protonflöde, medan de återstående stiften fortfarande ger tillräcklig måltäckning.
För patient 1 genererade forskarna en IPO-IMPT-plan med glesa åsfilter och flera strålar. Jämförelse med en IMPT-plan med vanliga åsfilter visade att tumörtäckningen för båda bibehölls och hotspots var väl kontrollerade. De glesa åsfiltren ökade emellertid OAR-volymen och fick en FLASH-doshastighet med 31 % och 50 % för hjärt- respektive lungutvärderingsvolymer.
De glesa åsfiltren ger flexibilitet för att realisera den fulla potentialen hos IPO-IMPT-ramverket. Till exempel kan nivåerna för borttagning av stift skräddarsys för individuella patientfall. En tröskel på 50 % för borttagning av stift gav rimliga resultat för patient 1:s stora tumör, medan en tröskel på 30 % var en bra utgångspunkt för de mindre målen för patienter 2 och 3, vars glesa åsfilterbaserade planer ökade DADR i matstrupen samtidigt som tumören bibehölls rapportering.
Slutligen, för att verifiera att en åsfilterenhet (filterstift och en kompensator) kunde leverera den förutsedda dosen, skrev forskarna 3D ut ett patientspecifikt åsfilter. De levererade en behandlingsplan utformad för att ge en enhetlig måldos och utförde dosmätningar med en joniseringskammaruppsättning. Den totala gamma-genomgångshastigheten var 92.9 % för absoluta doser, vilket överstiger standardpatients godkäntkriterier på 90 % och visar att aggregatet kan ge en kliniskt acceptabel dosfördelning.

NPL introducerar absolut dosimetri för FLASH protonstrålar
"Denna proof-of-concept-studie visar möjligheten att använda ett IPO-IMPT-ramverk för att åstadkomma FLASH stereotaktisk kroppsprotonterapi, med hänsyn till dos, DADR och LETd samtidigt”, avslutar forskarna. "Denna nya metod kommer att underlätta leverans av konforma protonfält till FLASH-hastigheter för prekliniska och kliniska studier."
Senior författare Liyong Lin berättar Fysikvärlden att teamet hoppas kunna vidareutveckla sin mjukvara för sådana applikationer. "Emorys Office of Technology Transfer uppmuntrade oss att bilda ett nystartat företag, Radiotherapy Biological Optimization (RBO) Solutions", förklarar Lin. "RBO har godkänts av National Institutes of Health's Applicant Assistance Program för att lämna in ett R41-bidrag för tekniköverföring för småföretag till National Cancer Institute senast den 5 april. IBA, den största leverantören av partikelterapi, och IBA:s dosimetriavdelning kommer att stödja RBO:s R41-bidragsförslag. ”
- SEO-drivet innehåll och PR-distribution. Bli förstärkt idag.
- Platoblockchain. Web3 Metaverse Intelligence. Kunskap förstärkt. Tillgång här.
- Källa: https://physicsworld.com/a/patient-specific-ridge-filters-enable-conformal-flash-proton-therapy/
- :är
- $UPP
- 1
- 10
- 2023
- 3d
- a
- förmåga
- Absolut
- godtagbart
- åstadkomma
- Redovisning
- Uppnå
- Fördel
- Alla
- och
- tillämpningar
- tillvägagångssätt
- April
- ÄR
- array
- Montage
- Bistånd
- At
- Författaren
- BE
- Stråle
- Bättre
- mellan
- störst
- biologi
- kropp
- företag
- by
- KAN
- Cancer
- Cancerbehandling
- Vid
- fall
- centrala
- Klimatkammare
- Charles
- Barn
- klick
- Klinisk
- Stäng
- kollegor
- kombination
- företag
- jämförelse
- avslutar
- kontroll
- kontrolleras
- konventionell
- kunde
- täcka
- täckning
- kriterier
- leverera
- levereras
- levererar
- leverans
- krav
- demonstrera
- demonstrerar
- beroende
- beskriven
- Designa
- utformade
- utveckla
- utvecklade
- utveckla
- Skillnaden
- fördelning
- Distributioner
- division
- eliminerar
- möjliggöra
- uppmuntras
- stödja
- energi
- utvärdering
- exempel
- överstiger
- utmärkt
- uppvisar
- Förklarar
- främja
- Fält
- filtrera
- filter
- Blixt
- Flexibilitet
- FLÖDE
- För
- formen
- Ramverk
- från
- full
- fungera
- ytterligare
- genereras
- Målet
- god
- bevilja
- headed
- Hjärta
- högre
- innehav
- hoppas
- hotspot
- Men
- html
- HTTPS
- bild
- förbättra
- BESKATTA
- in
- Öka
- ökat
- ökande
- individuellt
- påverka
- informationen
- Institute
- integrerade
- Introducerar
- undersöka
- IPO
- fråga
- IT
- DESS
- tidskriften
- jpg
- Nyckel
- Large
- nivåer
- BEGRÄNSA
- lokal
- platser
- upprätthålla
- större
- kartor
- marginaler
- max-bredd
- Maximera
- maximal
- mätningar
- Möt
- metod
- Modern Konst
- multipel
- nationell
- nod
- roman
- mål
- of
- erbjudanden
- Office
- on
- öppet
- optimering
- optimerar
- optimera
- parameter
- parametrar
- Partikelterapi
- passerar
- Förbi
- bana
- Patienten
- patienter
- Topp
- fysisk
- tall
- Planen
- planering
- planer
- plato
- Platon Data Intelligence
- PlatonData
- Punkt
- potentiell
- Precision
- förutsagda
- prioriteras
- Program
- förslag
- föreslå
- protoner
- ge
- förutsatt
- ger
- strålbehandling
- område
- Betygsätta
- rates
- inser
- rimlig
- mottagande
- minska
- reducerande
- regelbunden
- Återstående
- avlägsnande
- bort
- Kräver
- forskning
- forskare
- respons
- Resultat
- risker
- s
- liknande
- samtidigt
- Small
- Small Business
- mindre
- Mjukvara
- Lösningar
- några
- specifik
- Spot
- spridning
- standard
- Starta
- start
- Fortfarande
- studier
- Läsa på
- skicka
- sådana
- System
- skräddarsydd
- Målet
- mål
- grupp
- Teknologi
- berättar
- den där
- Smakämnen
- Dessa
- tre
- tröskelvärde
- Genom
- hela
- miniatyr
- till
- Totalt
- traditionell
- överföring
- behandling
- sann
- us
- leverantör
- verifiera
- volym
- volymer
- VÄL
- som
- medan
- VEM
- kommer
- med
- zephyrnet