Partikelterapi – cancerbehandling med hjälp av strålar av protoner eller tyngre joner – ger mycket konform dostillförsel och större sparande av normala vävnader än konventionell fotonbaserad strålbehandling. Men för långtidsöverlevande cancer är risken för strålningsinducerad sekundär cancer (SC) viktig och bör övervägas när man väljer sin behandlingsmodalitet.
Med epidemiologiska data knappa för nyare behandlingar som proton- och koljonterapi ledde ett team upp på GSI Helmholtz Center for Heavy Ion Research håller på att utveckla en modell för att jämföra SC-riskerna mellan partikelterapimodaliteter. Modellen, beskriven av Antonia Hufnagl och kollegor i Medicinsk fysik, skulle slutligen kunna införlivas i dosplaneringssystem för att inkludera SC-risk som ett ytterligare optimeringskriterium.
Dödliga kontra cancerframkallande händelser
SC riskmodeller fungerar vanligtvis genom att överväga balansen mellan celldöd (som leder till cancerdämpning) och celltransformation (induktion av mutationer som så småningom leder till cancer). Sannolikheten att en bestrålad volym kommer att utveckla cancer definieras med hjälp av den linjär-kvadratiska (LQ) modellen, som ger ett enkelt samband mellan cellöverlevnad och levererad fotondos.
I denna studie använde forskarna den lokala effektmodellen (LEM) för att förutsäga den relativa biologiska effektiviteten (RBE) av SC-induktion efter partikelterapi. För att ta hänsyn till den ökade RBE av partikelstrålning, ersatte de foton-LQ-parametrarna i riskmodellen med jonstråle-LQ-parametrarna som förutspåddes av LEM. En nyckelfunktion i deras tillvägagångssätt är användningen av LEM i både celldödande och cancerframkallande termer.

"Den dubbla användningen av LEM speglar konkurrensen mellan de två stora processerna som bestämmer SC-utveckling, nämligen celltransformation och celldöd", förklarar senior författare Michael Scholz. "Med ökande dos och/eller effektivitet kan celldöd undertrycka viabiliteten hos transformerade celler. Detta leder till ett komplext samspel, som inte helt enkelt kan återspeglas i ett enstegsprocedur.”
För att undersöka vilka faktorer som påverkar SC-risken använde forskarna planeringssystemet TPS TRiP98 för att generera biologiskt optimerade koljon- och protonbehandlingsplaner baserade på en idealiserad geometri. Planerna bestrålade ett 4x4x4 cm mål med en enda partikelstråle eller två motsatta strålar, med ett 4x4x1 cm organ-at-risk (OAR) framför målet. På grund av osäkerheter i foton-LQ-parametrarna som används som indata för LEM, uppskattade de proton-till-koljonriskförhållanden snarare än individuella riskvärden.
För dessa idealiserade uppställningar visade modellen inte en tydlig preferens för vare sig protoner eller koljoner, men avslöjade ett komplext beroende av olika parametrar. Den minskade laterala spridningen av koljoner leder till en lägre SC-risk än protoner i ingångskanalen. Men koljoner avsätter en högre dos bakom målet på grund av fragmenteringssvansen, vilket ökar SC-risken för OAR bakom tumören efter koljonbestrålning.
För enkelstråleplaner var den totala SC-risken ungefär 1.5 gånger högre för koljoner än för protoner. Med två motstående strålar var den totala SC-risken 1.16 gånger högre för protoner, även om denna varierade kraftigt beroende på den rumsliga platsen för den antagna känsliga volymen med avseende på målvolymen.
Vävnadsstrålningskänslighet (mot fotoner) hade en stor inverkan på SC-riskförhållandet, med radioresistenta OARs som gynnades av koljonbehandling och känsliga OAR från protonstrålar. Däremot hade fraktioneringsschemat liten inverkan på förväntade riskvärden.
Patientgeometri
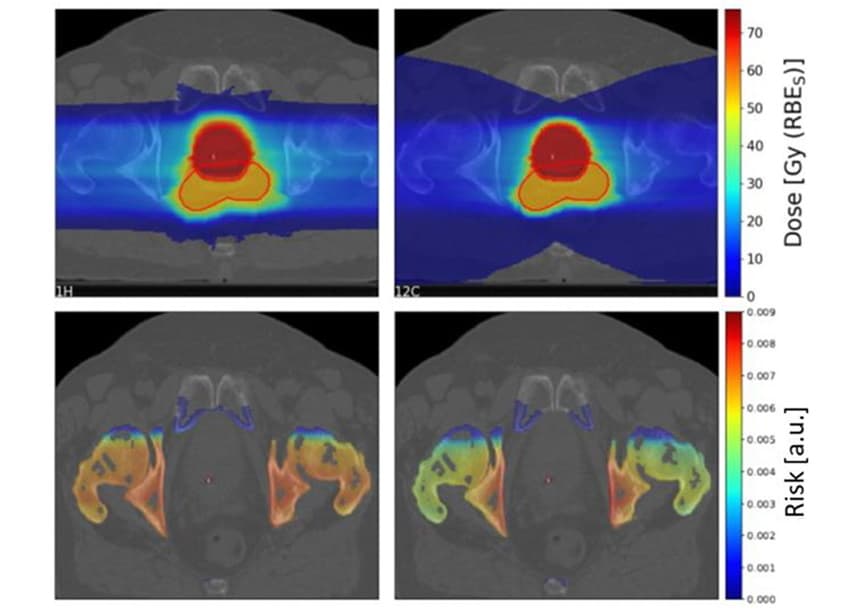
För att undersöka kliniska scenarier uppskattade Scholz och kollegor SC-riskerna för 10 prostatacancerpatienter som tidigare behandlats med fotonstrålbehandling vid Karolinska Universitetssjukhuset. De genererade behandlingsplaner för patienterna med hjälp av två lateralt motsatta skannade proton- och koljonfält.
Som sett tidigare resulterade fragmenteringssvansen av koljoner i ett stort lågdosområde bakom målet. Emellertid var högdosmålregionen mer konform för koljonen än protonplanerna.
Teamet beräknade proton-till-koljon SC riskförhållanden för fyra OARs (blåsa, ändtarm, ben och hud) för de 10 patienterna. För ben och hud gav protonplaner en något högre SC-risk än koljonplaner, med medianriskkvoter på 1.19 respektive 1.06 för ben och hud. För urinblåsa och ändtarm resulterade dock protonplaner i signifikant lägre SC-risker, med riskkvoter på 0.68 respektive 0.49 för urinblåsa och ändtarm.
Forskarna drar slutsatsen att de insikter som denna modell får kan hjälpa till att optimera framtida behandlingar. För närvarande är relativ riskmodellering främst lämplig som ett verktyg för att jämföra olika behandlingsscenarier för olika patientkohorter. Men Scholz noterar att det skulle vara enkelt att införliva sådana modeller i behandlingsplanering för enskilda patienter.

Koljonnätterapi skonar frisk vävnad
"Det kräver bara att planera för en given dosfördelning med två olika biologiska parameteruppsättningar som representerar celldöden respektive celltransformationsprocessen", förklarar han. "Då behövs bara viss efterbearbetning av de resulterande 3D-effektfördelningarna med matematiska standardverktyg för att härleda motsvarande riskkvotsfördelningar."
Nästa steg, säger han, är att validera modellen via jämförelse med kliniska data. "Eftersom dessa data för närvarande är knappa, skulle en utvidgning av tillvägagångssättet till att även inkludera fotonbehandlingar och bestämma motsvarande riskförhållanden för protoner kontra fotoner och koljoner mot fotoner vara ett viktigt nästa steg," säger Scholz Fysikvärlden.