Глибока стимуляція мозку (DBS), при якій електроди, імплантовані в мозок, подають електричні імпульси до певних цілей, є ефективним клінічним методом лікування кількох неврологічних станів. Зараз DBS використовується для лікування рухових розладів, таких як хвороба Паркінсона, есенціальний тремор і дистонія, а також таких станів, як епілепсія та обсесивно-компульсивний розлад. Однак лікування вимагає хірургічного втручання на головному мозку для введення стимуляційних електродів, що може спричинити численні побічні ефекти.
Щоб усунути потребу в інвазивній хірургії, дослідники з Університету науки і технологій Похан (ПОСТЕЧ) у Кореї розробляють стратегію неінвазивної нейростимуляції на основі п’єзоелектричних наночастинок. Наночастинки виконують дві функції – тимчасове відкриття гематоенцефалічного бар’єру (ГЕБ) і стимулювання вивільнення дофаміну – обидві контролюються зовнішнім сфокусованим ультразвуком.
П’єзоелектричні наночастинки представляють інтерес як нервові стимулятори, оскільки у відповідь на зовнішні подразники, такі як ультразвук, наприклад, вони деформуються та видають постійний струм. Дослідники припускають, що цей струм можна використовувати для стимулювання дофамінергічних нейронів до вивільнення нейромедіаторів.
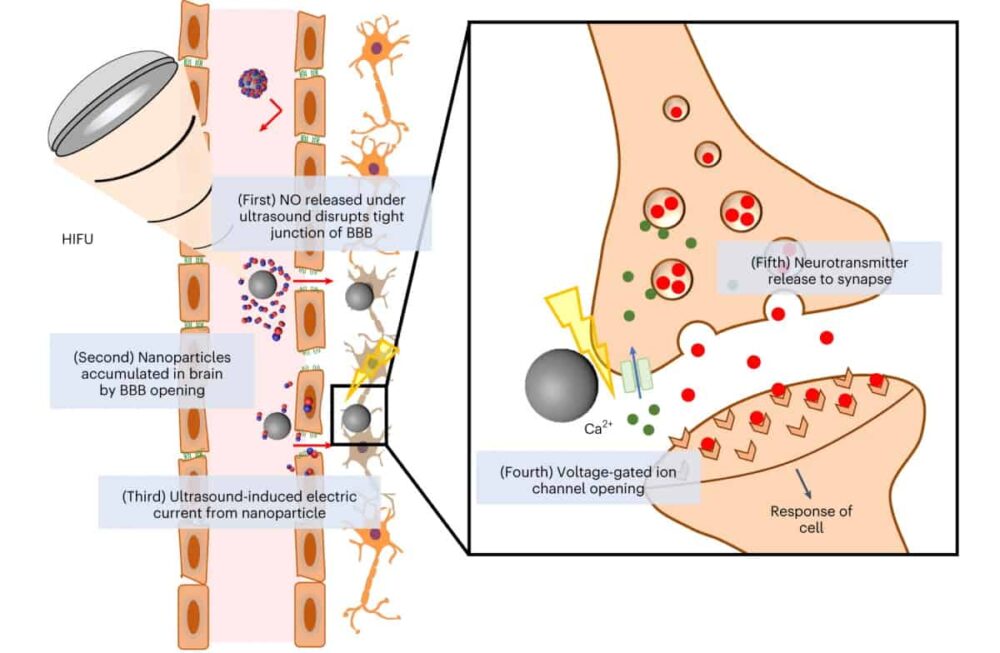
Однією з ключових проблем є доставка наночастинок до мозку, зокрема, як перенести їх через ГЕБ. Щоб досягти цього, дослідники звернулися до оксиду азоту (NO), високоактивної молекули, яка демонструє потенціал для руйнування BBB. Вони сконструювали багатофункціональну систему, описану в Природа Біомедична інженерія, що містить наночастинки титанату барію, вкриті BNN6, що вивільняє NO, і полідофаміном (pDA). У відповідь на ультразвук ці наночастинки повинні генерувати як NO, так і постійний струм.
Щоб перевірити їхній підхід, провідний автор Вон Чон Кім і його колеги вперше дослідили здатність наночастинок вивільняти NO. У відповідь на 5 с високоінтенсивного сфокусованого ультразвуку (HIFU) наночастинки миттєво виділяли NO. Вони також оцінили п’єзоелектричну поведінку, використовуючи установку патч-затискач. У той час як розчинник без наночастинок, покритих pDA, не демонстрував стрибків струму, у присутності наночастинок спостерігалися помітні стрибки струму з інтенсивністю, пропорційною інтенсивності ультразвуку.
Вважається, що DBS електрично стимулює нервову систему шляхом відкриття Ca2+ канали найближчих нейронів, а потім прискорення вивільнення нейромедіатора в синапсі. Щоб дослідити, чи може струм, що генерується наночастинками, забезпечувати аналогічну нервову стимуляцію, команда відстежувала Ca2+ динаміка нейроноподібних клітин. Внутрішньоклітинний Са2+ концентрація значно зросла в клітинах, які отримували як наночастинки, так і ультразвук, тоді як ні ультразвук, ні наночастинки самі по собі не мали ніякого ефекту.
Клітини, оброблені стимульованими ультразвуком наночастинками, також генерували підвищену позаклітинну концентрацію дофаміну, що вказує на Ca2+ опосередковане припливом вивільнення нейромедіатора. Знову ж таки, жодних суттєвих змін не було помічено ні з ультразвуком, ні з наночастинками. Тести з використанням неп'єзоелектричних наночастинок показали незначні зміни Ca2+ припливу та вивільнення нейромедіаторів, що вказує на те, що ці ефекти виникають переважно у відповідь на п’єзоелектричну стимуляцію.
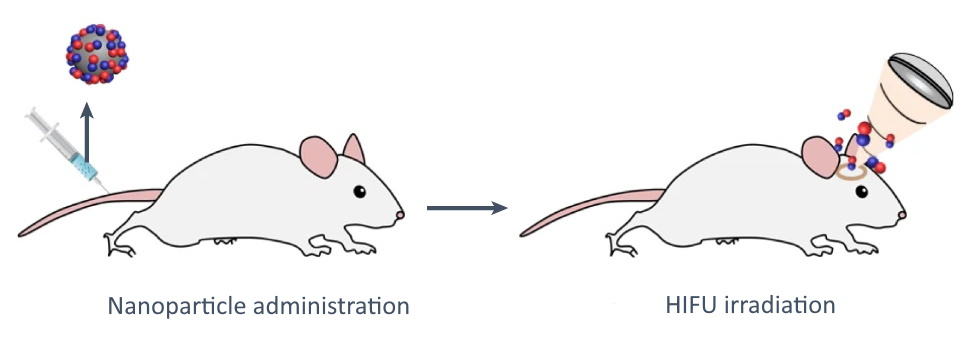
Потім дослідники виконали серію в природних умовах навчання. Щоб дослідити опосередковане NO відкриття BBB, вони внутрішньовенно ввели мишам п’єзоелектричні наночастинки, що вивільняють NO, а потім застосували HIFU до цільових ділянок мозку під ультразвуковим контролем.
Через дві години після ін’єкції трансмісійна електронна мікроскопія виявила значно більшу кількість наночастинок, накопичених у мозку тварин, порівняно з контрольними групами, демонструючи, що вивільнення NO тимчасово порушило щільні з’єднання в ГЕБ. Дослідники також показали, що через 2 години після застосування HIFU ГЕБ більше не був проникним, підтверджуючи, що опосередковане NO порушення ГЕБ є лише тимчасовим.
Нарешті, команда оцінила терапевтичні ефекти наночастинок за допомогою мишачої моделі хвороби Паркінсона. Мишам вводили наночастинки з подальшим множинним застосуванням HIFU в субталамічному ядрі (місце націлювання DBS, схвалене Управлінням з харчових продуктів і медикаментів США) для відновлення рівня дофаміну в мозку.
DBS з використанням ультразвукових наночастинок покращив поведінкові функції тварин, включаючи рухову координацію та рухову активність. У мишей спостерігалося поступове поліпшення рухової функції при щоденній стимуляції HIFU протягом 10 днів, причому рухова активність майже відновилася на 16 день. Команда припускає, що п’єзоелектричні наночастинки індукують вивільнення нейромедіаторів, що значно полегшує симптоми хвороби Паркінсона, не викликаючи значної токсичності. .

Персоналізована стимуляція мозку може лікувати невиліковну депресію
«Ми сподіваємося, що п’єзоелектричні наночастинки, що реагують на ультразвук, що вивільняють NO, можна буде розвинути в мінімально інвазивні терапевтичні підходи для лікування нейродегенеративних захворювань», – підсумовують вони.
Зараз група проводить фундаментальні дослідження, щоб визначити основні механізми відкриття ГЕБ, опосередкованого NO. «Ми також розробляємо NO-модулюючі матеріали нового покоління, щоб максимізувати їх клінічне використання, а також мінімізувати їхні небажані побічні ефекти», — пояснює перший автор Теджонг Кім.