وائرس کے اندر موجود جینیاتی مواد پروٹین کی حفاظتی کوٹنگ کے بغیر زیادہ دیر تک زندہ نہیں رہ سکتا۔ تاہم، وہ عمل جس کے ذریعے یہ پروٹین وائرل جینوم کو سمیٹنے کے لیے جمع ہوتے ہیں (اور اس وجہ سے حفاظت کرتے ہیں) - خاص طور پر کورونا وائرس کے لیے، جن میں بہت بڑے RNA جینوم ہوتے ہیں۔ ریور سائیڈ، یو ایس کی یونیورسٹی آف کیلیفورنیا اور چین میں سونگشن لیک میٹریلز لیبارٹری کے محققین کے ایک جوڑے نے اب SARS-CoV-2، کورونا وائرس جو COVID-19 کا سبب بنتا ہے کی اسمبلی کے دوران ہونے والے تعاملات کی نشاندہی کی ہے، اور یہ دریافت کیا ہے کہ یہ تعامل کیسے ہوتے ہیں۔ جینوم کو ایک نئے وائرس میں پیک کرنے کا باعث بنتا ہے۔ یہ کام اس اور دیگر کورونا وائرس سے لڑنے کے لیے دوائیوں کے ڈیزائن اور ترقی میں مدد دے سکتا ہے۔
SARS-CoV-2 میں چار ساختی پروٹین ہوتے ہیں: لفافہ (E)؛ جھلی (ایم)؛ nucleocapsid (N)؛ اور سپائیک (S) ایم، ای اور ایس پروٹین وائرس کی سب سے بیرونی تہہ، یا لفافے کو جمع کرنے اور بنانے کے لیے بہت ضروری ہیں، جو وائرس کو میزبان خلیوں میں داخل ہونے کے ساتھ ساتھ اسے نقصان سے بچانے میں مدد کرتا ہے۔
کمپیکٹ رائبونیوکلیوپروٹین کمپلیکس
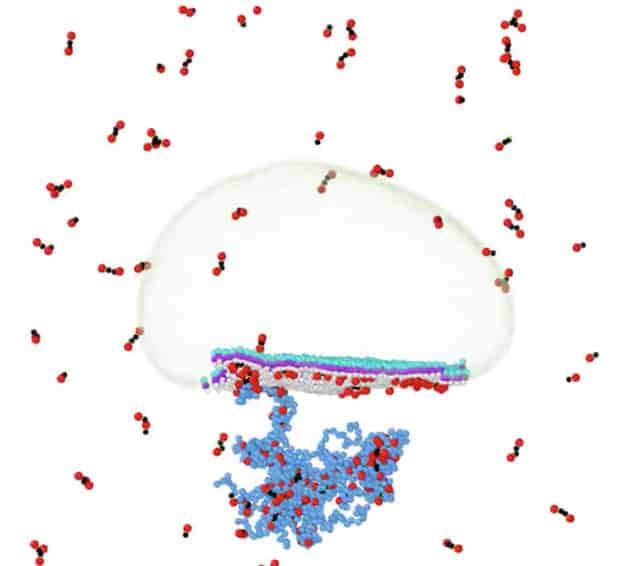
نئے کام میں، UC-Riverside ماہر طبیعیات رویا زندی اور اس کا سابق گریجویٹ طالب علم سیو لی (جو اب سونگھن جھیل میں پوسٹ ڈاک ہے) نے کمپیوٹیشنل ٹولز کا استعمال کیا جسے موٹے دانے والے ماڈل کہا جاتا ہے تاکہ ان اجزاء سے SARS-CoV-2 کیسے بنتا ہے۔ یہ ماڈل وائرل اجزاء کی لمبائی کے بڑے پیمانے پر نقل کرتے ہیں اور وائرس اسمبلی کے عمل کے بارے میں قیمتی معلومات فراہم کرتے ہیں۔
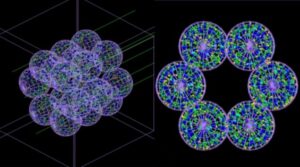
ان ماڈلز کا استعمال کرتے ہوئے، جوڑی نے حساب لگایا کہ N پروٹین وائرل RNA کو گاڑھا کر کے ایک نام نہاد کمپیکٹ رائبونیوکلیوپروٹین کمپلیکس بناتے ہیں، جو کہ پروٹین اور RNA دونوں پر مشتمل مالیکیولز کی اسمبلی ہے۔ یہ اسمبلی پھر لپڈ جھلی میں سرایت شدہ ایم پروٹین کے ساتھ تعامل کرتی ہے۔ آخر میں، ایک عمل ہوتا ہے جسے رائبونیوکلیوپروٹین کمپلیکس کا "ابڈنگ" کہا جاتا ہے، وائرل کی تشکیل کو مکمل کرتا ہے۔
N پروٹین کے درمیان تعامل بہت اہم ہے۔
محققین نے اپنے ماڈل میں N پروٹین کی شکل کو ادب میں بیان کردہ ایک معروف ساخت پر مبنی بنایا۔ "RNA ایک منفی چارج شدہ پولیمر ہے اور N پروٹین میں بہت سارے مثبت چارجز ہوتے ہیں،" زندی بتاتے ہیں۔ "N پروٹین پر مثبت چارجز اور RNA پر منفی چارجز کے درمیان تعامل کا نتیجہ RNA کی گاڑھا ہونے میں ہے۔"
زندی بتاتی ہے۔ طبیعیات کی دنیا کہ N پروٹین کے درمیان تعامل آر این اے گاڑھاو میں بہت اہم نکلے۔ وہ مزید کہتی ہیں، "ہمیں اس اثر کے بارے میں اپنی نقلیں کرنے سے پہلے معلوم نہیں تھا۔
اس جوڑے نے M پروٹین کو ان کی ساخت اور فنکشن کی بنیاد پر بھی ماڈل بنایا جیسا کہ ادب میں بیان کیا گیا ہے۔ انہوں نے ان پروٹینوں کو اس طرح ڈیزائن کیا کہ وہ N پروٹین کے ساتھ تعامل کرتے ہیں اور جھلی کو بھی موڑ دیتے ہیں۔ "موٹے دانے والے ماڈل نے ہمیں پروٹین اولیگومرائزیشن کے طریقہ کار کو سمجھنے کی اجازت دی ہے، ساختی پروٹین کے ذریعے آر این اے گاڑھا ہونا اور جھلی-پروٹین کے تعاملات، ان عوامل کی پیشین گوئی کرتے ہیں جو وائرس کو کنٹرول کرتے ہیں،" لی بتاتے ہیں۔

سپر ریزولوشن مائیکروسکوپی کورونا وائرس کی نقل تیار کرنے والی مشینری کو ظاہر کرتی ہے۔
ماضی میں، زندی نے نوٹ کیا کہ ان عوامل کو سمجھنا جو وائرس کی اسمبلی میں کردار ادا کرتے ہیں اکثر نئی علاج کی حکمت عملیوں کا باعث بنتے ہیں۔ ان کے خیال میں اس تحقیق سے حاصل ہونے والے نتائج، جس کی تفصیل جریدے میں ہے۔ وائرس، اسی طرح SARS-CoV-2 کا مقابلہ کرنے کے ذرائع فراہم کرنے میں مدد کرسکتا ہے۔ وہ کہتی ہیں، "ہم نے جس اسمبلی میکانزم کا پتہ لگایا ہے وہ چھوٹے مالیکیولز کے ڈیزائن اور نشوونما کو مطلع کر سکتا ہے جو وائرل ڈھانچے کے پروٹین کو نشانہ بناتے ہیں، اور ان کے افعال میں ترمیم کرتے ہوئے اسمبلی کے عمل کی وفاداری کو متاثر کرتے ہیں۔"
طویل مدتی میں، زندی کے خیال میں نیا کام تجربات اور خوردبینی تمام ایٹم تخروپن کے لیے بھی ایک معیار بن سکتا ہے۔ "ہم فی الحال اپنی تحقیقات کے اگلے مرحلے کے لیے تجرباتی اور کمپیوٹیشنل گروپس کے ساتھ تعاون کر رہے ہیں،" وہ بتاتی ہیں۔ "بالآخر، ہمارا مقصد اینٹی وائرل ادویات کی مسلسل ترقی کے لیے کثیر پیمانے پر تحقیق کو مربوط کرنا ہے تاکہ کورونا وائرس کو ان کے اسمبلی مرحلے میں گرفتار کیا جا سکے۔"