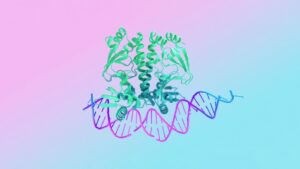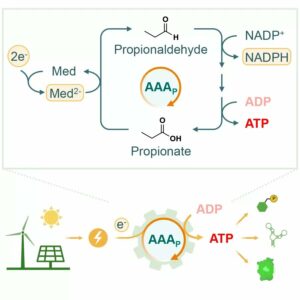
Protein thường được gọi là khối xây dựng của sự sống.
Mặc dù đúng, phép loại suy gợi lên hình ảnh các mảnh giống như Lego ghép lại với nhau để tạo thành các khối phức tạp nhưng cứng nhắc kết hợp thành cơ và các mô khác. Trên thực tế, các protein giống như các loài cỏ lăn linh hoạt hơn—cấu trúc cực kỳ tinh vi với “gai” và các nhánh nhô ra từ một khung trung tâm—biến hình và thay đổi theo môi trường của chúng.
Sự thay đổi hình dạng này kiểm soát các quá trình sinh học của các sinh vật sống—ví dụ: mở các đường hầm protein nằm rải rác dọc theo các tế bào thần kinh hoặc thúc đẩy sự phát triển của ung thư. Nhưng nó cũng làm cho việc hiểu hành vi của protein và phát triển các loại thuốc tương tác với protein trở thành một thách thức.
Trong khi gần đây Đột phá về AI trong dự đoán (và thế hệ chẵn) của cấu trúc protein là một tiến bộ vượt bậc trong 50 năm hình thành, chúng vẫn chỉ cung cấp ảnh chụp nhanh của protein. Để nắm bắt toàn bộ quá trình sinh học—và xác định nguyên nhân dẫn đến bệnh tật—chúng ta cần dự đoán cấu trúc protein ở nhiều “tư thế” và quan trọng hơn là cách mỗi tư thế này thay đổi các chức năng bên trong của tế bào. Và nếu chúng ta dựa vào AI để giải quyết thách thức, chúng ta cần nhiều dữ liệu hơn.
Nhờ bản đồ protein mới được xuất bản trong tháng này trong Thiên nhiên, bây giờ chúng ta có một khởi đầu tuyệt vời.
Là sự hợp tác giữa MIT, Trường Y Harvard, Trường Y Yale và Đại học Y Weill Cornell, nghiên cứu tập trung vào một sự thay đổi hóa học cụ thể trong protein—được gọi là sự phosphoryl hóa—được biết là hoạt động như một công tắc bật-tắt protein và trong nhiều trường hợp , dẫn đến hoặc ức chế ung thư.
Tập bản đồ sẽ giúp các nhà khoa học tìm hiểu xem tín hiệu bị sai lệch như thế nào trong các khối u. Nhưng với Sean Humphrey và Elise Needham, các bác sĩ tại Bệnh viện Nhi đồng Hoàng gia và Đại học Cambridge, những người không tham gia vào công việc, tập bản đồ cũng có thể bắt đầu giúp biến những dự đoán tĩnh của AI về hình dạng protein thành những dự đoán trôi chảy hơn về cách thức hoạt động của protein trong cơ thể.
Hãy nói về PTM (Hả?)
Sau khi chúng được sản xuất, bề mặt của protein được “chấm” bằng các nhóm hóa chất nhỏ—giống như thêm lớp trên bề mặt vào một que kem. Những lớp phủ này tăng cường hoặc tắt hoạt động của protein. Trong các trường hợp khác, các phần của protein bị cắt nhỏ để kích hoạt nó. Các thẻ protein trong tế bào thần kinh thúc đẩy sự phát triển của não bộ; các thẻ khác cắm cờ đỏ trên các protein đã sẵn sàng để xử lý.
Tất cả những chỉnh sửa này được gọi là sửa đổi sau dịch mã (PTM).
PTM về cơ bản biến protein thành bộ vi xử lý sinh học. Chúng là một cách hiệu quả để tế bào điều chỉnh hoạt động bên trong của nó mà không cần thay đổi DNA hoặc cấu trúc biểu sinh. PTM thường thay đổi đáng kể cấu trúc và chức năng của protein, và trong một số trường hợp, chúng có thể góp phần gây ra bệnh Alzheimer, ung thư, đột quỵ và tiểu đường.
Đối với Elisa Fadda tại Đại học Maynooth ở Ireland và Jon Agirre tại Đại học York, đã đến lúc chúng tôi kết hợp PTM vào các công cụ dự đoán protein AI như AlphaFold. Trong khi AlphaFold đang thay đổi cách chúng ta thực hiện sinh học cấu trúc, chúng nói, “thuật toán không tính đến những sửa đổi thiết yếu ảnh hưởng đến cấu trúc và chức năng của protein, điều này chỉ cung cấp cho chúng ta một phần của bức tranh.”
Vua PTM
Vì vậy, trước tiên chúng ta nên kết hợp loại PTM nào vào AI?
Hãy để tôi giới thiệu với bạn về quá trình phosphoryl hóa. PTM này thêm một nhóm hóa học, phốt phát, vào các vị trí cụ thể trên protein. Humphrey và Needham cho biết đó là một “cơ chế điều tiết nền tảng cho cuộc sống”.
Các điểm nóng protein cho quá trình phosphoryl hóa đã được biết rõ: hai axit amin, serine và threonine. Khoảng 99 phần trăm của tất cả các vị trí phosphoryl hóa là do bộ đôi này và các nghiên cứu trước đây đã xác định được khoảng 100,000 điểm tiềm năng. Vấn đề là xác định những protein nào—được gọi là kinase, trong số đó có hàng trăm loại—thêm các nhóm hóa học vào các điểm nóng.
Trong nghiên cứu mới, lần đầu tiên nhóm nghiên cứu sàng lọc hơn 300 kinase chuyên bám lấy hơn 100 mục tiêu. Mỗi mục tiêu là một chuỗi axit amin ngắn chứa serine và threonine, “mắt bò” cho quá trình phosphoryl hóa và được bao quanh bởi các axit amin khác nhau. Mục đích là để xem mức độ hiệu quả của mỗi kinase trong công việc của nó ở mọi mục tiêu - gần giống như một trò chơi mai mối kinase.
Điều này cho phép nhóm tìm ra mô típ được ưa thích nhất—chuỗi axit amin—cho mỗi kinase. Humphrey và Needham cho biết: Đáng ngạc nhiên là “gần hai phần ba vị trí phosphoryl hóa có thể được chỉ định cho một trong số ít kinase”.
Một viên đá Rosetta
Dựa trên những phát hiện của họ, nhóm nghiên cứu đã nhóm các kinase thành 38 lớp dựa trên mô típ khác nhau, mỗi lớp có sự thèm ăn đối với một mục tiêu protein cụ thể. Về lý thuyết, các kinase có thể xúc tác cho hơn 90,000 vị trí phosphoryl hóa đã biết trong protein.
Yaffe cho biết: “Bản đồ mô típ kinase này giờ đây cho phép chúng tôi giải mã các mạng báo hiệu.
Trong một thử nghiệm chứng minh khái niệm, nhóm đã sử dụng tập bản đồ để tìm kiếm các tín hiệu tế bào khác nhau giữa tế bào khỏe mạnh và tế bào tiếp xúc với bức xạ. Thử nghiệm đã tìm thấy 37 mục tiêu phosphoryl hóa tiềm năng của một kinase duy nhất, hầu hết trong số đó chưa được biết đến trước đây.
Ok, vậy thì sao?
Phương pháp của nghiên cứu có thể được sử dụng để theo dõi các PTM khác để bắt đầu xây dựng một tập bản đồ toàn diện về các tín hiệu và mạng di động điều khiển các chức năng sinh học cơ bản của chúng ta.
Tập dữ liệu, khi được đưa vào AlphaFold, RoseTTAFold, các biến thể của chúng hoặc các thuật toán dự đoán cấu trúc protein mới nổi khác, có thể giúp họ dự đoán tốt hơn cách protein tự động thay đổi hình dạng và tương tác trong tế bào. Điều này sẽ hữu ích hơn nhiều cho việc khám phá thuốc so với ảnh chụp nhanh protein tĩnh ngày nay. Nhà khoa học cũng có thể sử dụng những công cụ như vậy để giải quyết “vũ trụ đen tối” kinase. Tập hợp con kinase này, hơn 100, không có mục tiêu protein rõ ràng. Nói cách khác, chúng tôi không biết làm thế nào những protein mạnh mẽ này hoạt động bên trong cơ thể.
Humphrey và Needham cho biết: “Khả năng này sẽ thúc đẩy các nhà nghiên cứu mạo hiểm 'đi vào bóng tối', để mô tả rõ hơn các protein khó nắm bắt này.
Nhóm nghiên cứu thừa nhận rằng còn một chặng đường dài phía trước, nhưng họ hy vọng tập bản đồ và phương pháp của họ có thể ảnh hưởng đến những người khác để xây dựng cơ sở dữ liệu mới. Cuối cùng, chúng tôi hy vọng “phương pháp tiếp cận dựa trên mô típ toàn diện của chúng tôi sẽ được trang bị độc đáo để làm sáng tỏ tín hiệu phức tạp làm cơ sở cho sự tiến triển của bệnh ở người, cơ chế kháng thuốc ung thư, can thiệp chế độ ăn uống và các quá trình sinh lý quan trọng khác,” họ nói.
Ảnh: Deepmind
- Phân phối nội dung và PR được hỗ trợ bởi SEO. Được khuếch đại ngay hôm nay.
- Platoblockchain. Web3 Metaverse Intelligence. Khuếch đại kiến thức. Truy cập Tại đây.
- nguồn: https://singularityhub.com/2023/01/18/the-next-step-for-ai-in-biology-is-to-predict-how-proteins-behave-in-the-body/
- 000
- 100
- 50 năm
- a
- Có khả năng
- Giới thiệu
- Tài khoản
- Hành động
- hoạt động
- Thêm
- tiến
- ảnh hưởng đến
- trước
- AI
- thuật toán
- thuật toán
- Tất cả
- Alzheimer
- và
- cảm giác ngon miệng
- phương pháp tiếp cận
- giao
- cơ bản
- Hơn
- giữa
- sinh học
- Khối
- thân hình
- Brain
- chi nhánh
- xây dựng
- Xây dựng
- gọi là
- cambridge
- Ung thư
- nắm bắt
- trường hợp
- Tế bào
- trung tâm
- thách thức
- thay đổi
- Những thay đổi
- thay đổi
- đặc trưng
- hóa chất
- các lớp học
- hợp tác
- Trường đại học
- kết hợp
- phức tạp
- toàn diện
- Góp phần
- điều khiển
- có thể
- tín dụng
- dữ liệu
- cơ sở dữ liệu
- Deepmind
- phát triển
- Phát triển
- Bệnh tiểu đường
- khác nhau
- khác nhau
- ĐÀO
- phát hiện
- Bệnh
- dna
- Các bác sĩ
- xuống
- đột ngột
- lái xe
- lái xe
- thuốc
- Thuốc
- mỗi
- Hiệu quả
- hiệu quả
- hay
- mới nổi
- Môi trường
- đã trang bị
- thiết yếu
- chủ yếu
- ví dụ
- tiếp xúc
- Fed
- Tìm kiếm
- Tên
- cờ
- linh hoạt
- tập trung
- hình thức
- tìm thấy
- từ
- chức năng
- chức năng
- cơ bản
- trò chơi
- được
- cho
- mục tiêu
- Đi
- lấy
- tuyệt vời
- Nhóm
- Các nhóm
- Tăng trưởng
- số ít
- harvard
- khỏe mạnh
- giúp đỡ
- Cao
- mong
- Độ đáng tin của
- HTTPS
- Nhân loại
- ICE
- kem
- ý tưởng
- xác định
- xác định
- xác định
- hình ảnh
- quan trọng
- in
- Mặt khác
- kết hợp
- Hợp nhất
- ảnh hưởng
- tương tác
- giới thiệu
- tham gia
- ireland
- IT
- Việc làm
- Vua
- nổi tiếng
- dẫn
- cho phép
- Cuộc sống
- sống
- . Các địa điểm
- dài
- LÀM CHO
- trang điểm
- sản xuất
- nhiều
- cơ chế
- y khoa
- y học
- phương pháp
- Phương pháp luận
- MIT
- Sửa đổi
- tháng
- chi tiết
- hầu hết
- nhiều
- Thiên nhiên
- Cần
- cần
- mạng
- Neurons
- Mới
- tiếp theo
- cung cấp
- ONE
- mở
- Nền tảng khác
- Khác
- một phần
- riêng
- các bộ phận
- phần trăm
- hình ảnh
- miếng
- plato
- Thông tin dữ liệu Plato
- PlatoDữ liệu
- đặt ra
- khả năng
- tiềm năng
- mạnh mẽ
- dự đoán
- dự đoán
- Dự đoán
- ưa thích
- trước
- trước đây
- Vấn đề
- Quy trình
- Protein
- Protein
- công bố
- sẵn sàng
- Thực tế
- gần đây
- đỏ
- Cờ đỏ
- Quy định
- nhà nghiên cứu
- Sức đề kháng
- cứng nhắc
- đường
- khoảng
- hoàng gia
- Nói
- Trường học
- Nhà khoa học
- các nhà khoa học
- Sean
- Hình dạng
- hình dạng
- ngắn
- nên
- tín hiệu
- duy nhất
- Các trang web
- nhỏ
- So
- động SOLVE
- một số
- tinh vi
- riêng
- đặc biệt
- Bắt đầu
- Bước
- Vẫn còn
- cấu trúc
- cấu trúc
- nghiên cứu
- Học tập
- như vậy
- bao quanh
- Công tắc điện
- Thảo luận
- Mục tiêu
- mục tiêu
- nhóm
- thử nghiệm
- Sản phẩm
- cung cấp their dịch
- thời gian
- đến
- hôm nay
- bên nhau
- công cụ
- theo dõi
- Chuyển đổi
- đúng
- XOAY
- hai phần ba
- sự hiểu biết
- Vũ trụ
- trường đại học
- đại học Cambridge
- us
- sử dụng
- liên doanh
- nổi tiếng
- Điều gì
- cái nào
- trong khi
- CHÚNG TÔI LÀ
- sẽ
- không có
- Công việc
- hoạt động
- sẽ
- năm
- Bạn
- zephyrnet