Phẫu thuật cắt bỏ mô ung thư là phương pháp điều trị phổ biến được sử dụng để giảm khả năng ung thư lan sang các mô khỏe mạnh. Tuy nhiên, hiệu quả của phẫu thuật như vậy phụ thuộc rất nhiều vào khả năng của bác sĩ phẫu thuật để phân biệt giữa mô ung thư và mô khỏe mạnh.
Được biết, các hoạt động trao đổi chất của mô ung thư và mô khỏe mạnh có sự khác biệt đáng kể: các mô ung thư thường có lưu lượng máu hỗn loạn kết hợp với lượng oxy thấp hoặc tình trạng thiếu oxy. Với các vùng thiếu oxy phổ biến trong mô ung thư, việc xác định chính xác tình trạng thiếu oxy có thể giúp phân biệt ung thư với mô khỏe mạnh trong quá trình phẫu thuật.
Các nhà nghiên cứu từ Trường Kỹ thuật Thayer tại Dartmouth và Đại học Wisconsin-Madison đang nghiên cứu việc sử dụng các đầu dò huỳnh quang để chụp ảnh thời gian thực nồng độ oxy cục bộ trong mô trong quá trình phẫu thuật. Họ trình bày những phát hiện của họ trong Tạp chí Quang học Y sinh.
Khi các đầu dò huỳnh quang bị kích thích bởi ánh sáng, chúng sẽ trở về trạng thái cơ bản và phát ra ánh sáng ở một năng lượng khác. Ngay khi được chiếu sáng, các đầu dò phát ra một xung ánh sáng quang học ngắn được gọi là huỳnh quang nhanh. Một số đầu dò cũng có thể tạo ra tín hiệu huỳnh quang bị trễ một thời gian sau khi chiếu sáng.
Mặc dù cả tín hiệu huỳnh quang nhanh và chậm đều phân rã theo thời gian, tín hiệu huỳnh quang tức thì phân rã nhanh chóng so với sự phân rã kéo dài của huỳnh quang bị trễ. Sự phân rã tín hiệu huỳnh quang bị trì hoãn có thể được quan sát và phân tích sâu hơn để hiểu rõ hơn về hoạt động trao đổi chất của mô lân cận.
Đánh giá oxy hóa thời gian thực
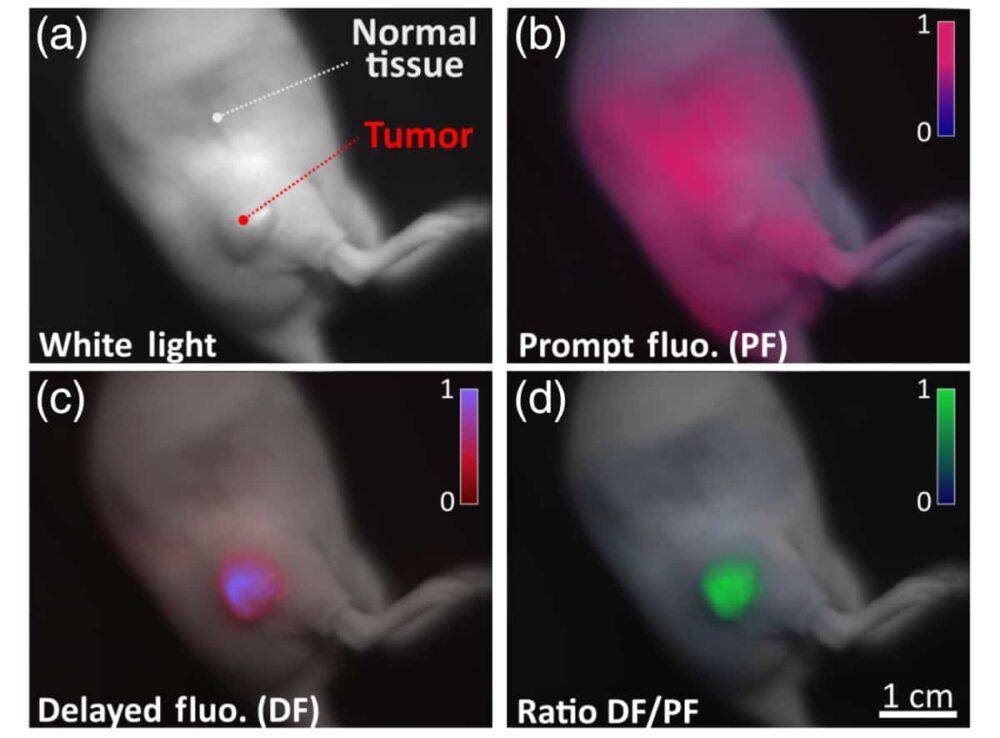
Tác giả đầu tiên Arthur Petusseau và các đồng nghiệp đã sử dụng một hệ thống hình ảnh quang học để theo dõi ánh sáng phát ra từ đầu dò phân tử nội sinh protoporphyrin IX (PpIX) trong mô hình chuột bị ung thư tuyến tụy nơi có các vùng thiếu oxy.

Các nhà nghiên cứu đã sử dụng PpIX dưới dạng thuốc mỡ tôpô hoặc thông qua tiêm vào sườn bên của con vật và tạo ra huỳnh quang bằng cách sử dụng điốt laze điều chế 635 nm làm nguồn kích thích. Họ phát hiện ra rằng tỷ lệ giữa huỳnh quang bị trì hoãn và nhanh chóng tỷ lệ nghịch với áp suất riêng phần của oxy trong mô.
Cường độ yếu của tín hiệu huỳnh quang bị trễ làm cho nó khó phát hiện về mặt kỹ thuật. Để khắc phục điều này, các nhà nghiên cứu đã sử dụng một hệ thống hình ảnh có kiểm soát thời gian cho phép theo dõi tuần tự tín hiệu huỳnh quang chỉ trong các cửa sổ thời gian nhỏ. Điều này cho phép họ giảm khả năng phát hiện tiếng ồn xung quanh và theo dõi chính xác những thay đổi trong tín hiệu huỳnh quang bị trễ.
Phân tích sâu hơn cho thấy tín hiệu huỳnh quang bị trì hoãn thu được từ các tế bào thiếu oxy ung thư lớn hơn gấp XNUMX lần so với tín hiệu thu được từ mô khỏe mạnh, được cung cấp đủ oxy. Ngoài ra, nhóm nghiên cứu cũng phát hiện ra rằng tín hiệu huỳnh quang bị trì hoãn có thể được khuếch đại hơn nữa bằng cách sờ nắn mô (dùng áp lực lên da khi kiểm tra thể chất), giúp tăng cường tình trạng thiếu oxy thoáng qua và tạo ra sự tương phản tạm thời giữa hai tín hiệu.
Petusseau cho biết: “Bởi vì hầu hết các khối u đều có sự hiện diện của tình trạng thiếu oxy vi mô trong khu vực, nên việc chụp ảnh các tín hiệu thiếu oxy từ huỳnh quang bị trì hoãn PpIX cho phép tạo ra sự tương phản tuyệt vời giữa mô bình thường và khối u”.
Quang phổ đa phương thức phát hiện khối u não trong cơ thể
Các nhà nghiên cứu kết luận rằng việc theo dõi huỳnh quang bị trì hoãn phát sinh do sự phát xạ độc nhất của đầu dò huỳnh quang PpIX khi có tình trạng thiếu oxy có một số lợi ích trong việc phân biệt giữa mô khỏe mạnh và mô ung thư trong quá trình phẫu thuật. Họ cho biết: “Việc thu được cả huỳnh quang nhanh và chậm trong một chu kỳ liên tiếp nhanh chóng cho phép chụp ảnh mức oxy theo cách không phụ thuộc vào nồng độ PpIX.
“Yêu cầu công nghệ đơn giản và khả năng tốc độ khung hình nhanh cùng với độc tính thấp của PpIX làm cho cơ chế tạo độ tương phản này có thể chuyển đổi sang con người. Nó có thể dễ dàng được sử dụng trong tương lai như một cơ chế tương phản nội tại để hướng dẫn phẫu thuật ung thư,” Petusseau tuyên bố.