U ác tính ở da là loại ung thư nguy hiểm nhất trong tất cả các loại ung thư da, đặc biệt là do nó có xu hướng xâm lấn và phát triển di căn ở các vị trí xa. Đây là bệnh ác tính nguyên phát thứ ba sau ung thư phổi và ung thư vú thường xâm chiếm não, với tỷ lệ phát triển di căn não.
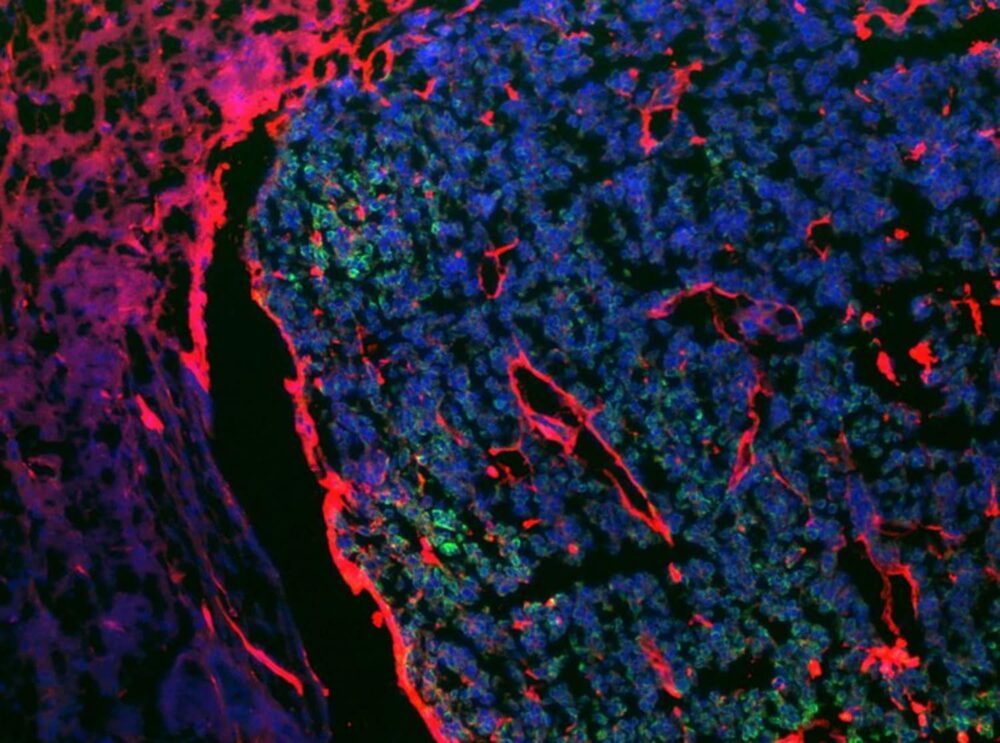
Lần đầu tiên, các nhà khoa học từ Đại học Tel Aviv đã làm sáng tỏ một cơ chế cho phép ung thư da di căn lên não và có thể làm chậm sự lây lan của bệnh từ 60% đến 80% bằng các phương pháp điều trị hiện có. Họ phát hiện ra rằng các tế bào ung thư “tuyển dụng” tế bào hình sao, tế bào hình ngôi sao nằm trong tủy sống và não chịu trách nhiệm duy trì cân bằng nội môi, hoặc các điều kiện ổn định, trong cơ thể. não, ở bệnh nhân u ác tính di căn não.
GS Ronit Satchi-Fainaro cho biết, “Ở giai đoạn nặng, 90% bệnh nhân ung thư hắc tố (ung thư da) sẽ di căn não. Đây là một thống kê khó hiểu. Chúng tôi hy vọng sẽ thấy di căn ở phổi và gan, nhưng não được cho là cơ quan được bảo vệ. Hàng rào máu não ngăn không cho các chất có hại xâm nhập vào não, và ở đây, nó được cho là không thực hiện được nhiệm vụ này—các tế bào ung thư từ da lưu thông trong máu và tìm cách đến được não. Chúng tôi tự hỏi các tế bào ung thư 'nói chuyện' với 'ai' trong não để xâm nhập vào nó.
Giáo sư Satchi-Fainaro cho biết, “Chẳng hạn, các tế bào hình sao là những tế bào đầu tiên đến để khắc phục tình hình trong trường hợp bị đột quỵ hoặc chấn thương, và cùng với chúng, tế bào ung thư tương tác, trao đổi các phân tử và làm hỏng chúng. Hơn nữa, các tế bào ung thư tuyển dụng các tế bào hình sao để chúng không ức chế sự lây lan của di căn. Do đó, chúng tạo ra tình trạng viêm cục bộ trong các khu vực tương tác giữa tế bào khối u ác tính và tế bào hình sao làm tăng tính thấm qua hàng rào máu não và sự phân chia cũng như di chuyển của các tế bào ung thư.”
“Sự giao tiếp giữa chúng được phản ánh trong thực tế là các tế bào hình sao bắt đầu tiết ra một loại protein thúc đẩy quá trình viêm gọi là MCP-1 (còn được gọi là CCL2), và để đáp ứng với điều này, các tế bào ung thư bắt đầu biểu hiện các thụ thể CCR2 và CCR4 của nó, mà chúng tôi nghi ngờ là nguyên nhân gây ra sự giao tiếp phá hoại với các tế bào hình sao.”
Các nhà khoa học đã thử nghiệm giả thuyết của họ bằng cách ức chế sự biểu hiện của protein và các thụ thể của nó trong các mô hình phòng thí nghiệm biến đổi gen và mô hình 3D của khối u ác tính nguyên phát và di căn não. Họ đã sử dụng cả kháng thể (phân tử sinh học) và phân tử nhỏ (tổng hợp) được thiết kế để ngăn chặn protein MCP-1.
Họ cũng sử dụng công nghệ CRISPR để chỉnh sửa gen tế bào ung thư và cắt bỏ hai gen biểu hiện hai thụ thể có liên quan là CCR2 và CCR4. Với mỗi phương pháp, các nhà nghiên cứu có thể trì hoãn sự lây lan của di căn.
Giáo sư Satchi-Fainaro nói, “Những phương pháp điều trị này đã thành công trong việc trì hoãn sự xâm nhập của các tế bào ung thư vào não và sau đó là sự lan rộng của chúng khắp não. Điều quan trọng cần lưu ý là khối u ác tính di căn trong não rất hung dữ, với tiên lượng xấu trong 15 tháng sau phẫu thuật, xạ trị và hóa trị. Tùy thuộc vào giai đoạn can thiệp, chúng tôi đã đạt được độ trễ từ 60% đến 80%.
“Chúng tôi đã đạt được kết quả tốt nhất với việc điều trị được tiến hành ngay sau khi phẫu thuật để loại bỏ khối u ác tính nguyên phát và chúng tôi có thể ngăn chặn các di căn xâm nhập vào não; do đó, tôi tin rằng phương pháp điều trị phù hợp với phòng khám như một biện pháp phòng ngừa.”
“Cả kháng thể và phân tử nhỏ mà chúng tôi sử dụng—chủ yếu nhằm điều trị bệnh xơ cứng bì, tiểu đường, xơ gan và bệnh tim mạch, cũng như đóng vai trò là dấu ấn sinh học cho các loại ung thư khác—đã được thử nghiệm trên người như một phần của thử nghiệm lâm sàng . Do đó, những phương pháp điều trị này an toàn và chúng ta có thể thử tái sử dụng chúng cho khối u ác tính.”
Tạp chí tham khảo:
- Sabina Pozzi, Anna Scomparin và cộng sự. Ức chế trục MCP-1/CCR2 làm nhạy cảm môi trường vi mô não chống lại sự tiến triển di căn não của khối u ác tính. Cái nhìn sâu sắc của JCI. DOI: 10.1172 / jci.insight.154804