神经退行性疾病的特征是脑功能进行性丧失,主要由中枢神经系统中的突触丧失和神经元细胞死亡引起。阿尔茨海默病(AD)可以说是导致痴呆的最常见的神经退行性疾病。 AD 的病因和发病机制尚不完全清楚,并且缺乏有效的缓解疾病的药物治疗。
先前的研究表明,遗传、环境和年龄相关因素,以及能量代谢、自噬和突触功能的改变,都有助于 AD 的发病机制。科学家们的一项新研究 斯克里普斯研究 和 麻省理工学院 (麻省理工学院)找到了分子原因的线索 阿尔茨海默氏症。这一线索也可以解释为什么女性患这种疾病的风险更大。
科学家发现,死于这种疾病的女性大脑中补体 C3 的浓度要高得多,补体 C3 是一种经过化学修饰的危险炎症反应蛋白。此外,他们证明雌激素通常可以防止形成这种类型的补体 CXNUMX。
该研究的资深作者斯图尔特·利普顿(Stuart Lipton)医学博士、哲学博士、斯克里普斯研究中心分子医学系教授兼 Step Family 基金会捐赠主席表示, “我们的新发现表明,补体系统某个组成部分的化学修饰有助于引发阿尔茨海默病,并可能至少部分解释为什么这种疾病主要影响女性。”
Lipton 的实验室研究生物化学和分子过程,例如蛋白质 S-亚硝基化,这会导致补体 C3 的修饰版本,这可能是导致 神经退行性疾病。当一氧化氮 (NO) 相关分子安全地附着在蛋白质特定氨基酸结构单元上的硫原子 (S) 上时,这种化学过程会产生修饰的“SNO 蛋白质”,这一化学过程是由 Lipton 和他的同事首先发现的。小原子团(例如 NO)经常修饰细胞中的蛋白质。
这些修饰通常会激活或失活靶蛋白的功能。由于技术困难,S-亚硝基化比其他蛋白质修饰受到的关注较少。尽管如此,Lipton 假设这些蛋白质的“SNO 风暴”可能在阿尔茨海默病和其他疾病的发展中发挥重要作用。 神经退行性疾病.
在最新的研究中,科学家们测量了 40 名死后人类体内蛋白质变化的数量。 大脑 使用全新的技术来识别S-亚硝基化。男性和女性的大脑平均分配,一半来自死于阿尔茨海默病的人,另一半来自没有死于阿尔茨海默病的人。
科学家们在这些大脑中发现了 1,449 种不同的蛋白质,这些蛋白质已被 S-亚硝基化。许多与阿尔茨海默病有关的蛋白质都是最常发生改变的蛋白质,其中包括补体 C3。令人惊讶的是,女性阿尔茨海默病患者大脑中的 S-亚硝基化 C3 (SNO-C3) 水平比男性阿尔茨海默病患者大脑高六倍多。
就进化而言,补体系统是人类免疫系统中较古老的组成部分。 “补体级联”由一系列蛋白质组成,其中包括 C3,它们可以相互激活以引起炎症。 30多年来,科学家们已经知道,与神经系统健康的大脑相比,阿尔茨海默病患者的大脑表现出更高含量的补体蛋白和其他炎症指标。
最近的研究特别证明了补体蛋白如何导致大脑驻留的免疫细胞(称为小胶质细胞)降解突触。在这些路口, 神经元 互相沟通。突触丧失与阿尔茨海默病认知能力下降有很大关系,许多科学家现在认为这种突触破坏机制至少部分驱动了疾病进程。
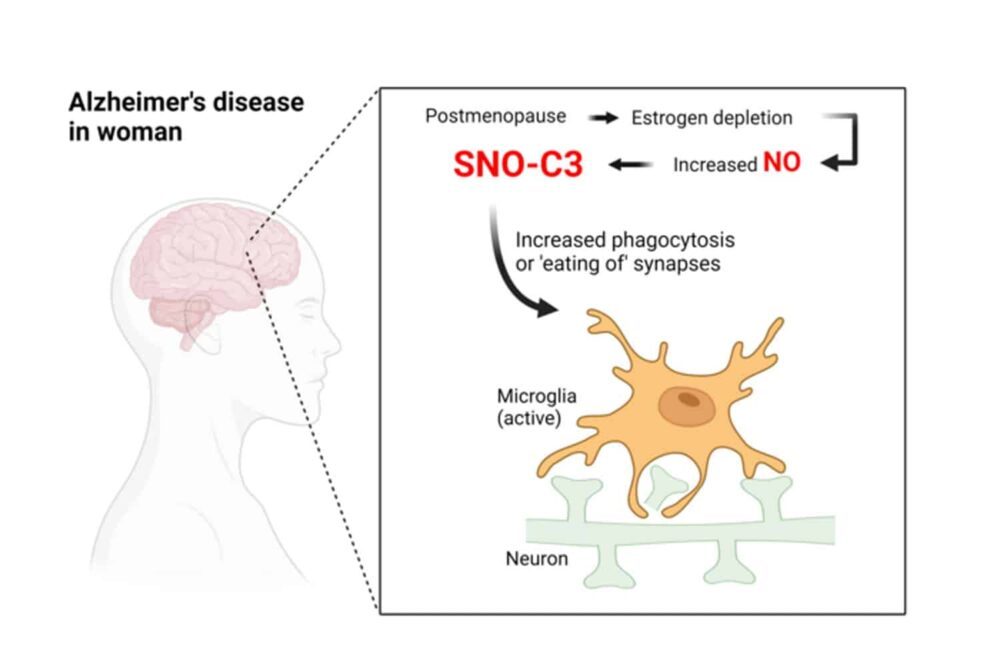
为什么患有阿尔茨海默病的女性大脑中 SNO-C3 的患病率更高?科学家们提出了这样的假设:雌激素明确地保护女性大脑免受 C3 S-亚硝基化作用,并且当雌激素水平随着更年期急剧下降时,这种保护就会消失。长期以来就有证据表明,女性荷尔蒙雌激素在某些情况下可以具有大脑保护作用。
这一理论得到了使用培养的人脑细胞的实验的验证,该实验表明,由于激活了脑细胞中产生 NO 的酶,随着雌激素(-雌二醇)水平下降,SNO-C3 会增加。 SNO-C3 的升高会引发小胶质细胞对突触的降解。
研究资深作者斯图尔特·利普顿(Stuart Lipton)医学博士、博士, 说过, “为什么女性更容易患阿尔茨海默氏症长期以来一直是个谜,但我认为我们的研究结果代表了这个谜题的重要组成部分,从机械上解释了女性随着年龄增长而变得越来越脆弱。”
“基于 C3 蛋白的异常 S-亚硝基化,深入了解女性在阿尔茨海默病中占主导地位的机制。”
杂志参考:
- 杨红梅等。基于 C3 异常蛋白 S-亚硝基化对女性在阿尔茨海默病中占主导地位的机制洞察。 科学进展。 DOI: 10.1126/sciadv.ade0764