免疫疗法——利用人体自身的免疫系统来对抗癌症——有可能彻底改变癌症治疗。 但是,虽然白血病和淋巴瘤等血癌对癌症免疫疗法反应良好,但实体瘤的反应有限。
造成这种差异的一个可能原因是不同癌症中表面蛋白的不同表达。 例如,膜结合蛋白 SLAMF7——激活免疫系统并促使免疫细胞吞噬(摄取)癌细胞——由血癌细胞表达,但不由实体瘤表达。
为了使实体瘤细胞更容易接受免疫疗法,研究人员在 德克萨斯州大学安德森癌症中心 开发了一个纳米技术平台来触发他们对 SLAMF7 的表达。 描述于 自然纳米技术,该平台基于双特异性肿瘤转化纳米颗粒 (BiTN),该纳米颗粒包含与肿瘤靶向配体和 SLAMF7 结合的聚合物核心。
“有了这个新平台,我们现在有了一种策略,可以至少在免疫学上将实体瘤转化为类似于血液肿瘤,这种肿瘤通常对免疫疗法有更高的反应率,”说 文江, 谁与共同领导了这项研究 贝蒂·金. “如果我们能够在临床上转化和验证这种方法,它可能使我们能够更接近免疫治疗药物对传统上反应不佳的癌症的最大活性水平。”
细胞/组织 和 体内 评定
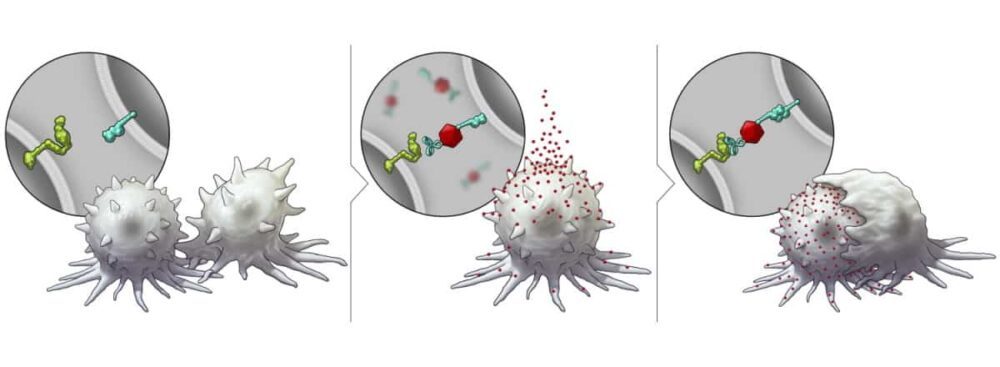
研究人员首先调查了该平台 细胞/组织,使用 HER2 阳性乳腺癌细胞。 他们通过将纳米颗粒与抗 HER2 抗体结合以结合肿瘤细胞,并结合 SLAMF7 来激活免疫反应,从而为该应用创造了细胞特异性 BiTN。 由此产生的纳米偶联物——BiTNHER – 选择性靶向 HER2 阳性乳腺癌细胞并用 SLAMF7 标记它们。
该团队证实,BiTNHER与未结合的纳米颗粒相比,-标记的癌细胞引起更高水平的吞噬作用。 BiTNHER 还使乳腺癌细胞对抗 CD47 抗体治疗敏感,从而阻断肿瘤细胞发出的“别吃我”信号,进一步提高吞噬活性。
接下来,团队评估了 BiTNHER 在患有乳腺癌肿瘤的小鼠中,TUBO 细胞表达啮齿类动物的 HER2,或缺乏该受体的 4T1 细胞。 用 BiTN 处理HER 加上抗 CD47 显着降低了肿瘤负荷并延长了患有 TUBO 肿瘤的小鼠的生存期; 在4T1肿瘤中未观察到抗肿瘤作用。
研究人员指出,与单独使用 BiTN 或抗 CD47 相比,联合治疗可显着抑制肿瘤。 一项长期毒性研究发现,未治疗和治疗小鼠的血细胞计数没有显着差异。
为了证明 BiTN 平台的多功能性,研究人员定制了纳米颗粒以靶向另一种肿瘤受体——三阴性乳腺癌表达的叶酸受体。 他们创造了 BiTNFo 通过用叶酸替代抗 HER2 抗体。 BiTNFo 靶向癌细胞并将其转化为表达 SLAMF7 的细胞。 正如预期的那样,用 BiTN 孵育 4T1 细胞Fo 和抗 CD47 导致比 TUBO 细胞更大的吞噬作用。
“因为这些是工程构造,这可以作为一种即插即用的方法,将不同的肿瘤靶向剂或免疫分子结合到纳米颗粒的表面上,”Kim 在一份新闻声明中说。
研究人员还测试了 BiTNFo 在自发性 4T1 转移小鼠模型中,用 BiTN 治疗原发性肿瘤Fo 和手术切除前的抗 CD47。 这种组合抑制了局部疾病复发,但没有减少远处转移或延长总生存期。 然而,在治疗中加入抗 PD1 会导致转移抑制延长,七只小鼠中有两只表现出长期无肿瘤存活。
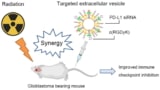
免疫疗法加放射治疗可治疗小鼠脑肿瘤
最后,为了进一步增强该模型的转化相关性,该团队研究了一种术后治疗方案。 在这里,小鼠的肿瘤在第 12 天未经任何预处理被切除,然后从第 15 天开始,动物接受 BiTN 的三重组合治疗Fo,抗CD47和抗PD1。 这种术后治疗抑制了转移并延长了生存期——这表明即使没有肿瘤内治疗,BiTN 也可以帮助消除残留的肿瘤细胞并减少全身性疾病。
接下来,研究人员正专注于将这项新技术转化为临床。 “为了使临床转化更容易,我们正在探索一种基于蛋白质的策略,我们将开发一种双特异性蛋白质,其作用类似于 BiTN,”Jiang 说。 物理世界. “这将需要一些蛋白质/抗体工程,但可能更容易满足监管部门的批准。”