Ældrende immunsystemceller er potentielt blandt de mest skadelige af alle ældende celler, fordi de spreder vævsskade og hurtig aldring på tværs af andre kropsorganer og -systemer. Men en opdagelse af UC San Francisco tyder på, at ikke alle ældre celler er skadelige "zombier".
Mens de genvurderede rollen som "zombie"-celler, som anti-aldringsmedicin har forsøgt at eliminere, fandt forskerne ud af, at nogle er indlejret i unge, sunde væv og fremmer normal reparation fra skader.
Forskere har nu observeret disse celler i aktion i lungevæv og andre organer, der fungerer som barrierer i kroppen, såsom tyndtarmen, tyktarmen og huden. Lungevævsskader kommer sig langsommere, når de behandles med senolytiske lægemidler, og dræber disse celler.
Tien Peng, MD, lektor i lunge-, kritisk pleje, allergi og søvnmedicin og seniorforfatter af undersøgelsen, sagde: "Senescentceller kan indtage nicher med privilegerede positioner som 'vagtposter', der overvåger væv for skader og reagerer ved at stimulere nærliggende stamceller til at vokse og igangsætte reparation."
"Det var forståeligt, at videnskabsmænd oprindeligt så senescerende celler som rent skadelige. Efterhånden som mennesker bliver ældre, akkumulerer ældningsceller karakteristika af gamle, slidte celler, herunder manglende evne til at lave nye celler. I stedet for at dø som normale gamle celler, lever de videre og udspyder en cocktail af inflammatoriske forbindelser, der danner den senescens-associerede sekretoriske fænotype (SASP). Disse faktorer er knyttet til Alzheimers, artritis, og andre aldersrelaterede lidelser, herunder kræft. Det iørefaldende navn "zombieceller" blev opfundet for dem.
Forskere gjorde den fantastiske opdagelse, at fjernelse af ældningsceller fra mus forhindrede eller reducerede aldersrelateret sygdom og øgede dyrenes levetid ved hjælp af senolytika, der målretter mod og dræber "zombieceller." Derefter skete der en stigning i aktiviteten i forskningslaboratorier og farmaceutiske virksomheder, dedikeret til at finde og udvikle mere potente versioner af disse medikamenter.
Fjernelse af senescentceller indebærer dog risici. For eksempel viste denne nylige undersøgelse, at senescerende celler også kan fremme rutinemæssig heling ved at udløse stamcellereparation. Ifølge den nye forskning kan analyser have en negativ indvirkning på normal reparation, men de behandler også potentielt lidelser, hvor ældre celler er ansvarlige for patologisk stamcelleadfærd.
Ældrende celler kan være udfordrende at undersøge, da deres indikatorer, såsom genet p16, nogle gange er knappe og udfordrende at finde. I tidlige eksperimenter blev fibroblastiske celler isoleret, dyrket i kulturskåle, indtil der var tilstrækkeligt antal celler til eksperimenter, og derefter stresset med kemikalier, der forårsagede ældning i cellerne. Men i levende ting, interaktioner mellem celler og vævene omkring dem påvirker cellernes genaktivitet væsentligt. Dette betyder, at sammenlignet med celler i deres normale miljø, kan funktionerne ved celler, der vokser isoleret i en glasfad, afvige.
For at skabe et mere kraftfuldt værktøj til deres undersøgelser forbedrede forskerne en almindelig teknik til at fusionere et relevant gen - i dette tilfælde p16-genet, som er alt for aktivt i senescerende celler - med et grønt fluorescerende protein (GFP) som en markør, der kan afsløre cellernes placering under ultraviolet lys. Forskere forstærkede signifikant det fluorescerende signal ved at øge mængden og stabiliteten af det grønne fluorescerende protein i disse senescerende celler. Dette gjorde det muligt for dem at se senescent celler i deres naturlige habitat af levende væv.
Forskerne fandt ud af, at ældningsceller eksisterer i unge og sunde væv i større omfang end tidligere antaget og begynder at udvikle sig kort efter fødslen ved hjælp af denne ekstremt følsomme teknologi. Forskerne opdagede også særlige vækstfaktorer, som senescentceller udsender for at tilskynde stamceller til at formere sig og hele væv. Afsløringen af, at immunsystemceller som makrofager og monocytter kan aktivere ældningsceller, er relevant for aldring og vævsskade. Dette fund indebærer, at betændelse i gammelt eller skadet væv er en afgørende regulator af senescent celleaktivitet og regenerering.
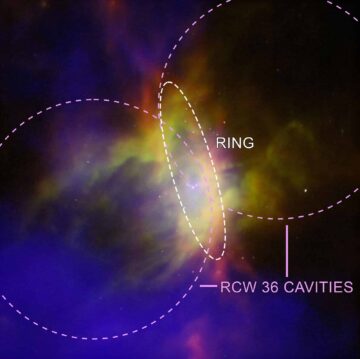
I deres undersøgelser af lungevæv observerede Pengs hold grønt lysende senescentceller, der lå ved siden af stamceller på basalmembranen, der fungerer som en barriere, der forhindrer fremmede celler og skadelige kemikalier i at trænge ind i kroppen og tillader ilt at diffundere fra luften i lungerne ind i underliggende væv. Der kan opstå skader på denne dynamiske grænseflade. Holdet så senescerende celler i lignende positioner i andre barriereorganer, såsom tyndtarmen, tyktarmen og huden. Deres eksperimenter bekræftede, at hvis senescerende celler blev dræbt med senolytika, kunne lungestamceller ikke reparere barriereoverfladen korrekt.
Uddannet professor i eksperimentel patologi sagde Pengs undersøgelse er virkelig vigtig for aldringsforskning, hvor målet er at hjælpe individer med at leve længere og sundere.
"Undersøgelserne tyder på, at forskning i senolytik bør fokusere på at genkende og præcist målrette skadelige senescerende celler, måske ved de tidligste tegn på sygdom, samtidig med at de hjælper intakte," sagde hun. "Disse resultater understreger behovet for at udvikle bedre lægemidler og små molekyler, der vil målrette mod specifikke undergrupper af senescerende celler, der er involveret i sygdom frem for regenerering."
Journal Reference:
- Nabora S. Reyes et al. Sentinel p16INK4a+ celler i basalmembranen danner en reparativ niche i lungen. Videnskab. DOI: 10.1126/science.abf33