Die altersbedingte Makuladegeneration (AMD) ist eine der Hauptursachen für Blindheit. Es beginnt in der äußeren Blut-Retina-Barriere (oBRB), die vom retinalen Pigmentepithel (RPE), der Bruch-Membran und der Choriocapillaris gebildet wird. Aufgrund des Mangels an physiologisch relevanten menschlichen oBRB-Modellen müssen die Entstehungs- und Progressionsmechanismen der AMD noch besser verstanden werden.
Das Forschungsteam des National Eye Institute (NEI), Teil der National Institutes of Health, verwendete einen Patienten Stammzellen und 3D-Bioprinting zur Herstellung von Augengewebe, das das Verständnis der Mechanismen von Erblindungskrankheiten voranbringen wird. Wissenschaftler haben eine Kombination von Zellen gedruckt, die die äußere Blut-Retina-Schranke bilden.
Das retinale Pigmentepithel (RPE), getrennt von der blutgefäßreichen Choriocapillaris Bruchsche Membran, bildet die äußere Blut-Retina-Schranke. Choriocapillaris und RPE tauschen Nährstoffe und Abfallstoffe unter der Kontrolle der Bruch-Membran aus. Drusen, das sind Lipoproteinansammlungen, entwickeln sich bei AMD außerhalb der Bruch-Membran und behindern deren Funktion. Der RPE-Abbau führt im Laufe der Zeit zu einer Verschlechterung der Photorezeptoren und einem Sehverlust.
Wissenschaftler kombinierten drei unreife Aderhautzelltypen in einem Hydrogel: Perizyten, Endothelzellen und Fibroblasten. Anschließend druckten sie das Gel auf ein biologisch abbaubares Gerüst. Innerhalb weniger Tage begannen die Zellen zu einem dichten Kapillarnetzwerk heranzureifen.
Am neunten Tag besiedelten die Wissenschaftler retinale Pigmentepithelzellen auf der Rückseite des Gerüsts. Das bedruckte Gewebe erreichte am 42. Tag seine volle Reife. Gewebeanalysen sowie genetische und funktionelle Tests zeigten, dass das gedruckte Gewebe ähnlich aussah und sich ähnlich verhielt wie die natürliche äußere Blut-Retina-Schranke.
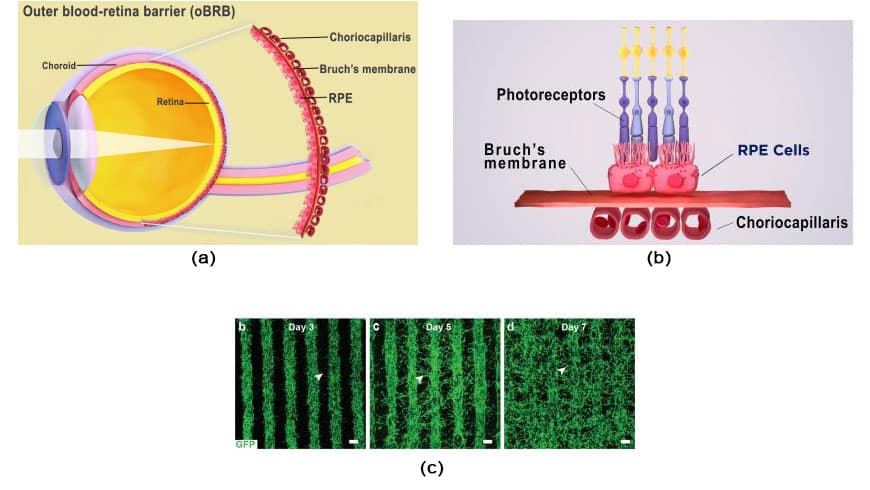
B. Die äußere Blut-Netzhaut-Schranke des Auges besteht aus dem retinalen Pigmentepithel, der Bruch-Membran und der Choriocapillaris. Bildnachweis: National Eye Institute.
C. Wachstum von Blutgefäßen über gedruckte Reihen einer Endothel-Perizyten-Fibroblasten-Zellmischung. Am 7. Tag füllen Blutgefäße den Raum zwischen den Reihen und bilden ein Netzwerk aus Kapillaren. Bildnachweis: Kapil Bharti.
Unter Belastung zeigte bedrucktes Gewebe AMD-Merkmale im Frühstadium, wie z. B. Drusenablagerungen unter dem RPE, und entwickelte sich zu einem trockenen AMD-Stadium im Spätstadium, bei dem ein Gewebeabbau beobachtet wurde. Niedrige Sauerstoffwerte verursachten ein feuchtes AMD-ähnliches Aussehen mit Hyperproliferation der Aderhautgefäße, die sich in die Sub-RPE-Zone verlagerte. Bei der Behandlung von AMD verlangsamten Anti-VEGF-Medikamente die Bildung und Migration von Blutgefäßen und verbesserten gleichzeitig die Gewebeform.
Kapil Bharti, Ph.D., der die NEI-Sektion für translationale Augen- und Stammzellforschung leitet, sagte: „Durch das Drucken von Zellen erleichtern wir den Austausch zellulärer Signale, die für die normale Anatomie der äußeren Blut-Retina-Barriere erforderlich sind. Beispielsweise induziert die Anwesenheit von RPE-Zellen Genexpression Veränderungen in Fibroblasten, die zur Bildung der Bruch-Membran beitragen – etwas, das vor vielen Jahren vorgeschlagen, aber erst mit unserem Modell bewiesen wurde.“
Die Wissenschaftler befassten sich mit zwei technologischen Problemen: der Schaffung eines geeigneten biologisch abbaubaren Gerüsts und der Erzielung eines konsistenten Druckmusters. Sie entwickelten ein temperaturempfindliches Hydrogel, das bei kaltem Gel deutliche Reihen erzeugte, sich aber auflöste, wenn das Gel erwärmt wurde. Durch die gute Reihenkonsistenz wurde ein genaueres System zur Beurteilung der Gewebearchitektur ermöglicht. Darüber hinaus optimierten sie den Anteil von Fibroblasten, Endothelzellen und Perizyten im Zellverbund.
Co-Autor Marc Ferrer, Ph.D., Direktor des 3D Tissue Bioprinting Laboratory am National Center for Advancing Translational Sciences des NIH, und sein Team stellten Fachwissen für die Biofabrikation der äußeren Blut-Retina-Barrieregewebe „in-a-well“ zur Verfügung. ” zusammen mit analytischen Messungen, um ein Drogenscreening zu ermöglichen.
[Eingebetteten Inhalt]
„Unsere gemeinsamen Bemühungen haben zu sehr relevanten Netzhautgewebemodellen degenerativer Augenerkrankungen geführt“, sagte Ferrer sagte. „Solche Gewebemodelle haben viele potenzielle Einsatzmöglichkeiten für translationale Anwendungen, einschließlich der Entwicklung von Therapeutika.“
Journal Referenz:
- Min Jae Song, Russ Quinn et al. Bioprinted 3D äußere Netzhautbarriere deckt RPE-abhängigen Aderhautphänotyp bei fortgeschrittener Makuladegeneration auf. Nature Methods, 2022; DOI: 10.1038/s41592-022-01701-1