معرفی
کشف در خلال پروژه ژنوم انسان در اوایل دهه 2000 مبنی بر اینکه ما انسان ها تنها حدود 20,000 ژن کد کننده پروتئین داریم - تقریباً به اندازه کرم نماتد کوچک ساکن در خاک و کمتر از نصف گیاه برنج - باعث شوکه شد. . با این حال، این ضربه به غرور ما با این ایده که ژنوم انسان غنی از ارتباطات نظارتی است، کاهش یافت. ژنهای ما در شبکهای متراکم برهمکنش میکنند، که در آن قطعات DNA و مولکولهایی که کدگذاری میکنند (RNA و پروتئینها) «بیان» ژنهای دیگر را کنترل میکنند و بر ساختن RNA و پروتئینهای مربوطه خود تأثیر میگذارند. برای درک ژنوم انسان، باید این فرآیند تنظیم ژن را درک کنیم.
با این حال، این کار بسیار دشوارتر از رمزگشایی توالی ژنوم است.
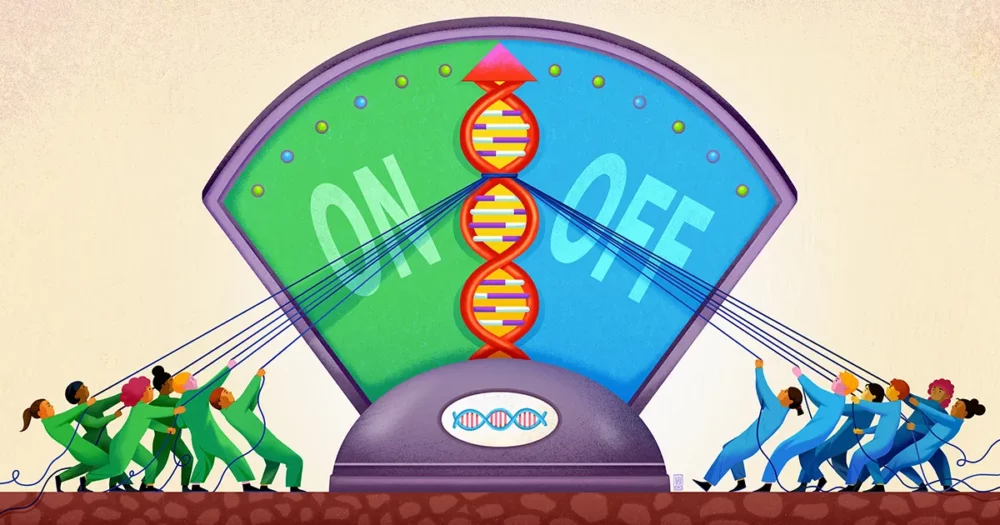
در ابتدا، گمان بر این بود که تنظیم ژن یک موضوع ساده از یک محصول ژنی است که به عنوان کلید روشن/خاموش برای یک ژن دیگر، به روش دیجیتال عمل می کند. در دهه 1960، زیست شناسان فرانسوی فرانسوا ژاکوب و ژاک مونود برای اولین بار توضیح دادند. یک فرآیند تنظیم ژن در جزئیات مکانیکی: در اشریشیا کولی هنگامی که یک پروتئین سرکوبگر به بخش خاصی از DNA متصل می شود، رونویسی و ترجمه مجموعه ای از ژن های مجاور را که آنزیم هایی را برای هضم لاکتوز قند رمزگذاری می کنند، مسدود می کند. این مدار تنظیمی که مونود و ژاکوب به آن لقب دادند لاک اپرون، منطق منظم و شفافی دارد.
اما به نظر می رسد تنظیم ژن در متازوئن های پیچیده - حیواناتی مانند انسان، با سلول های یوکاریوتی پیچیده - به طور کلی به این روش کار نمی کند. در عوض، شامل گروهی از مولکولها، از جمله پروتئینها، RNA ها و تکههای DNA از سرتاسر کروموزوم است که به نوعی برای کنترل بیان یک ژن با یکدیگر همکاری میکنند.
این فقط این نیست که این فرآیند تنظیمی در یوکاریوت ها تعداد بازیکنان بیشتری نسبت به باکتری ها و سایر سلول های ساده پروکاریوتی دارد. به نظر می رسد که این روند کاملاً متفاوت و مبهم تر است.
تیمی در دانشگاه استنفورد به رهبری این بیوفیزیکدان و مهندس زیستی پولی فوردایسبه نظر می رسد که اکنون جزء این حالت فازی تنظیم ژن را کشف کرده است. کار آنها، منتشر شده در سپتامبر گذشته در علم، نشان می دهد که DNA نزدیک یک ژن به عنوان نوعی چاه کم عمق برای به دام انداختن مولکول های تنظیم کننده مختلف عمل می کند و آنها را برای عمل آماده نگه می دارد تا در صورت نیاز بتوانند صدای خود را به تصمیم در مورد فعال کردن ژن اضافه کنند.
معرفی
این چاههای تنظیمی از بخشهای مشخصی از DNA ساخته شدهاند. آنها متشکل از توالی هایی هستند که در آن یک کشش کوتاه از DNA، از یک تا شش جفت باز، چندین بار تکرار می شود. دهها نسخه از این «تکرارهای پشت سر هم کوتاه» (STR) را میتوان در این توالیها، مانند همان «کلمه» کوچکی که بارها و بارها نوشته میشود، کنار هم قرار داد.
STRها در ژنوم انسان فراوان هستند: آنها حدود 5 درصد از کل DNA ما را تشکیل می دهند. زمانی تصور میشد که آنها نمونههای کلاسیک DNA ناخواسته هستند، زیرا یک «متن» DNA تکراری که فقط از STR تشکیل شده است، نمیتواند تقریباً به اندازه توالی نامنظم حروفی که یک جمله را در این جمله میسازد، اطلاعات معنیداری را در خود جای دهد. مقاله.
با این حال، STR ها به وضوح بی اهمیت نیستند: آنها با بیماری هایی مانند بیماری هانتینگتون، آتروفی عضلانی اسپینوبولبار، بیماری کرون و برخی سرطان ها مرتبط هستند. در طول چند دهه گذشته، شواهدی جمع آوری شده است که نشان می دهد آنها می توانند به نحوی تنظیم ژن را تقویت یا مهار کنند. رمز و راز این بود که چگونه میتوانستند با محتوای اطلاعاتی اینقدر قدرتمند باشند.
کنترل های پیچیده برای سلول های پیچیده
برای درک اینکه چگونه STRها در تصویر بزرگ تنظیم ژن قرار می گیرند، اجازه دهید یک قدم به عقب برگردیم. ژنها معمولاً توسط قطعاتی از DNA احاطه میشوند که RNA یا پروتئین را کد نمیکنند، اما عملکردهای تنظیمی دارند. ژنهای باکتری دارای نواحی «پروتکن» هستند که در آن آنزیمهای پلیمراز میتوانند برای شروع رونویسی DNA مجاور به RNA متصل شوند. آنها همچنین به طور معمول دارای مناطق "اپراتور" هستند، جایی که پروتئین های سرکوب کننده می توانند برای مسدود کردن رونویسی متصل شوند و یک ژن را خاموش کنند، همانطور که در لاک اپرون
در انسان و سایر یوکاریوت ها، توالی های تنظیمی می توانند متعدد، متنوع تر و گیج کننده باشند. به عنوان مثال، مناطقی که تقویت کننده نامیده می شوند، بر احتمال رونویسی یک ژن تأثیر می گذارند. تقویت کننده ها اغلب هدف پروتئین هایی به نام فاکتورهای رونویسی هستند که می توانند برای تقویت یا مهار بیان ژن متصل شوند. به طرز عجیبی، برخی از تقویتکنندهها دهها هزار جفت باز از ژنهایی که تنظیم میکنند فاصله دارند و تنها از طریق بازآرایی فیزیکی حلقههای DNA در یک کروموزوم پر شده به آنها نزدیک میشوند.
تنظیم ژن یوکاریوتی معمولاً شامل این بلوکهای تنظیمکننده متنوع DNA، همراه با یک یا چند فاکتور رونویسی و مولکولهای دیگر است که همگی در اطراف یک ژن جمع میشوند، مانند کمیتهای که برای تصمیمگیری در مورد اینکه چه کاری باید انجام دهد، جمع میشوند. آنها در یک خوشه شل و متراکم جمع می شوند.
اغلب، به نظر نمیرسد که شرکتکنندگان مولکولی از طریق جفتهای بسیار انتخابی «قفل و کلید» رایج در زیستشناسی مولکولی تعامل داشته باشند. آنها در عوض بسیار کمتر اهل انتخاب هستند، نسبتاً ضعیف و غیرانتخابی تعامل می کنند، گویی در حال سرگردانی و گفتگوهای کوتاه با یکدیگر هستند.
در واقع، نحوه اتصال عوامل رونویسی به DNA در یوکاریوتها یک معما بوده است. مدتها تصور میشد که بخشی از یک فاکتور رونویسی باید دقیقاً با یک توالی «موتیف» پیوندی در DNA مطابقت داشته باشد، مانند قطعات یک پازل. اما اگرچه برخی از این نقوش شناسایی شدهاند، حضور آنها همیشه با جایی که دانشمندان فاکتورهای رونویسی چسبیده به DNA در سلولها را پیدا میکنند، ارتباط خوبی ندارد. گاهی اوقات عوامل رونویسی در مناطق بدون هیچ نقش و نگار باقی می مانند، در حالی که برخی از نقوش که به نظر می رسد باید به شدت عوامل رونویسی را پیوند دهند خالی می مانند.
فوردایس گفت: "به طور سنتی در ژنومیک، هدف طبقه بندی مکان های ژنومی به روشی [دودویی] به عنوان "محصول" یا "بی بند" توسط فاکتورهای رونویسی بوده است. "اما تصویر بسیار ظریف تر از این است." به نظر نمیرسد که اعضای فردی آن «کمیتههای» تنظیمکننده ژن همیشه در جلسات خود حضور داشته باشند یا در آن غایب باشند، بلکه احتمالات متفاوتی برای حضور یا عدم حضور دارند.
این بیوفیزیکدان گفت: تمایل به تنظیم ژن در یوکاریوت ها برای تکیه بر بسیاری از برهمکنش های ضعیف و متنوع در میان کمپلکس های مولکولی بزرگ «یکی از مواردی است که کنترل آن را از نظر تئوری بسیار دشوار می کند». توماس کولمن از دانشگاه کالیفرنیا، ریورساید، که نوشت یک تفسیر روی کاغذ آزمایشگاه فوردایس برای علم. این یک معمای عمیق است که چگونه، از این فرآیند به ظاهر آشفته، تصمیمات دقیق در مورد روشن و خاموش کردن ژن ها پدید می آید.
فراتر از منطق فازی مرموز این فرآیند تصمیم گیری، این سؤال نیز وجود دارد که چگونه همه اعضای کمیته حتی راه خود را به اتاق مناسب پیدا می کنند - و سپس در آنجا می مانند. مولکولها عموماً با انتشار در اطراف سلول حرکت میکنند، توسط سایر مولکولهای اطراف مانند آب تحت تأثیر قرار میگیرند و در جهتهای تصادفی سرگردان میشوند. ممکن است انتظار داشته باشیم که این کمیته های سست خیلی سریع از هم جدا شوند تا بتوانند وظایف نظارتی خود را انجام دهند.
فوردایس و همکارانش فکر میکنند که این همان جایی است که STRها وارد میشوند. در مقاله خود، محققان استدلال میکنند که STRها بهعنوان تکههای چسبنده عمل میکنند که فاکتورهای رونویسی را تشکیل میدهند و از انحراف آنها جلوگیری میکنند.
تنظیم دقیق چسبندگی
گروه فوردایس به طور سیستماتیک بررسی کردند که چگونه تفاوتها در توالی STR بر چسبیدن فاکتورهای رونویسی به یک موتیف اتصال تأثیر میگذارد. آنها دو عامل را مورد بررسی قرار دادند - یکی از مخمرها، یکی از انسان ها - که به یک موتیف شش پایه خاص می چسبند. محققان هم قدرت (یا میل ترکیبی) آن اتصال و هم سرعت گیرکردن و گیر نکردن فاکتورهای رونویسی (سینتیک) را هنگامی که موتیف به جای دنباله تصادفی توسط یک STR کنار هم قرار میگیرد، اندازهگیری کردند. برای مقایسه، آنها بررسی کردند که چگونه فاکتورها به تنهایی به STR و به یک توالی DNA کاملا تصادفی متصل می شوند.
گفت: «یکی از بزرگترین چالشهای این زمینه، تفکیک بیشمار متغیرهایی است که بر اتصال [عامل رونویسی] در یک موقعیت خاص از ژنوم تأثیر میگذارند». دیوید سوتر، زیست شناس مولکولی در موسسه فناوری فدرال سوئیس لوزان در سوئیس. شکل DNA، نزدیکی به بخشهای دیگر DNA و کشش فیزیکی در مولکولهای DNA، همگی میتوانند در اتصال فاکتور رونویسی نقش داشته باشند. مقادیر این پارامترها احتمالاً در هر موقعیتی در ژنوم و شاید بین انواع سلول ها و در یک سلول واحد در طول زمان در یک موقعیت مشخص متفاوت است. ساتر گفت: "این فضای وسیعی از متغیرهای ناشناخته است که تعیین کمیت آنها بسیار دشوار است."
معرفی
کولمن افزود، به همین دلیل است که آزمایشهای خوب کنترل شده مانند آزمایشهای تیم استنفورد بسیار مفید است. معمولاً، وقتی محققان نیاز به اندازهگیری برهمکنشهای ضعیف مانند این دارند، دو انتخاب دارند: میتوانند چند اندازهگیری بسیار دقیق و بسیار دقیق انجام دهند و از آنها تعمیم دهند، یا میتوانند تعداد زیادی اندازهگیری سریع و کثیف انجام دهند و از نظر ریاضی پیچیده استفاده کنند. روش های آماری برای استنباط نتایج اما فوردایس و همکارانش، کولمن گفت، از یک روش خودکار مبتنی بر تراشه میکروسیال برای انجام اندازهگیریهای دقیق در طول آزمایشهای با توان بالا استفاده کردند تا «بهترینها را از هر دو دنیا به دست آورند».
تیم استنفورد دریافتند که توالیهای مختلف STR میتوانند پیوندهای فاکتورهای رونویسی به DNA را تا 70 تغییر دهند. آنها گاهی اوقات تأثیر بیشتری بر اتصال فاکتور رونویسی نسبت به تغییر توالی خود موتیف اتصال دارند. و اثرات برای دو فاکتور رونویسی متفاوتی که آنها به آن نگاه کردند متفاوت بود.
بنابراین به نظر می رسد که STRها قادر به تنظیم دقیق توانایی فاکتورهای رونویسی برای اتصال به یک سایت DNA و در نتیجه تنظیم یک ژن هستند. اما دقیقاً چگونه؟
یک اتاق انتظار در نزدیکی یک ژن
محققان دریافتند که بخشی از یک فاکتور رونویسی که DNA را به هم متصل میکند، ممکن است برهمکنش ضعیفی با یک STR داشته باشد، با شدت دقیق آن وابستگی بسته به توالی STR. از آنجا که چنین اتصال ضعیفی است، ویژگی خاصی نخواهد داشت. اما اگر یک فاکتور رونویسی بارها و بارها توسط یک STR آزاد شده و آزاد شود، اثر تجمعی این است که فاکتور رونویسی را در مجاورت ژن نگه میدارد تا در صورت نیاز احتمال بیشتری وجود داشته باشد که به طور ایمن به ناحیه موتیف متصل شود.
فوردایس و همکارانش پیشبینی کردند که STRها در نتیجه بهعنوان یک «لابی» یا چاهی عمل میکنند که عوامل رونویسی میتوانند، هرچند موقت، در نزدیکی یک سایت الزامآور نظارتی جمع شوند. گفت: "ماهیت تکراری یک STR اثر ضعیف هر محل اتصال واحدی را که از آن ساخته شده است، تقویت می کند." کانر هورتون، اولین نویسنده این مطالعه که اکنون دانشجوی دکترا در دانشگاه کالیفرنیا، برکلی است.
برعکس، او افزود، برخی از STR ها همچنین می توانند عوامل رونویسی را از توالی های تنظیمی دور کنند و عوامل رونویسی را در جاهای دیگر مانند یک اسفنج جذب کنند. به این ترتیب آنها می توانند بیان ژن را مهار کنند.
سوتر گفت: این کار به طور قانع کننده ای نشان می دهد که STR ها مستقیماً بر اتصال فاکتورهای رونویسی در شرایط آزمایشگاهی تأثیر می گذارند. علاوه بر این، تیم استنفورد از یک الگوریتم یادگیری ماشین استفاده کرد تا نشان دهد که اثرات مشاهده شده در آزمایشات آزمایشگاهی آنها در سلولهای زنده نیز به نظر میرسد (یعنی in vivo).
اما رابرت تجیانیک بیوشیمیدان در برکلی و محقق در موسسه پزشکی هاوارد هیوز، فکر میکند برای اطمینان از اینکه ترکیب فاکتور رونویسی STR چه تأثیری بر بیان ژن در سلولهای واقعی دارد، خیلی زود است.
تژیان، خاویر دارزاک و همکارانشان در آزمایشگاهی که با هم در برکلی اداره میکنند موافق هستند که به نظر میرسد STRها راهی برای متمرکز کردن فاکتورهای رونویسی در نزدیکی مکانهای تنظیمکننده ژن ارائه میدهند. با این حال، بدون دانستن اینکه فاکتورها چقدر باید برای فعال کردن رونویسی نزدیک باشند، درک اهمیت عملکردی آن نتیجه دشوار است. Tjian گفت که او مایل است ببیند که آیا معرفی یک STR به یک سلول زنده به طور قابل پیش بینی بر بیان یک ژن هدف تأثیر می گذارد یا خیر. او گفت که در حال حاضر "متقاعد نشده است که STR ها لزوماً یک جنبه اصلی مکانیسم های [تنظیمی] در داخل بدن باشند."
یک گرامر ترکیبی
یکی از معماهای ماندگار این است که چگونه چنین مکانیزمی به طور قابل اعتمادی نوع تنظیم دقیق ژن مورد نیاز سلول ها را فراهم می کند، زیرا هم قدرت و هم گزینش پذیری اتصال فاکتور رونویسی در چاهک های STR ضعیف است. فوردایس فکر میکند که چنین ویژگی تأثیری میتواند از منابع بسیاری ناشی شود - نه فقط از تفاوتها در توالیهای STR، بلکه همچنین از تعاملات مشترک بین فاکتورهای رونویسی و سایر پروتئینهای دخیل در تنظیم.
هورتون گفت با توجه به همه اینها، مشخص نیست که پیشبینی اثر یک ترکیب فاکتور رونویسی STR بر بیان یک ژن ساده باشد. منطق این فرآیند در واقع مبهم است. و هورتون اضافه کرد که "دستور زبان" تأثیر احتمالاً ترکیبی است: نتیجه به ترکیبات مختلف عوامل رونویسی و سایر مولکول ها بستگی دارد.
تیم استنفورد فکر میکند که شاید 90 درصد از فاکتورهای رونویسی به STR حساس باشند، اما انواع فاکتورهای رونویسی در ژنوم انسان بسیار بیشتر از انواع STR هستند. هورتون گفت: جهش یک توالی STR ممکن است بر اتصال 20 فاکتور رونویسی مختلف در آن نوع سلول تأثیر بگذارد و منجر به کاهش کلی رونویسی آن ژن مجاور بدون دخالت هیچ عامل رونویسی خاصی شود.
بنابراین در واقع، تیم استنفورد با Tjian موافق است که تنظیم ژن در سلولهای زنده توسط یک مکانیسم ساده و ساده انجام نمیشود. در عوض، عوامل رونویسی، مکانهای اتصال DNA آنها و سایر مولکولهای تنظیمی ممکن است در تجمعات متراکمی جمع شوند که تأثیر خود را به طور جمعی اعمال میکنند.
در حال حاضر نمونههای متعددی وجود دارد که از این ایده حمایت میکند که عناصر DNA میتوانند فاکتورهای رونویسی را تا حدی جمع کنند که با کوفاکتورها متراکم شوند. ریچارد یانگ، زیست شناس سلولی در موسسه وایتهد موسسه فناوری ماساچوست. تقویت کننده ها بسیاری از فاکتورهای رونویسی را برای ایجاد آن شلوغی متصل می کنند. STR ها ممکن است عنصری باشند که به جمع آوری فاکتورهای رونویسی برای جمع شدن در نزدیکی یک ژن کمک می کند، اما آنها تمام ماجرا نیستند.
چرا به جای تکیه بر نوع تعاملات قوی و خاص بین پروتئین های تنظیم کننده و سایت های DNA که در پروکاریوت ها غالب هستند، ژن ها را به این شیوه پیچیده تنظیم کنیم؟ ممکن است چنین ابهامی همان چیزی باشد که متازوئن های پیچیده بزرگ را ممکن کرده است.
برای اینکه موجودات زنده باشند، باید بتوانند تکامل یافته و با شرایط متغیر سازگار شوند. اگر سلولهای ما به شبکهای عظیم و در عین حال کاملاً تجویز شده از فعل و انفعالات تنظیمکننده ژن متکی باشند، ایجاد هر گونه تغییر در آن بدون برهم زدن کل ساختار دشوار خواهد بود، همانطور که یک ساعت سوئیسی در صورت حذف (یا حتی کمی جابهجا کردن) هر یک را از بین میبرد. از هزاران چرخ دنده آن با این حال، اگر برهمکنشهای مولکولی تنظیمی شل و نسبتاً نامشخص باشند، سستی مفیدی در سیستم وجود دارد - همانطور که یک کمیته معمولاً میتواند تصمیم خوبی بگیرد حتی اگر یکی از اعضای آن بیمار باشد.
فوردایس خاطرنشان میکند که در پروکاریوتهایی مانند باکتریها، یافتن مکانهای اتصال خود برای فاکتورهای رونویسی ممکن است نسبتاً آسان باشد زیرا ژنوم مورد جستجو کوچکتر است. اما با بزرگتر شدن ژنوم این کار سخت تر می شود. فوردایس گفت: در ژنوم بزرگ یوکاریوتها، «دیگر نمیتوانید این خطر را تحمل کنید که به طور موقت در یک محل اتصال «اشتباه» گیر کنید، زیرا این کار توانایی واکنش سریع به شرایط محیطی در حال تغییر را به خطر میاندازد.
علاوه بر این، STR ها خود بسیار قابل تکامل هستند. طولانی شدن یا کوتاه شدن توالی آنها، یا تغییر در اندازه و عمق "چاه فاکتور رونویسی"، می تواند به راحتی از طریق اشتباهات در همانندسازی یا ترمیم DNA، یا از طریق بازترکیب جنسی کروموزوم ها رخ دهد. به فوردایس، پیشنهاد میکند که STRها «بنابراین ممکن است به عنوان ماده خام برای تکامل عناصر نظارتی جدید و تنظیم دقیق ماژولهای نظارتی موجود برای برنامههای رونویسی حساس، مانند برنامههایی که توسعه حیوانات و گیاهان را کنترل میکنند، عمل کنند.
قدرت تعاملات ضعیف
چنین ملاحظاتی باعث می شود که زیست شناسان مولکولی توجه بیشتری به برهمکنش های ضعیف و نسبتاً غیرانتخابی در ژنوم داشته باشند. بسیاری از این ها شامل پروتئین هایی می شوند که به جای داشتن ساختار ثابت و دقیق، شل و فلاپی هستند - همانطور که بیوشیمی دانان می گویند "ذاتاً بی نظم هستند". یانگ توضیح داد که اگر پروتئینها فقط از طریق حوزههای ساختاری سفت و سخت کار کنند، نه تنها چگونگی تکامل سیستمهای تنظیمی بلکه انواع تنظیم دینامیکی که در زندگی مشاهده میشود را نیز محدود میکند. یانگ گفت: "شما یک موجود زنده - یا حتی یک ویروس - را پیدا نخواهید کرد که فقط با عناصر ساختاری پایدار مانند عناصر موجود در ساعت سوئیسی کار کند."
شاید تکامل فقط به STR ها به عنوان یک جزء از چنین راه حل پیچیده اما در نهایت موثرتر برای تنظیم ژن در یوکاریوت ها برخورد کرده است. خود STR ها ممکن است به روش های مختلفی ایجاد شوند - به عنوان مثال، از طریق خطا در همانندسازی DNA یا فعالیت بخش های DNA به نام عناصر قابل انتقال که از خود در سراسر ژنوم کپی می کنند.
کولمن گفت: «این اتفاق افتاد که برهمکنشهای ضعیف بین پروتئینها و توالیهای تکراری چیزی بود که میتوانست برای سلولهایی که در آن رخ میداد مزیت انتخابی ایجاد کند.» حدس او این است که احتمالاً این ابهام بر یوکاریوت ها تحمیل شده است، اما «آنها متعاقباً توانستند از [آن] به نفع خود بهره برداری کنند». باکتریها و سایر پروکاریوتها میتوانند به منطق تنظیمکننده «دیجیتال» کاملاً تعریفشده تکیه کنند، زیرا سلولهای آنها تنها در چند حالت ساده و متمایز وجود دارند، مانند حرکت در اطراف و تکثیر.
اما ساتر گفت، حالات سلولی مختلف برای متازوئهها «بسیار پیچیدهتر و گاهی نزدیک به یک پیوستار» هستند، بنابراین با تنظیم «آنالوگ» فازیتر، بهتر عمل میکنند.
Tjian موافق است: "به نظر می رسد که سیستم های تنظیم کننده ژن در باکتری ها و یوکاریوت ها به طور قابل توجهی از هم جدا شده اند." در حالی که گفته می شود مونود یک بار اظهار داشت که «در مورد چه چیزی صادق است باکتری E. coli برای فیل درست است.» به نظر می رسد که همیشه اینطور نیست.
- محتوای مبتنی بر SEO و توزیع روابط عمومی. امروز تقویت شوید.
- PlatoData.Network Vertical Generative Ai. به خودت قدرت بده دسترسی به اینجا.
- PlatoAiStream. هوش وب 3 دانش تقویت شده دسترسی به اینجا.
- PlatoESG. کربن ، CleanTech، انرژی، محیط، خورشیدی، مدیریت پسماند دسترسی به اینجا.
- PlatoHealth. هوش بیوتکنولوژی و آزمایشات بالینی. دسترسی به اینجا.
- منبع: https://www.quantamagazine.org/a-lobby-where-a-molecule-mob-tells-genes-what-to-do-20240214/
- : دارد
- :است
- :نه
- :جایی که
- ][پ
- $UP
- 000
- 20
- 70
- a
- توانایی
- قادر
- درباره ما
- غایب
- فراوان
- جمع آوری شده
- عمل
- بازیگری
- عمل
- فعال کردن
- فعالیت
- اعمال
- وفق دادن
- اضافه کردن
- اضافه
- مجاور
- مزیت - فایده - سود - منفعت
- اثر
- قرابت
- از نو
- موافقت کرد
- موافق است
- الگوریتم
- معرفی
- تنها
- در امتداد
- همچنین
- هر چند
- همیشه
- در میان
- تقویت
- an
- و
- حیوانات
- دیگر
- هر
- جدا
- هستند
- استدلال
- بوجود می آیند
- دور و بر
- مقاله
- AS
- ظاهر
- فرض
- At
- توجه
- نویسنده
- خودکار
- دور
- به عقب
- باکتری
- پایه
- BE
- زیرا
- شدن
- بوده
- شروع
- بودن
- سود
- برکلی
- بهترین
- بهتر
- میان
- بزرگ
- تصویر بزرگ
- بزرگتر
- بزرگترین
- اتصال
- الزام آور
- زیست شناسی
- مسدود کردن
- بلاک ها
- فوت
- بالا بردن
- هر دو
- آورده
- اما
- by
- کالیفرنیا
- نام
- آمد
- CAN
- سلول
- سلول ها
- معین
- چالش ها
- تبادل
- متغیر
- انتخاب
- کروموزوم
- موقعیت
- کلاسیک
- طبقه بندی کنید
- واضح
- به وضوح
- نزدیک
- نزدیک
- خوشه
- همکاری
- همکاران
- مجموعا
- ترکیب
- ترکیب
- بیا
- کمیسیون
- مشترک
- مقایسه
- پیچیده
- بغرنج
- جزء
- سازش
- شرایط
- اتصالات
- ملاحظات
- محتوا
- زنجیره
- کنترل
- گروه شاهد
- گفتگو
- تعاونی
- میتوانست
- زن و شوهر
- جمعیت
- دهه
- تصمیم گیری
- تصمیم
- تصمیم گیری
- رمز گشایی
- کاهش
- بستگی دارد
- بستگی دارد
- عمق
- جزئیات
- دقیق
- پروژه
- متفاوت است
- تفاوت
- مختلف
- مشکل
- انتشار
- دیجیتال
- مد دیجیتال
- مستقیما
- کشف
- مرض
- متمایز
- مختلف
- DNA
- do
- بارانداز
- نمی کند
- حوزه
- تسلط داشتن
- آیا
- رانده
- دوبله شده
- در طی
- پویا
- در اوایل
- به آسانی
- ساده
- اثر
- موثر
- اثرات
- هر دو
- عناصر
- فیل
- در جای دیگر
- ظهور
- بالا بردن
- محیطی
- خطاهای
- حتی
- هر
- مدرک
- تکامل
- تکامل یابد
- در حال تحول
- کاملا
- مثال
- مثال ها
- وجود داشته باشد
- موجود
- انتظار
- آزمایش
- توضیح داده شده
- بهره برداری
- بیان
- خیلی
- واقعیت
- عامل
- عوامل
- روش
- فدرال
- کمی از
- رشته
- شکل گرفت
- پیدا کردن
- نام خانوادگی
- مناسب
- ثابت
- برای
- مجبور
- فرم
- یافت
- فرانسوی
- از جانب
- تابعی
- عملکرد
- توابع
- گروه
- جمع آوری
- جمع آوری
- اجتماعات
- عموما
- ژنومیک
- دریافت کنید
- می شود
- داده
- هدف
- رفتن
- خوب
- حکومت داری
- بزرگ
- گروه
- حدس
- نیم
- دسته
- اتفاق افتاده است
- سخت
- سخت تر
- آیا
- داشتن
- he
- کمک می کند
- او
- خیلی
- خود را
- نگه داشتن
- چگونه
- اما
- HTML
- HTTPS
- بزرگ
- انسان
- انسان
- اندیشه
- شناسایی
- if
- تأثیر
- in
- از جمله
- در واقع
- فرد
- نفوذ
- تأثیرگذار
- اطلاعات
- ناچیز
- در عوض
- موسسه
- تعامل
- تعامل
- فعل و انفعالات
- به
- معرفی
- همیشه
- شامل
- گرفتار
- شامل
- IT
- ITS
- خود
- یعقوب
- اره منبت کاری اره مویی
- کار
- تنها
- نگاه داشتن
- نگهداری
- نوع
- انواع
- دانا
- آزمایشگاه
- بزرگ
- نام
- برجسته
- یادگیری
- رهبری
- کمتر
- زندگی
- پسندیدن
- احتمالا
- مرتبط
- کوچک
- زندگی
- منطق
- طولانی
- دیگر
- نگاه
- دستگاه
- فراگیری ماشین
- ساخته
- مجله
- عمده
- ساخت
- باعث می شود
- روش
- بسیاری
- ماساچوست
- موسسه تکنولوژی ماساچوست
- مسابقه
- ماده
- از نظر ریاضی
- ماده
- ممکن است..
- شاید
- معنی دار
- اندازه
- اندازه گیری
- مکانیزم
- مکانیسم
- پزشکی
- جلسات
- اعضا
- روش
- قدرت
- MIT
- حالت
- ماژول ها
- مولکولی
- مولکول
- بیش
- حرکت
- متحرک
- بسیار
- چندگانه
- باید
- بی شمار
- مرموز
- راز
- طبیعت
- نزدیک
- تقریبا
- لزوما
- نیاز
- ضروری
- شبکه
- نه
- یادداشت
- اکنون
- ظریف
- متعدد
- رخ می دهد
- رخ داده است
- اتفاق می افتد
- of
- خاموش
- ارائه
- غالبا
- on
- یک بار
- ONE
- فقط
- or
- دیگر
- ما
- خارج
- نتیجه
- روی
- به طور کلی
- خود
- بسته بندی شده
- جفت شدن
- جفت
- مقاله
- پارامترهای
- بخش
- شرکت کنندگان
- ویژه
- گذشته
- پچ های
- پرداخت
- شاید
- متقاعد شد
- فیزیکی
- تصویر
- قطعات
- گیاهان
- افلاطون
- هوش داده افلاطون
- PlatoData
- بازی
- بازیکنان
- نقطه
- موقعیت
- ممکن
- قدرت
- قوی
- دقیق
- پیش بینی
- پیش بینی
- حضور
- در حال حاضر
- غرور
- شاید
- روش
- روند
- تولید کردن
- محصول
- عمیق
- برنامه ها
- پروژه
- پروتئين
- پروتئین ها
- ارائه
- فراهم می کند
- اثبات كردن
- منتشر شده
- قرار دادن
- پازل
- سوال
- به سرعت
- کاملا
- تصادفی
- نرخ
- نسبتا
- خام
- به راحتی
- اماده
- واقعی
- منطقه
- مناطق
- تنظیم کردن
- تنظیم
- تنظیم کننده
- نسبتا
- منتشر شد
- تکیه
- تکیه بر
- ماندن
- اظهار داشت
- برداشتن
- تعمیر
- تکراری
- تکرار
- محققان
- قابل احترام
- پاسخ
- نتیجه
- نتیجه
- نتایج
- برنج
- غنی
- راست
- سفت و محکم
- خطر
- کنار رودخانه
- RNA
- نقش
- اتاق
- به طور معمول
- دویدن
- سعید
- همان
- گفتن
- دانشمندان
- ایمن
- دیدن
- به نظر می رسد
- ظاهرا
- به نظر می رسد
- مشاهده گردید
- بخش
- بخش ها
- تصاحب کردن
- انتخابی
- حساس
- جمله
- سپتامبر
- دنباله
- خدمت
- خدمت کرده است
- چند
- جنسی
- کم عمق
- شکل
- کوتاه
- باید
- نشان
- اهمیت
- ساده
- پس از
- تنها
- سایت
- سایت
- شش
- اندازه
- شل
- کوچکتر
- So
- راه حل
- برخی از
- به نحوی
- چیزی
- گاهی
- منابع
- فضا
- خاص
- اختصاصی
- پایدار
- استنفورد
- دانشگاه استنفورد
- ایالات
- آماری
- ماندن
- گام
- چسبیده
- چسبنده
- توقف
- داستان
- ساده
- استحکام
- قوی
- به شدت
- ساختاری
- ساختار
- دانشجو
- مهاجرت تحصیلی
- متعاقبا
- قابل ملاحظه ای
- چنین
- قند
- حاکی از
- دنباله
- پشتیبانی
- مطمئن
- اطراف
- سویسی
- گزینه
- سویس
- سیستم
- سیستم های
- گرفتن
- پشت سر هم
- هدف
- اهداف
- کار
- تیم
- پیشرفته
- می گوید
- تمایل
- ده ها
- نسبت به
- که
- La
- شان
- آنها
- خودشان
- سپس
- آنجا.
- از این رو
- اینها
- آنها
- اشیاء
- فکر می کنم
- فکر می کند
- این
- کسانی که
- اگر چه؟
- فکر
- هزاران نفر
- از طریق
- سراسر
- بدین ترتیب
- محکم
- زمان
- بار
- به
- با هم
- هم
- ترجمه
- شفاف
- به دام انداختن
- درست
- عطف
- دو
- نوع
- انواع
- به طور معمول
- ukr
- در نهایت
- کشف
- فهمیدن
- دانشگاه
- دانشگاه کالیفرنیا
- ناشناخته
- بر
- استفاده کنید
- استفاده
- مفید
- معمولا
- ارزشها
- مختلف
- وسیع
- بسیار
- قابل اعتماد
- ویروس
- صدا
- منتظر
- بود
- تماشا کردن
- آب
- مسیر..
- راه
- we
- ضعیف
- وب سایت
- خوب
- به خوبی تعریف شده است
- ولز
- بود
- چی
- چه زمانی
- چه
- که
- در حین
- WHO
- تمام
- کاملا
- چرا
- اراده
- با
- در داخل
- بدون
- مهاجرت کاری
- مشغول به کار
- جهان
- کرم
- خواهد بود
- کتبی
- نوشت
- هنوز
- شما
- جوان
- زفیرنت