بیماریهای تخریبکننده عصبی، که با از دست دادن تدریجی عملکرد مغز مشخص میشوند، عمدتاً از از دست دادن سیناپسی و مرگ سلولهای عصبی در سیستم عصبی مرکزی ناشی میشوند. آلزایمر بیماری (AD) مسلماً شایع ترین اختلال عصبی است که منجر به زوال عقل می شود.
کاستی های درمان نشان می دهد که دانشمندان هرگز به طور کامل درک نکرده اند که آلزایمر چگونه ایجاد می شود. دانشمندان همچنین نمی دانند که چرا زنان تقریباً دو سوم موارد را تشکیل می دهند.
محققان در MIT و تحقیقات Scripps اشاره ای به اتیولوژی مولکولی بیماری آلزایمر کشف کرده اند. این سرنخ همچنین ممکن است توضیح دهد که چرا زنان بیشتر مستعد ابتلا به این بیماری هستند.
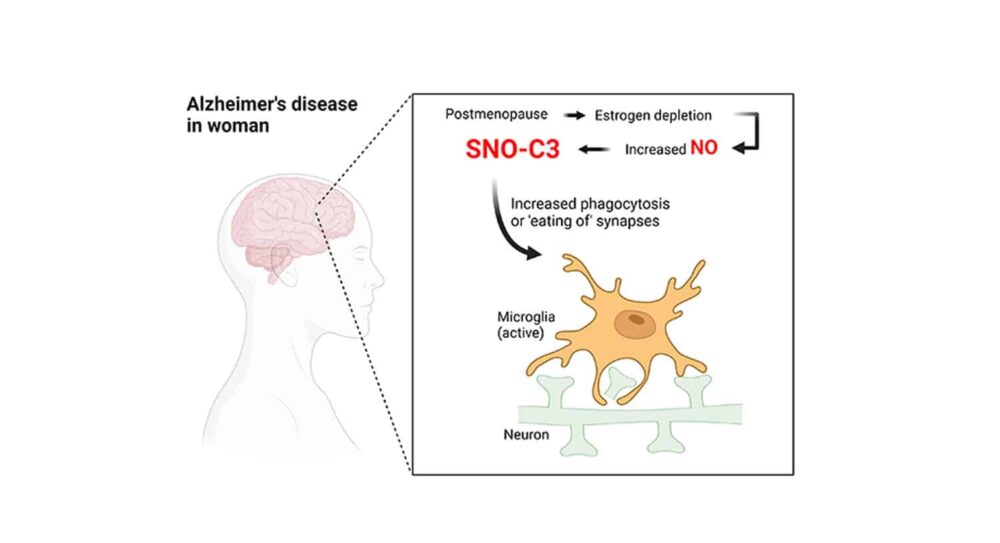
محققان کشف کردند که شکل مخصوصاً مضر و اصلاح شده شیمیایی یک پروتئین ایمنی التهابی به نام مکمل C3 در مغز زنانی که بر اثر این بیماری جان خود را از دست داده بودند در مقایسه با مردانی که بر اثر این بیماری مرده بودند، در سطوح بسیار بالاتری وجود دارد. آنها هم این را نشان دادند استروژن- که در طول تولید کاهش می یابد يائسگي- معمولاً در برابر ایجاد این شکل از مکمل C3 محافظت می کند.
نویسنده ارشد این مطالعه استوارت لیپتون، دکترا، دکترا، استاد و رئیس بنیاد استپ خانواده در بخش پزشکی مولکولی در تحقیقات اسکریپس و یک متخصص مغز و اعصاب بالینی در لا جولا، کالیفرنیا، گفت: یافتههای جدید ما نشان میدهد که اصلاح شیمیایی یک جزء از سیستم کمپلمان به ایجاد آلزایمر کمک میکند و ممکن است حداقل تا حدودی توضیح دهد که چرا این بیماری عمدتاً زنان را تحت تأثیر قرار میدهد.
آزمایشگاه لیپتون فرآیندهای بیوشیمیایی و مولکولی مانند پروتئین S-nitrosylation را بررسی می کند که منجر به یک نسخه اصلاح شده از مکمل C3 می شود که ممکن است علت آن باشد. اختلالات نوروژنیک. این فرآیند شیمیایی، که زمانی که یک مولکول مرتبط با اکسید نیتریک (NO) به طور ایمن به یک اتم گوگرد (S) روی یک واحد ساختمانی اسید آمینه خاص از پروتئین میچسبد، یک «پروتئین SNO» اصلاحشده تولید میکند، اولین بار توسط لیپتون و همکارانش پیدا شد. .
خوشه های کوچک اتم، مانند NO، اغلب تغییر می کنند پروتئین ها در سلول ها. این تغییرات معمولاً عملکرد پروتئین هدف را فعال یا غیرفعال می کند. به دلیل مشکلات فنی، S-nitrosylation کمتر از سایر اصلاحات پروتئین مورد توجه قرار گرفته است. با این حال، لیپتون فرض میکند که «طوفانهای SNO» این پروتئینها ممکن است نقش مهمی در ایجاد بیماری آلزایمر و سایر بیماریهای تخریبکننده عصبی داشته باشند.
آزمایشگاه لیپتون فرآیندهای بیوشیمیایی و مولکولی مانند پروتئین S-nitrosylation را بررسی می کند که منجر به یک نسخه اصلاح شده از مکمل C3 می شود که ممکن است علت اختلالات عصبی باشد. این فرآیند شیمیایی، که زمانی که یک مولکول مرتبط با اکسید نیتریک (NO) به طور ایمن به یک اتم گوگرد (S) روی یک واحد ساختمانی اسید آمینه خاص از پروتئین میچسبد، یک «پروتئین SNO» اصلاحشده تولید میکند، اولین بار توسط لیپتون و همکارانش پیدا شد. .
خوشههای کوچک اتمها، مانند NO، اغلب پروتئینها را در سلولها تغییر میدهند. این تغییرات معمولاً عملکرد پروتئین هدف را فعال یا غیرفعال می کند. به دلیل مشکلات فنی، S-nitrosylation کمتر از سایر اصلاحات پروتئین مورد توجه قرار گرفته است. با این حال، لیپتون فرض میکند که «طوفانهای SNO» این پروتئینها ممکن است نقش مهمی در ایجاد بیماری آلزایمر و سایر بیماریهای تخریبکننده عصبی داشته باشند.
در جدیدترین مطالعه، دانشمندان با استفاده از تکنیکهای کاملاً جدید برای شناسایی S-nitrosylation، میزان پروتئینهای تغییر یافته را در 40 مغز انسان پس از مرگ اندازهگیری کردند. مغزها به طور مساوی بین مردان و زنان تقسیم شده بود، نیمی از افرادی که بر اثر بیماری آلزایمر مرده بودند و نیمی دیگر از افرادی بود که به بیماری آلزایمر مرده بودند.
محققان 1,449 پروتئین مجزا را کشف کردند که در این مغزها S-nitrosylated شده بودند. پروتئینهای متعددی که قبلاً با بیماری آلزایمر مرتبط بودهاند، از جمله پروتئینهایی بودند که اغلب تغییر میکردند، از جمله مکمل C3. با کمال تعجب، مغز آلزایمر زنان دارای سطوح C3 نیتروسیله S (SNO-C3) بود که بیش از شش برابر بیشتر از مغز آلزایمر مردان بود.
سیستم مکمل از نظر تکاملی بخش قدیمیتری از انسان است سیستم ایمنی بدن. این شامل خانواده ای از پروتئین ها، از جمله C3 است که می توانند یکدیگر را برای تحریک التهاب در "آبشار مکمل" فعال کنند.
برای بیش از 30 سال، محققان میدانستند که در مقایسه با مغزهای سالم از نظر عصبی، مغز آلزایمر مقادیر بیشتری از پروتئینهای مکمل و سایر شاخصهای التهابی را نشان میدهد. مطالعات جدیدتر به ویژه نشان داده است که چگونه پروتئین های مکمل می توانند باعث شوند سلول های ایمنی مقیم مغز به نام میکروگلیا سیناپس ها را تخریب کنند. در این تقاطع ها، نورون ها با یکدیگر ارتباط برقرار می کنند.
اکنون بسیاری از محققان بر این باورند که این مکانیسم تخریب سیناپس تا حدی زمینه ساز بیماری آلزایمر است. ثابت شده است که از دست دادن سیناپس ها ارتباط قابل توجهی با کاهش شناختی در مغز آلزایمر دارد.
چرا مغز زنان مبتلا به آلزایمر شیوع بیشتری از SNO-C3 دارد؟ محققان این فرضیه را مطرح کردند که استروژن از مغز زنان در برابر نیتروزیلاسیون C3 S محافظت می کند و این محافظت زمانی که سطح استروژن به شدت با یائسگی کاهش می یابد از بین می رود. مدتهاست شواهدی وجود دارد که هورمون زنانه استروژن میتواند تحت برخی شرایط اثرات محافظتی بر مغز داشته باشد. این نظریه با آزمایش هایی با استفاده از انسان پرورش یافته تأیید شد سلول های مغزکه نشان داد SNO-C3 با کاهش سطح استروژن (-استرادیول) به دلیل فعال کردن آنزیمی که NO در سلولهای مغزی تولید میکند، افزایش مییابد. سیناپس ها با افزایش سطح SNO-C3 توسط میکروگلیا از بین می روند.
لیپتون می گوید:, اینکه چرا زنان بیشتر به آلزایمر مبتلا میشوند مدتها یک راز بوده است، اما من فکر میکنم نتایج ما نشاندهنده بخش مهمی از پازل است که به طور مکانیکی افزایش آسیبپذیری زنان را با افزایش سن توضیح میدهد.
مرجع مجله:
- هونگمی یانگ، چانگ کی اوه، و همکاران. بینش مکانیکی در مورد غلبه زنان در بیماری آلزایمر بر اساس پروتئین S-nitrosylation نابجا C3. با پیشرفتهای علمیبه DOI: 10.1126/sciadv.ade0764