Loppuvaiheen munuaissairaus, jolloin munuaiset eivät enää pysty vastaamaan elimistön tarpeisiin, hoidetaan parhaiten munuaisensiirrolla. Luovuttajien tarjonta on kuitenkin rajallista, ja monien potilaiden on turvauduttava sen sijaan dialyysiin. Ja vaikka munuaisensiirto tarjoaa erinomaisia tuloksia, se vaatii potilaan elinikäistä immunosuppressiolääkkeitä, jotka aiheuttavat hänen omia terveysongelmiaan. Näiden ongelmien ratkaisemiseksi tutkijat toivovat kehittävänsä implantoitavan biokeinotekoisen munuaisen munuaisten vajaatoiminnan hoitoon.
UC San Franciscon (UCSF) tutkijat työskentelevät luodakseen tällaisen laitteen. Heidän uusimmassa tutkimuksessaan, joka raportoi vuonna Luonto Viestintä, ne osoittavat, että implantoitavassa bioreaktorissa sijaitsevat munuaissolut voivat selviytyä sian sisällä ja jäljitellä useita tärkeitä munuaistoimintoja. Ratkaisevaa on, että istutettu laite ei aiheuttanut immuunireaktiota. Tutkimus on osa MunuaisprojektiUCSF:n yhdessä johtamana Shuvo Roy ja William Fissell Vanderbilt University Medical Centeristä.
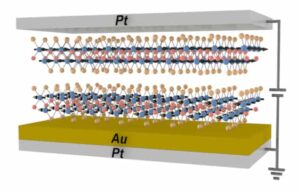
Ensimmäisenä askeleena kohti implantoitavaa biokeinotekoista munuaista Roy, Fissel ja kollegat loivat soluja sisältävän bioreaktorin, joka toistaa munuaistiehyen tärkeimmät toiminnot, joihin kuuluu hapen ja ravinteiden toimittaminen munuaissoluihin samalla kun ne suojelevat niitä vastaanottajan immuunisoluilta, jotka voivat aiheuttaa hyljintäreaktion. . Tämän immunosuojauksen saavuttamiseksi ryhmä suunnitteli ohuen (alle 1 μm) piinanohuokoskalvon (SNM) piikiekoista, jotka sisälsivät nanomittakaavan rakoisia huokosia.
Tutkijat rakensivat prototyypin bioreaktorin, joka sisälsi SNM:n, jossa on 10 nm:n leveät huokoset, ja ihmisen munuaisepiteelisoluja (HREC) viljeltiin akryyliinserteillä SNM:n kummallakin puolella. Testaa, tarjoaako SNM immunosuojaavan esteen vitro, he altistivat SNM:n yhden puolen tulehdusta edistävälle sytokiinille TNF-α.
Kuusi tuntia altistuksen jälkeen TNF-α:n tasot SNM:n suojaamassa osastossa olivat mitättömät, mikä osoittaa, että 10 nm:n leveät huokoset estävät suurten sytokiinien (ja siten myös suurempien immuunijärjestelmän komponenttien, kuten T-solujen ja vasta-aineiden) kulkeutumisen. . Suoraan TNF-a:lle altistetun puolen solujen elinkelpoisuus oli alle 50 %, kun taas SNM:llä suljetuilla soluilla oli korkea, lähes 90 % elinkelpoisuus.
On myös tärkeää, että implantti ei aiheuta verihyytymiä, jotka voivat muodostua veren kanssa kosketuksiin joutuville pinnoille ja johtaa laitteen vioittumiseen ja vakaviin komplikaatioihin potilaalle. Tämän välttämiseksi tutkijat käyttivät laskennallista nestedynamiikkaa optimoidakseen U-muotoisen verenvirtauspolun geometrian bioreaktorin läpi.
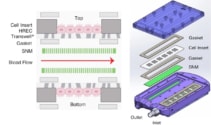
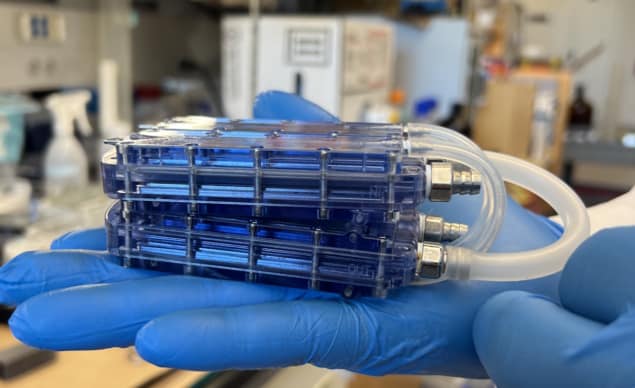
He käyttivät tätä mallia luodakseen implantoitavan bioreaktorin, joka sisälsi neljä SNM:ää polykarbonaattikotelossa, linjassa verikanavien ylä- ja alapinnan kanssa. He asettivat akryylisisäkkeet, joihin oli ympätty yhtyviä HREC:itä kunkin SNM:n vastakkaisille puolille, ja käyttivät ruostumattomasta teräksestä valmistettuja liittimiä veren siirtämiseen SNM:iden ja PTFE-vaskulaaristen siirteiden välillä.
Näiden bioreaktoriprototyyppien biologisen yhteensopivuuden testaamiseksi ryhmä kokosi ja istutti kirurgisesti laitteita viiteen terveeseen porsaan, jotka käyttivät kaksoisverihiutalehoitoa (ilman immunosuppressiota). Bioreaktorit yhdistettiin eläinten verisuoniin PTFE-siirteiden kautta. Laitteisiin tai leikkaukseen liittyviä komplikaatioita ei esiintynyt, ja eläimet pysyivät terveinä kolmen tai seitsemän päivän kokeiden ajan (aika, jolloin hyperakuutti hyljintä tyypillisesti tapahtui), ilman merkkejä hylkimisestä.
Tutkijat arvioivat, aiheuttiko ksenogeenisiä ihmissoluja sisältävien bioreaktorien istuttaminen immuunireaktion sioissa. 13 yleisen tulehduksellisen biomarkkerin tutkiminen paljasti joidenkin sytokiinien lisääntymisen kaksi päivää implantoinnin jälkeen, kuten odotettiin postoperatiivisen tulehduksen vuoksi. Mutta seitsemän päivää implantoinnin jälkeen kaikki sytokiinitasot olivat laskeneet minimaalisen tulehduksen tilaan. Tämä havainto on päinvastainen voimakkaalle vasteelle, jota odotetaan tyypillisessä ksenograftimallissa, jossa on immunokompetentti vastaanottaja.
OCT voisi auttaa laajentamaan munuaisten luovuttajapoolia
Kolmen tai seitsemän päivän kuluttua tutkijat poistivat bioreaktorit eläimistä arviointia varten. He havaitsivat, että eksplantoitu SNM oli ehjä, solujen ja proteiinien kiinnittyminen oli minimaalista eikä laitteeseen muodostunut verihyytymiä. Tämä on tärkeä askel sen turvallisuuden osoittamisessa. Lisäksi kapseloidut HREC-solut säilyivät yli 90-prosenttisesti elävinä ilman todisteita solujen irtoamisesta ja tiukkojen solujen välisten liitosten ylläpidosta.
"Meidän piti todistaa, että toimiva bioreaktori ei vaadi immunosuppressiivisia lääkkeitä, ja teimme sen", Roy sanoo tiedotteessa. "Meillä ei ollut komplikaatioita, ja nyt voimme toistaa koko munuaistoimintojen paneelin ihmisen mittakaavassa."
- SEO-pohjainen sisällön ja PR-jakelu. Vahvista jo tänään.
- PlatoData.Network Vertical Generatiivinen Ai. Vahvista itseäsi. Pääsy tästä.
- PlatoAiStream. Web3 Intelligence. Tietoa laajennettu. Pääsy tästä.
- PlatoESG. Autot / sähköautot, hiili, CleanTech, energia, ympäristö, Aurinko, Jätehuolto. Pääsy tästä.
- PlatonHealth. Biotekniikan ja kliinisten kokeiden älykkyys. Pääsy tästä.
- ChartPrime. Nosta kaupankäyntipeliäsi ChartPrimen avulla. Pääsy tästä.
- BlockOffsets. Ympäristövastuun omistuksen nykyaikaistaminen. Pääsy tästä.
- Lähde: https://physicsworld.com/a/implantable-bioartificial-kidney-aims-to-free-patients-from-dialysis/
- :On
- :ei
- $ YLÖS
- 1
- 10
- 125
- 13
- a
- Saavuttaa
- Lisäksi
- osoite
- Jälkeen
- tavoitteet
- linjassa
- Kaikki
- Myös
- an
- ja
- eläimet
- OVAT
- AS
- koolla
- At
- välttää
- este
- PARAS
- välillä
- veri
- pohja
- rakennettu
- mutta
- by
- CAN
- Aiheuttaa
- Solut
- keskus
- kanavat
- napsauttaa
- työtovereiden
- Yhteinen
- täydellinen
- osat
- käsittää
- yhtyviä
- kytketty
- ottaa yhteyttä
- sisältää
- kontrasti
- voisi
- luoda
- luotu
- ratkaisevasti
- päivää
- vähentynyt
- tuottaa
- osoittaa
- esittelyssä
- Malli
- kehittää
- laite
- Laitteet
- dialyysi
- DID
- ohjata
- suoraan
- Sairaus
- Lääkäri
- ei
- Huumeet
- kaksi
- aikana
- dynamiikka
- kukin
- myöskään
- Työllisiä
- kapseloitu
- arvioitu
- arviointi
- näyttö
- tutkii
- erinomainen
- Laajentaa
- odotettu
- kokeiluja
- avoin
- Valotus
- Epäonnistuminen
- löytäminen
- viisi
- virtaus
- neste
- Neste dynamiikkaa
- varten
- muoto
- muodostivat
- löytyi
- neljä
- Francisco
- Ilmainen
- alkaen
- toiminnallinen
- tehtävät
- HAD
- headed
- terveys
- terve
- auttaa
- Korkea
- pito
- toivoen
- TUNTIA
- kotelo
- Kuitenkin
- HTTPS
- ihmisen
- kuva
- Immuunijärjestelmä
- tärkeä
- in
- sisältää
- Kasvaa
- tiedot
- ensimmäinen
- insertit
- sisällä
- sen sijaan
- tulee
- kysymys
- kysymykset
- IT
- SEN
- jpg
- avain
- munuainen
- munuaiset
- suuri
- suurempi
- uusin
- johtaa
- vasemmalle
- vähemmän
- tasot
- rajallinen
- kauemmin
- huolto
- monet
- max-width
- lääketieteellinen
- minimi
- malli
- lisää
- täytyy
- nanohuokoset
- luonto
- lähes
- tarvitaan
- tarpeet
- Uusi
- Nro
- nyt
- tapahtui
- of
- on
- ONE
- avata
- päinvastainen
- Optimoida
- or
- tuloksiin
- oma
- Happi
- paneeli
- osa
- kulku
- polku
- potilas
- potilaat
- Fysiikka
- Fysiikan maailma
- Platon
- Platonin tietotieto
- PlatonData
- painaa
- estää
- projekti
- suojattu
- suojella
- Proteiini
- prototyyppi
- prototyyppejä
- todistaa
- tarjoaa
- päästäisiin
- reaktio
- liittyvä
- luottaa
- pysyi
- poistettu
- munuais-
- rinnakkaista
- raportoitu
- edellyttää
- Vaatii
- tutkimus
- Tutkijat
- vastaus
- Revealed
- oikein
- roy
- Turvallisuus
- San
- San Francisco
- sanoo
- Asteikko
- Osa
- osiot
- vakava
- seitsemän
- useat
- puoli
- Sides
- merkki
- Pii
- jonkin verran
- Osavaltio
- Lausunto
- Vaihe
- tutkimus
- Onnistuneesti
- niin
- toimittaa
- tuki
- Leikkaus
- hengissä
- järjestelmä
- T-solut
- ottaa
- joukkue-
- testi
- testattu
- kuin
- että
- -
- heidän
- Niitä
- Nämä
- ne
- tätä
- ne
- vaikka?
- kolmella
- kauttaaltaan
- thumbnail
- Näin
- aika
- että
- ylin
- kohti
- siirtyminen
- siirto
- kohdella
- käsittelemällä
- hoito
- totta
- kaksi
- tyypillinen
- tyypillisesti
- yliopisto
- käytetty
- kautta
- kannattavuus
- kannattava
- oli
- we
- olivat
- kun
- onko
- joka
- vaikka
- koko
- tulee
- with
- ilman
- työskentely
- maailman-
- olisi
- zephyrnet