L’imagerie par résonance magnétique (IRM) est une technique d’imagerie médicale courante dans les hôpitaux du monde entier et que beaucoup d’entre nous connaîtront à un moment donné de leur vie. La technique non invasive identifie les tissus malades en détectant les différences de morphologie des tissus sur la base des différents temps de relaxation du tissu après exposition à des impulsions RF dans un champ magnétique. La résonance magnétique peut également être utilisée comme mécanisme de mesure fondamental pour d’autres types de scanners d’imagerie médicale.
Il existe un intérêt pour la création d'appareils portables au point d'intervention (POC) capables d'imager les tissus mous, tout comme une IRM. De tels systèmes pourraient détecter rapidement des anévrismes ou des poches de liquide, par exemple, sans qu'il soit nécessaire de transporter les patients vers des établissements de soins centralisés pour effectuer des procédures d'IRM. La capacité de fournir ces informations diagnostiques au chevet du patient avec un appareil portable pourrait améliorer les résultats pour les patients, réduire le temps de traitement des patients et réduire les coûts de diagnostic pour les établissements de santé.
L'IRM elle-même est cependant trop volumineuse pour une imagerie au chevet du patient et ne convient pas aux patients porteurs de certains implants métalliques. De plus, les besoins en énergie de l’IRM dépassent de loin les capacités énergétiques d’un scanner portable, tout comme le poids de l’équipement.
Ces défis liés au transfert des capacités d’IRM vers les appareils POC ont conduit les chercheurs à développer de nouveaux dispositifs de capteurs basés sur la résonance magnétique. L’un de ces développements a été réalisé par des chercheurs du Massachusetts Institute of Technology et de l’Université Harvard. "Notre étude clinique précédente a révélé que le liquide interstitiel des muscles squelettiques est un réservoir important de liquide dans le corps", auteur principal Michael Cima raconte Monde de la physique. "Nous avions besoin d'un modèle magnétique capable de mesurer ce volume au chevet d'un patient."
Analyse POC du tissu musculaire
Cima et ses collègues ont choisi de créer un dispositif POC utilisant un capteur de résonance magnétique simple face (SSMR) à faible champ pour examiner les muscles squelettiques in vivo. Comparé à un équipement IRM standard, le système est beaucoup plus portable avec un poids de seulement 11 kg. Les capteurs SSMR utilisent la puissance du contraste basé sur la résonance magnétique pour acquérir des données spectroscopiques (sans imagerie) sur une profondeur tissulaire limitée et fournir des informations sur la structure des différents types de tissus, permettant ainsi de les distinguer les uns des autres.
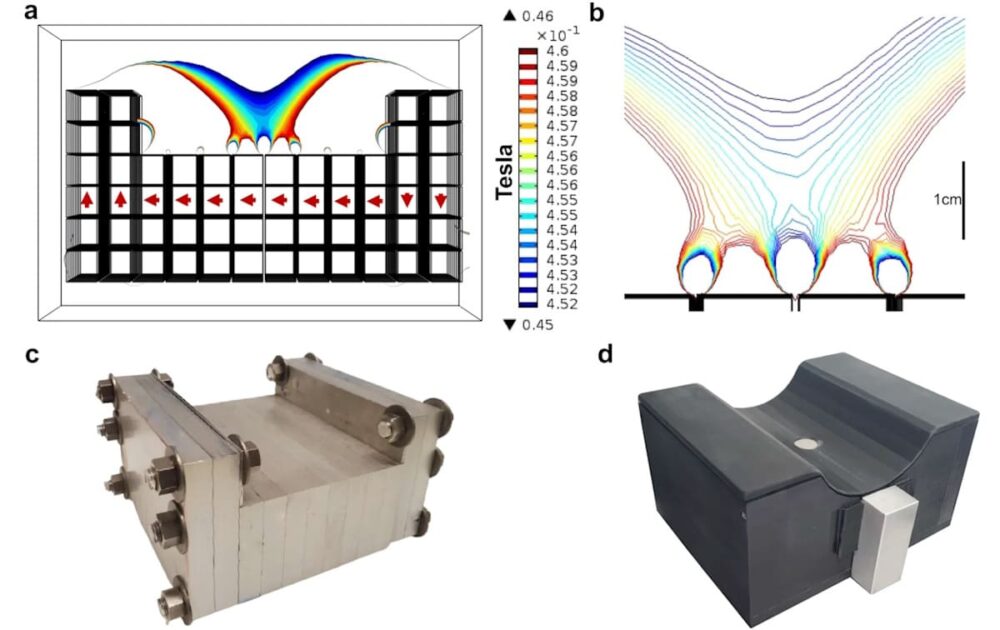
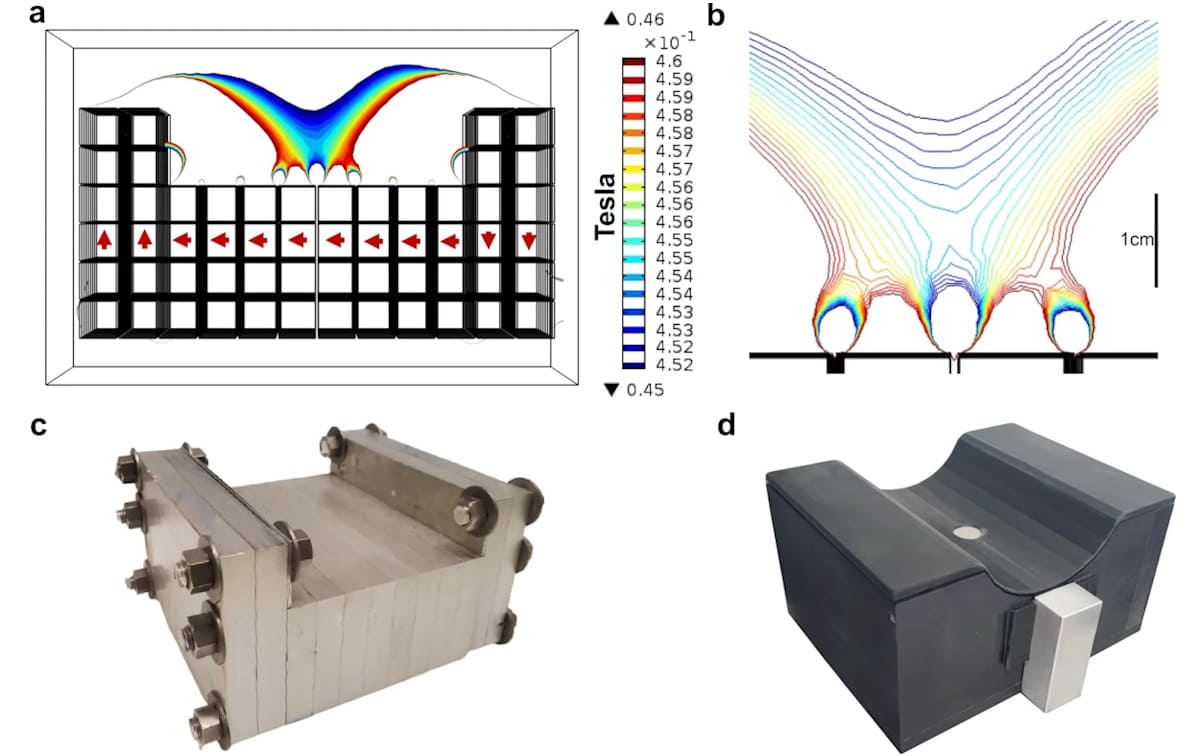
Le capteur portable utilise un réseau d'aimants permanents et une bobine RF de surface pour fournir une faible puissance opérationnelle et des exigences de blindage minimales. Le réseau magnétique, construit à partir de 12.7 mm3 Les aimants en néodyme déployés dans des cadres en aluminium sont conçus pour asseoir confortablement les muscles du mollet. Le capteur entièrement assemblé avec boîtier Delrin mesure 22 × 17.4 x 11 cm.
Le capteur peut capturer des mesures diagnostiques à faible bruit en quelques minutes, y compris des données de relaxation T2, qui peuvent fournir un aperçu de l'état des fluides, de la cinétique vasculaire et de l'oxygénation du tissu musculaire squelettique, entre autres applications. La surchauffe des tissus est évitée en enfermant la bobine dans du nitrure d'aluminium, qui possède une conductivité thermique élevée capable de dissiper la chaleur générée. Tous ces aspects se combinent pour rendre le capteur SSMR adapté à une utilisation comme dispositif POC.
Les chercheurs ont testé le capteur à la fois in vitro ainsi que le in vivo, y compris une étude clinique sur des humains en bonne santé pour déterminer si l’appareil pouvait détecter avec succès les tissus musculaires – ce qu’il a fait. Par rapport aux tentatives précédentes visant à créer des capteurs SSMR similaires pour les applications POC, les appareils de Cima et de son équipe présentent une meilleure sensibilité et des profondeurs de pénétration plus grandes, et sont plus sûrs pour une utilisation clinique.

Un capteur MR portable diagnostique la déshydratation
Le nouveau capteur a une profondeur de pénétration supérieure à 8 mm, surpassant les autres systèmes décrits dans la littérature, limités à une profondeur inférieure à 6 mm. L'analyse à ces niveaux a permis une évaluation précise du tissu musculaire tout en évitant les signaux provenant d'autres couches sous-cutanées, telles que le tissu adipeux (graisse sous la peau) qui se trouve plus près de la surface de la peau.
Les résultats les plus importants de cette étude, selon Cima, sont que « la conception de l'aimant répondait aux spécifications de performances requises et est maintenant utilisée dans un essai portant sur 90 patients avec des patients rénaux en phase terminale ». Interrogé sur le potentiel futur de ces dispositifs, Cima déclare que « la valeur clinique de cette technologie sera démontrée si nous pouvons montrer qu'elle prédit le « poids sec » [poids normal sans excès de liquide dans le corps] des maladies rénales terminales. les patients. Il n’existe actuellement aucun moyen cliniquement accepté de le faire.
La recherche est publiée dans Communications Nature.
- Contenu propulsé par le référencement et distribution de relations publiques. Soyez amplifié aujourd'hui.
- PlatoData.Network Ai générative verticale. Autonomisez-vous. Accéder ici.
- PlatoAiStream. Intelligence Web3. Connaissance Amplifiée. Accéder ici.
- PlatonESG. Carbone, Technologie propre, Énergie, Environnement, Solaire, La gestion des déchets. Accéder ici.
- PlatoHealth. Veille biotechnologique et essais cliniques. Accéder ici.
- La source: https://physicsworld.com/a/single-sided-mr-sensor-provides-tissue-analysis-at-the-patient-bedside/
- :possède
- :est
- :ne pas
- 10
- 11
- 12
- 17
- 22
- 7
- 8
- a
- capacité
- A Propos
- accepté
- Avec cette connaissance vient le pouvoir de prendre
- acquérir
- Après
- Tous
- permis
- Permettre
- aussi
- parmi
- an
- selon une analyse de l’Université de Princeton
- ainsi que le
- Une autre
- applications
- SONT
- autour
- tableau
- AS
- aspects
- assemblé
- At
- Tentatives
- auteur
- évité
- en évitant
- basé
- BE
- va
- Améliorée
- corps
- tous les deux
- by
- CAN
- capacités
- capturer
- les soins
- centralisée
- certaines
- globaux
- choisir
- cliquez
- Infos sur les
- plus
- bobine
- collègues
- combiner
- comment
- Commun
- par rapport
- construit
- contraste
- Costs
- pourriez
- engendrent
- La création
- Lecture
- données
- démontré
- déployé
- profondeur
- Profondeurs
- décrit
- Conception
- un
- détecter
- Déterminer
- développer
- Développement
- dispositif
- Compatibles
- diagnostique
- DID
- différences
- différent
- Distingué
- do
- pendant
- l'équipements
- évaluation
- exemple
- excès
- existe
- d'experience
- Exposition
- installations
- loin
- Lipides
- champ
- fluide
- Pour
- trouvé
- De
- d’étiquettes électroniques entièrement
- fondamental
- avenir
- généré
- plus grand
- harvard
- Harvard University
- Vous avez
- la médecine
- la santé
- Haute
- sa
- les hôpitaux
- Cependant
- HTTPS
- Les êtres humains
- identifie
- if
- image
- Imagerie
- important
- améliorer
- in
- Y compris
- indiquer
- d'information
- perspicacité
- Institut
- intérêt
- développement
- aide
- IT
- lui-même
- jpg
- juste
- plus importantes
- poules pondeuses
- conduire
- LED
- moins
- niveaux
- se trouve
- comme
- limité
- littérature
- Style
- Faible
- baisser
- réseau d'aimants
- Champ magnétique
- Aimants
- a prendre une
- de nombreuses
- Massachusetts
- Massachusetts Institute of Technology
- assorti
- largeur maximale
- mesurer
- mesures
- des mesures
- les mesures
- mécanisme
- médical
- la ficelle d'étiquettes/étiquettes volantes en carton
- Métal
- minimal
- Minutes
- MIT
- PLUS
- Par ailleurs
- (en fait, presque toutes)
- mr
- MRI
- beaucoup
- Nature
- nécessaire
- besoin
- réseau et
- Nouveauté
- aucune
- Ordinaire
- maintenant
- of
- on
- ONE
- uniquement
- ouvert
- opérationnel
- or
- Autre
- nos
- les résultats
- surperformant
- plus de
- patientforward
- patients
- pénétration
- Effectuer
- performant
- permanent
- Physique
- Monde de la physique
- Platon
- Intelligence des données Platon
- PlatonDonnées
- PoC
- les poches
- Point
- portable
- défaillances
- power
- Prévoit
- représentent
- précédent
- procédures
- Profil
- fournir
- fournit
- publié
- rapidement
- Rouge
- réduire
- détente
- rénal
- conditions
- Exigences
- un article
- chercheurs
- résonance
- Révélé
- plus sûre
- dit
- balayage
- Sensibilité
- capteur
- capteur
- montrer
- signaux
- similaires
- Peau
- Soft
- quelques
- quelque chose
- caractéristiques
- Standard
- Statut
- structure
- Étude
- Avec succès
- tel
- convient
- Surface
- combustion propre
- Système
- équipe
- technique
- Technologie
- raconte
- examiné
- que
- qui
- La
- El futuro
- le monde
- Les
- thermique
- Ces
- this
- thumbnail
- fiable
- fois
- à
- trop
- Transfert
- transport
- traiter
- procès
- oui
- types
- sous
- université
- us
- utilisé
- d'utiliser
- Usages
- en utilisant
- Plus-value
- le volume
- Façon..
- we
- poids
- ont été
- quand
- que
- qui
- tout en
- WHO
- sera
- comprenant
- dans les
- sans
- world
- X
- zéphyrnet