L'insuffisance rénale terminale, lorsque les reins ne peuvent plus répondre aux besoins de l'organisme, est mieux traitée par transplantation rénale. Cependant, l’approvisionnement en organes donneurs est limité et de nombreux patients doivent plutôt recourir à la dialyse. Et même si une greffe de rein donne d’excellents résultats, elle oblige le patient à prendre des médicaments immunosuppresseurs à vie, ce qui entraîne des complications pour sa santé. Pour résoudre ces problèmes, les chercheurs espèrent développer un rein bioartificiel implantable pour traiter l’insuffisance rénale.
Des chercheurs de l'UC San Francisco (UCSF) travaillent à la création d'un tel appareil. Dans leur dernière étude, rapportée dans Communications Nature, ils démontrent que les cellules rénales hébergées dans un bioréacteur implantable pourraient survivre à l’intérieur d’un porc et imiter plusieurs fonctions rénales importantes. Surtout, le dispositif implanté n’a pas provoqué de réaction immunitaire. La recherche fait partie de Le projet Rein, dirigé conjointement par l'UCSF Chouvo Roy et de William Fissell du centre médical de l'université Vanderbilt.
Comme première étape vers un rein bioartificiel implantable, Roy, Fissel et leurs collègues ont créé un bioréacteur contenant des cellules qui reproduit les fonctions clés du tubule rénal, notamment l'apport d'oxygène et de nutriments aux cellules rénales tout en les protégeant des cellules immunitaires du receveur qui pourraient provoquer un rejet. . Pour obtenir cette immunoprotection, l’équipe a conçu une fine membrane nanopore de silicium (SNM) à partir de tranches de silicium contenant des pores fendus à l’échelle nanométrique.
Les chercheurs ont construit un prototype de bioréacteur abritant un SNM doté de pores de 10 nm de large, avec des cellules épithéliales rénales humaines (HREC) cultivées sur des inserts acryliques de chaque côté du SNM. Pour tester si le SNM fournit une barrière immunoprotectrice in vitro, ils ont exposé un côté du SNM à la cytokine pro-inflammatoire TNF-α.
Six heures après l'exposition, les niveaux de TNF-α dans le compartiment protégé par le SNM étaient négligeables, démontrant que les pores de 10 nm de large empêchent le passage des grosses cytokines (et donc également des composants plus importants du système immunitaire tels que les lymphocytes T et les anticorps). . Les cellules du côté directement exposé au TNF-α avaient une viabilité inférieure à 50 %, tandis que celles scellées par le SNM maintenaient une viabilité élevée de près de 90 %.
Il est également important qu'un implant ne provoque pas de caillots sanguins, qui peuvent se former sur les surfaces en contact avec le sang et entraîner une défaillance du dispositif et des complications graves pour le patient. Pour éviter cela, les chercheurs ont utilisé la dynamique des fluides computationnelle pour optimiser la géométrie du trajet du flux sanguin en forme de U à travers le bioréacteur.
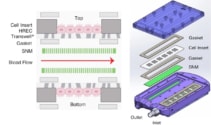
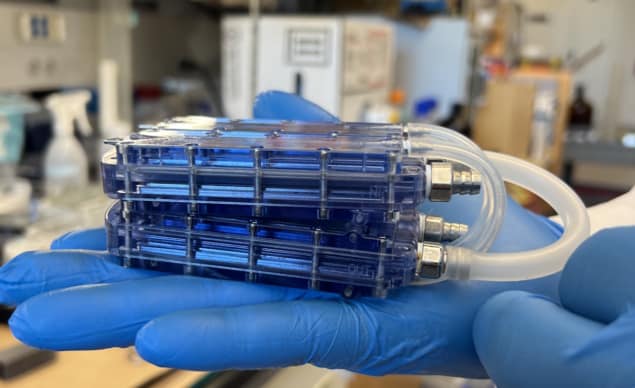
Ils ont utilisé cette conception pour créer un bioréacteur implantable contenant quatre SNM dans un boîtier en polycarbonate, aligné avec les surfaces supérieure et inférieure des canaux sanguins. Ils ont placé des inserts en acrylique ensemencés de HREC confluents sur les côtés opposés de chaque SNM et ont utilisé des connecteurs en acier inoxydable pour faire passer le sang entre les SNM et les greffons vasculaires en PTFE.
Pour tester la biocompatibilité de ces prototypes de bioréacteurs, l’équipe a assemblé et implanté chirurgicalement des dispositifs chez cinq porcs sains sous double thérapie antiplaquettaire (sans immunosuppression). Les bioréacteurs connectés au système vasculaire des animaux via les greffons PTFE. Aucune complication liée aux dispositifs ou à la chirurgie n'est survenue et les animaux sont restés en bonne santé tout au long des expériences de trois ou sept jours (période pendant laquelle un rejet hyperaigu se produirait généralement), sans aucun signe de rejet.
Les chercheurs ont évalué si l'implantation de bioréacteurs contenant des cellules humaines xénogéniques provoquait une réaction immunitaire chez les porcs. L'examen de 13 biomarqueurs inflammatoires courants a révélé une augmentation de certaines cytokines deux jours après l'implantation, comme prévu en raison d'une inflammation postopératoire. Mais sept jours après l’implantation, tous les niveaux de cytokines avaient diminué jusqu’à un état d’inflammation minime. Cette découverte contraste avec la réponse vigoureuse attendue dans un modèle typique de xénogreffe avec un receveur immunocompétent.
L'OCT pourrait aider à élargir le bassin de donneurs de rein
Après trois ou sept jours, les chercheurs ont retiré les bioréacteurs des animaux pour évaluation. Ils ont constaté que le SNM explanté était intact, avec un minimum d’attachement de cellules et de protéines et aucun caillot sanguin ne s’est formé dans le dispositif – une étape importante pour démontrer sa sécurité. De plus, les cellules HREC encapsulées sont restées viables à plus de 90 %, sans aucune preuve de détachement cellulaire ni de maintien de jonctions intercellulaires serrées.
"Nous devions prouver qu'un bioréacteur fonctionnel ne nécessiterait pas de médicaments immunosuppresseurs, et nous l'avons fait", a déclaré Roy dans un communiqué de presse. "Nous n'avons eu aucune complication et pouvons désormais itérer, atteignant l'ensemble des fonctions rénales à l'échelle humaine."
- Contenu propulsé par le référencement et distribution de relations publiques. Soyez amplifié aujourd'hui.
- PlatoData.Network Ai générative verticale. Autonomisez-vous. Accéder ici.
- PlatoAiStream. Intelligence Web3. Connaissance Amplifiée. Accéder ici.
- PlatonESG. Automobile / VE, Carbone, Technologie propre, Énergie, Environnement, Solaire, La gestion des déchets. Accéder ici.
- PlatoHealth. Veille biotechnologique et essais cliniques. Accéder ici.
- GraphiquePrime. Élevez votre jeu de trading avec ChartPrime. Accéder ici.
- Décalages de bloc. Modernisation de la propriété des compensations environnementales. Accéder ici.
- La source: https://physicsworld.com/a/implantable-bioartificial-kidney-aims-to-free-patients-from-dialysis/
- :est
- :ne pas
- $UP
- 1
- 10
- 125
- 13
- a
- atteindre
- ajout
- propos
- Après
- vise
- aligné
- Tous
- aussi
- an
- et de
- animaux
- SONT
- AS
- assemblé
- At
- éviter
- une barrière
- LES MEILLEURS
- jusqu'à XNUMX fois
- sang
- Bas et Leggings
- construit
- mais
- by
- CAN
- Causes
- Cellules
- Canaux centraux
- Canaux de vente
- cliquez
- collègues
- Commun
- complet
- composants électriques
- comprend
- ConFluent™
- connecté
- contact
- contient
- contraste
- pourriez
- engendrent
- créée
- de manière cruciale
- jours
- diminué
- livrer
- démontrer
- démontrer
- Conception
- développer
- dispositif
- Compatibles
- dialyse
- DID
- directement
- Maladie
- Docteur
- Médicaments
- deux
- pendant
- dynamique
- chacun
- non plus
- employés
- encapsulé
- évalué
- évaluation
- preuve
- Examiner
- excellent
- Développer vous
- attendu
- expériences
- exposé
- Exposition
- Échec
- trouver
- cinq
- flux
- fluide
- dynamique des fluides
- Pour
- formulaire
- formé
- trouvé
- quatre
- Francisco
- gratuitement ici
- De
- fonctionnel
- fonctions
- ait eu
- à tête
- Santé
- la santé
- aider
- Haute
- tenue
- en espérant
- HEURES
- logement
- Cependant
- HTTPS
- humain
- image
- Système immunitaire
- important
- in
- inclut
- Améliore
- d'information
- initiale
- Inserts
- à l'intérieur
- plutôt ;
- développement
- aide
- vous aider à faire face aux problèmes qui vous perturbent
- IT
- SES
- jpg
- ACTIVITES
- un rein
- reins
- gros
- plus importantes
- Nouveautés
- conduire
- à gauche
- moins
- niveaux
- limité
- plus long
- facile
- de nombreuses
- largeur maximale
- médical
- minimal
- modèle
- PLUS
- must
- nanopore
- Nature
- presque
- nécessaire
- Besoins
- Nouveauté
- aucune
- maintenant
- a eu lieu
- of
- on
- ONE
- ouvert
- opposé
- Optimiser
- or
- les résultats
- propre
- Oxygène
- panneau
- partie
- passage
- chemin
- patientforward
- patients
- Physique
- Monde de la physique
- Platon
- Intelligence des données Platon
- PlatonDonnées
- Press
- empêcher
- Projet
- protégé
- L'utilisation de sélénite dans un espace est un excellent moyen de neutraliser l'énergie instable ou négative.
- Protéines
- prototype
- prototypes
- Prouver
- fournit
- atteindre
- réaction
- en relation
- compter
- resté
- Supprimé
- rénal
- réplique
- Signalé
- exigent
- a besoin
- un article
- chercheurs
- réponse
- Révélé
- bon
- roy
- Sécurité
- San
- San Francisco
- dit
- Escaliers intérieurs
- Section
- les sections
- grave
- sept
- plusieurs
- côté
- Accompagnements
- signer
- Silicium
- quelques
- Région
- Déclaration
- étapes
- Étude
- Avec succès
- tel
- la quantité
- Support
- #
- survivre
- combustion propre
- Les cellules T
- Prenez
- équipe
- tester
- examiné
- que
- qui
- La
- leur
- Les
- Ces
- l'ont
- this
- ceux
- bien que?
- trois
- tout au long de
- thumbnail
- Ainsi
- fiable
- à
- top
- vers
- transition
- transplantation
- traiter
- traitement
- traitement
- oui
- deux
- débutante
- typiquement
- université
- d'utiliser
- via
- viabilité
- viable
- était
- we
- ont été
- quand
- que
- qui
- tout en
- la totalité
- sera
- comprenant
- sans
- de travail
- world
- pourra
- zéphyrnet