La thermoradiothérapie est un traitement anticancéreux dans lequel l'hyperthermie - chauffer la tumeur au-dessus de la température corporelle - est utilisée pour améliorer l'efficacité de la radiothérapie. Le montant de cette amélioration est exprimé en EQDRT, la dose de rayonnement équivalente nécessaire pour obtenir le même effet thérapeutique sans chauffage.
Des essais cliniques ont montré que cette approche peut améliorer considérablement les résultats du traitement dans plusieurs types de tumeurs, sans augmenter la toxicité des tissus normaux. Des études antérieures ont également démontré que la température atteinte et l'intervalle de temps entre la radiothérapie et l'hyperthermie ont un impact sur le résultat clinique.
Pour comprendre ce processus plus en détail et aider à optimiser les traitements, les chercheurs de UMC d'Amsterdam ont utilisé la modélisation biologique pour étudier l'impact de la température maximale et de l'intervalle de temps sur l'EQDRT. Décrivant leurs découvertes dans le Journal international de radio-oncologie Biologie Physique, ils rapportent que des températures élevées et des intervalles de temps courts sont essentiels pour maximiser l'amélioration thérapeutique.
Modèle biologique
Pour effectuer la thermoradiothérapie, les cliniciens utilisent un appareil de radiofréquence ou de micro-ondes pour appliquer de la chaleur sur la tumeur une ou deux fois par semaine, avant ou après une séance de radiothérapie. La température de la tumeur est maintenue en dessous de 45°C pour éviter de chauffer les tissus normaux, mais des points chauds parfois indésirables (et douloureux) peuvent se produire, ce qui limite le niveau de puissance maximal tolérable pouvant être utilisé lors d'un traitement d'hyperthermie.
Premier auteur Pétra Kok et ses collègues ont développé un logiciel pour modéliser les effets biologiques de la radiothérapie plus l'hyperthermie en termes de distributions de doses équivalentes. Le modèle, qui tient compte de l'inhibition de la réparation de l'ADN par hyperthermie, ainsi que de la cytotoxicité induite par la chaleur directe, permet d'évaluer la qualité des plans de traitement combinés à l'aide d'histogrammes dose-volume standard.
Pour obtenir un aperçu de base de l'impact des paramètres d'hyperthermie, l'équipe a d'abord calculé l'amélioration d'une distribution de dose standard de 23 × 2 Gy par des températures homogènes comprises entre 37 et 43 °C, pour des intervalles de temps compris entre 0 et 4 h.
Le modèle a montré que EQDRT augmenté de manière significative avec l'augmentation de la température et la diminution de l'intervalle de temps. Pour un intervalle de temps de 1 h, par exemple, il a prédit un EQDRT augmentation de 2 à 15 Gy pour des températures de 39 à 43 °C. Ces résultats soulignent l'importance d'atteindre la température tumorale tolérable la plus élevée pour optimiser les résultats cliniques.
L'impact de l'intervalle de temps était le plus prononcé à des températures plus élevées (supérieures à 41 °C). A une température hyperthermique typique de 41.5°C, un EQDRT une augmentation d'environ 10 Gy a été obtenue avec un intervalle de temps de 0 h. Cela a diminué à environ 4 Gy d'amélioration avec un intervalle de 4 h, indiquant qu'à mesure que l'intervalle de temps augmente, une température plus élevée est nécessaire pour obtenir le même effet.
Cas cliniques
Ensuite, les chercheurs ont évalué des scénarios de traitement réalistes basés sur des distributions de température inhomogènes et des plans de radiothérapie clinique. Ils ont calculé l'EQDRT pour 10 patientes atteintes d'un cancer du col de l'utérus localement avancé. Tous les patients avaient reçu une arcthérapie volumétrique modulée (VMAT) de 23 × 2 Gy, avec une hyperthermie appliquée chaque semaine pendant le traitement.
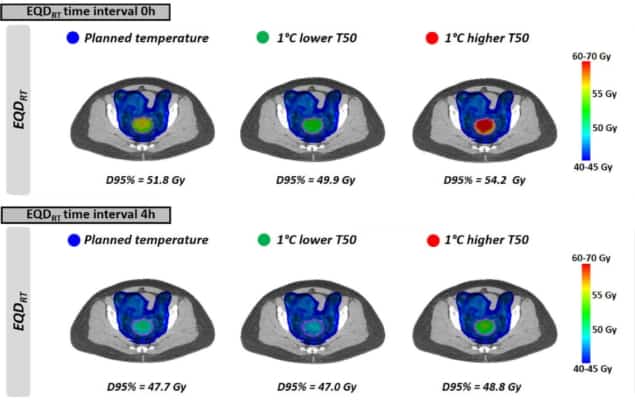
Comme on le voit avec les températures uniformes, EQDRT était le plus grand pour le plus petit intervalle de temps. Lorsque l'hyperthermie a été appliquée immédiatement avant ou après la radiothérapie (intervalle de temps de 0 h), l'EQD moyenRT à 95 % du volume (D95 %) était de 51.7 Gy, soit un gain de 6.3 Gy par rapport au rayonnement seul. L'augmentation de l'intervalle de temps à 4 h réduit ce gain à 2.2 Gy.
Le modèle a prédit que la majeure partie de l'amélioration de la dose est perdue au cours de la première heure. Pour une utilisation clinique, par conséquent, le temps entre la radiothérapie et l'administration de l'hyperthermie doit être aussi court que possible - idéalement par des patients recevant les deux traitements dans le même hôpital. L'équipe note que si l'ordre des deux traitements n'est pas cliniquement pertinent, car il faut du temps pour réchauffer la tumeur, l'application préalable de l'hyperthermie pourrait permettre des intervalles de temps significativement plus courts, même proches de 0 h.
Enfin, les chercheurs ont modélisé l'impact de l'obtention de températures tumorales légèrement inférieures à celles prévues, en raison de l'apparition de points chauds limitant le traitement. L'effet sur l'EQDRT était le plus prononcé pendant un court intervalle de temps entre la radiothérapie et l'hyperthermie. Pour une température inférieure de 1°C et un intervalle de temps de 0 h, par exemple, la moyenne prédite EQDRT(D95 %) diminué de 1.8 Gy (de 51.7 à 49.9 Gy) ; pour un intervalle de 4 h, la diminution était d'environ 0.7 Gy.
La radiothérapie est plus efficace dans les tumeurs réchauffées
Dans les cas où aucun point chaud n'apparaît, il peut être possible d'augmenter la puissance de sortie et d'atteindre une température plus élevée que prévu. Une fois de plus, l'avantage d'atteindre une température plus élevée était plus grand pour des intervalles de temps plus courts, le gain exact dépendant des températures réelles atteintes.
"La modélisation biologique fournit des informations pertinentes sur la relation entre les paramètres de traitement et l'EQD attenduRT», concluent Kok et ses collègues. "Des températures élevées et des intervalles de temps courts sont essentiels pour maximiser l'EQDRT.