空間トランスクリプトミクスとプロテオミクスは、複雑な生物学的プロセスの理解を変える補完的な情報を提供します。ただし、これらのモダリティの実験的な統合には制限があります。
Spatial PrOtein and Transcriptome Sequencing (SPOTS) と呼ばれる新しい方法は、器官または腫瘍全体の細胞の正体と活動を前例のない解像度で明らかにすることができます。の研究者によって開発されました。 ウィルコーネル医学、ニューヨーク長老派教会、およびニューヨークゲノムセンターの共同研究により、SPOTS は臓器や腫瘍全体の細胞の正体と活動を前例のない解像度で明らかにすることができます。
この技術は、遺伝子活性のパターンや必須物質の存在を記録しながら、細胞の正確な位置に関する情報を保存します。 タンパク質 組織サンプル全体の細胞内で。これにより、病気の臓器や腫瘍を含む臓器の複雑でデータが豊富な「マップ」を作成することが可能になり、基礎研究と臨床研究の両方で非常に役立つ可能性があります。
研究の共同上級著者であるダン・ランドー博士は、血液学・腫瘍内科の准教授であり、ワイル・コーネル医科大学のサンドラ・エドワード・マイヤーがんセンターのメンバーであり、ニューヨークゲノムセンターの中心教員でもある。言った、 「この技術は、細胞の種類、細胞活動、細胞間の相互作用など、組織の空間構成をこれまでにない方法でマッピングできるため、興味深いものです。」
この新しいアプローチは、臓器や組織がどのように機能するかを顕微鏡レベルで「見る」ためのより効果的な手段を作成する科学者や技術者による大規模な取り組みの一部です。近年、研究、特に単一細胞または小グループの遺伝子活性およびその他のデータ層をプロファイリングする方法において、顕著な進歩が見られます。 細胞。ただし、これらのアプローチでは組織を破壊し、隣接する細胞から細胞を分離することが頻繁に必要となるため、組織内のプロファイリングされた細胞の元の配置に関する情報を回復する必要があります。新しい技術はその空間データも記録し、優れた解像度で記録します。
このメソッドは、既存の 10x Genomics テクノロジーに部分的に基づいています。通常の顕微鏡ベースの病理学法で組織サンプルを画像化するのに適したスライドガラスを使用しますが、何千もの特定のプローブ分子でコーティングされています。
各プローブ分子の化学「バーコード」は、スライド上のその二次元位置を識別します。スライド上のプローブ分子は、 メッセンジャーRNA 薄くスライスされた組織サンプルがスライド上に置かれると、その細胞は透過性になります。この手順ではデザイナー抗体が使用され、組織内の目的の固有のプローブ分子およびタンパク質に結合します。
研究者は、収集した mRNA と選択したタンパク質を迅速かつ自動的に特定し、組織サンプル全体の元の位置にそれらを正確にマッピングできます。作成されたマップは、独立して検討することも、サンプルの日常的な病理イメージングと比較して検討することもできます。
研究チームは、健康なマウスの脾臓から採取した組織で、SPOTSを使用して、さまざまな種類の細胞のクラスター、その機能状態、細胞の配置に応じてそれらの状態がどのように変化するのかなど、この臓器の複雑な機能構造を示した。
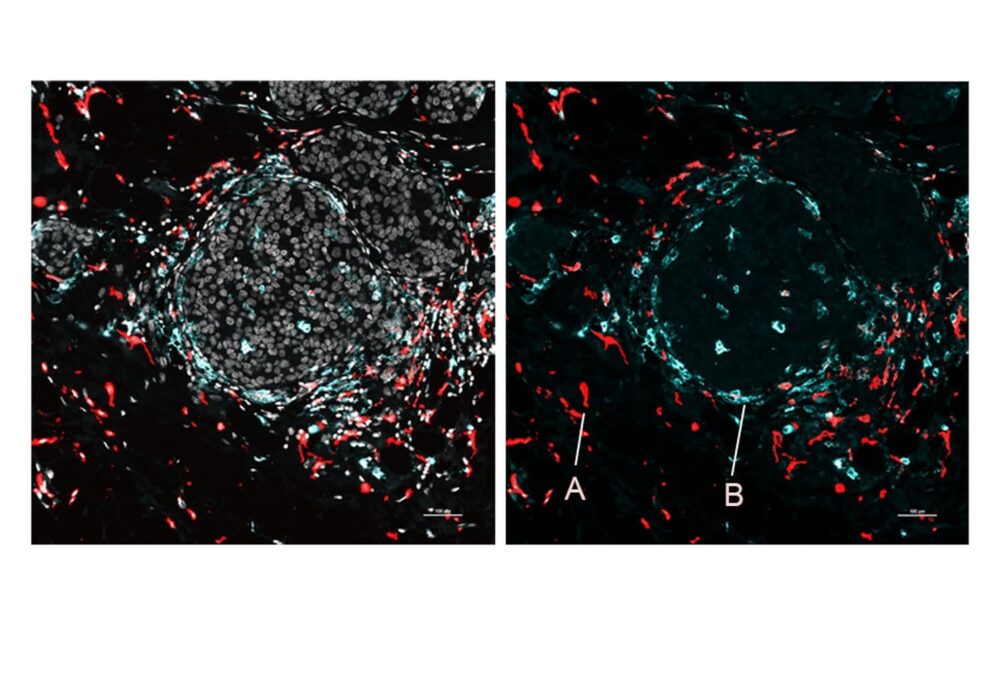
研究者らはまた、SPOTS を利用してマウス乳房腫瘍の細胞構造をマッピングし、次の分野での使用の可能性を強調しました。 がん研究。生成されたマップは、マクロファージと免疫細胞が 2 つの異なる状態にあることを示し、それぞれが異なるタンパク質マーカーによって示されました。1 つの状態は活動状態で腫瘍と闘っていて、もう 1 つは免疫抑制状態で腫瘍を遮蔽するバリアを確立していました。
ニューヨーク長老派教会/ワイル・コーネル医療センターの腫瘍学者であるランドー博士は、 と, 「これら 2 つのマクロファージ サブセットが腫瘍の異なる領域に存在し、異なる細胞と相互作用していることがわかりました。そして、微小環境の違いがそれらの異なる活動状態を引き起こしている可能性があります。」
「腫瘍の免疫環境のこのような詳細は、腫瘍内の免疫細胞がまばらであるために解決できないことが多い詳細ですが、一部の患者がなぜ免疫環境に反応するのかを説明するのに役立つかもしれません。」 免疫増強療法 そうでないものもあり、したがって将来の免疫療法の設計に情報を与える可能性があります。」
「SPOTS のこの初期バージョンは、結果として得られるデータセットの各「ピクセル」が少なくともいくつかの細胞の遺伝子活性情報を合計するような空間解像度を備えています。しかし、研究者らは、重要な細胞情報の他の層を追加しながら、すぐにこの解像度を単一細胞に絞り込むことを望んでいます。」
ジャーナルリファレンス:
- Ben-Chetrit、N.、Niu、X.、Swett、AD 他。トランスクリプトーム全体の空間プロファイリングとタンパク質マーカーの統合。 ネイチャーバイオテクノロジー (2023)。 DOI: 10.1038/s41587-022-01536-3