Partikkelterapi – kreftbehandling ved bruk av stråler av protoner eller tyngre ioner – gir svært konform dosetilførsel og større sparing av normalt vev enn konvensjonell fotonbasert strålebehandling. Men for langsiktige kreftoverlevere er risikoen for strålingsindusert sekundær kreft (SC) viktig, og bør vurderes når de velger behandlingsmetode.
Med knappe epidemiologiske data for nyere behandlinger som proton- og karbonionterapi, ledet et team opp ved GSI Helmholtz Center for Heavy Ion Research utvikler en modell for å sammenligne SC-risikoen mellom partikkelterapimodaliteter. Modellen, beskrevet av Antonia Hufnagl og kolleger i Medisinsk fysikk, kan til slutt bli inkorporert i behandlingsplanleggingssystemer for å inkludere SC-risiko som et ekstra optimaliseringskriterium.
Dødelige versus kreftfremkallende hendelser
SC-risikomodeller fungerer vanligvis ved å vurdere balansen mellom celledrap (som fører til kreftundertrykkelse) og celletransformasjon (induksjon av mutasjoner som til slutt fører til kreft). Sannsynligheten for at et bestrålt volum vil utvikle kreft er definert ved hjelp av den lineær-kvadratiske (LQ) modellen, som gir et enkelt forhold mellom celleoverlevelse og levert fotondose.
I denne studien brukte forskerne den lokale effektmodellen (LEM) for å forutsi den relative biologiske effektiviteten (RBE) av SC-induksjon etter partikkelterapi. For å gjøre rede for den økte RBE av partikkelstråling, erstattet de foton-LQ-parametrene i risikomodellen med ionestråle-LQ-parametere forutsagt av LEM. Et nøkkeltrekk ved deres tilnærming er bruken av LEM både når det gjelder celledrap og kreftinduksjon.

"Den doble bruken av LEM reflekterer konkurransen mellom de to hovedprosessene som bestemmer utviklingen av SC, nemlig celletransformasjon og celledrap," forklarer seniorforfatter Michael Scholz. "Med økende dose og/eller effektivitet kan celledrap undertrykke levedyktigheten til transformerte celler. Dette fører til et komplekst samspill, som ikke bare kan reflekteres ellers i en ett-trinns prosedyre.»
For å undersøke hvilke faktorer som påvirker SC-risiko, brukte forskerne planleggingssystemet TPS TRiP98 for å generere biologisk optimaliserte karbonion- og protonbehandlingsplaner basert på en idealisert geometri. Planene bestrålte et 4x4x4 cm mål med en enkelt partikkelstråle eller to motstående stråler, med et 4x4x1 cm organ-at-risk (OAR) foran målet. På grunn av usikkerhet i foton-LQ-parametrene som ble brukt som input for LEM, estimerte de proton-til-karbonion-risikoforhold, i stedet for individuelle risikoverdier.
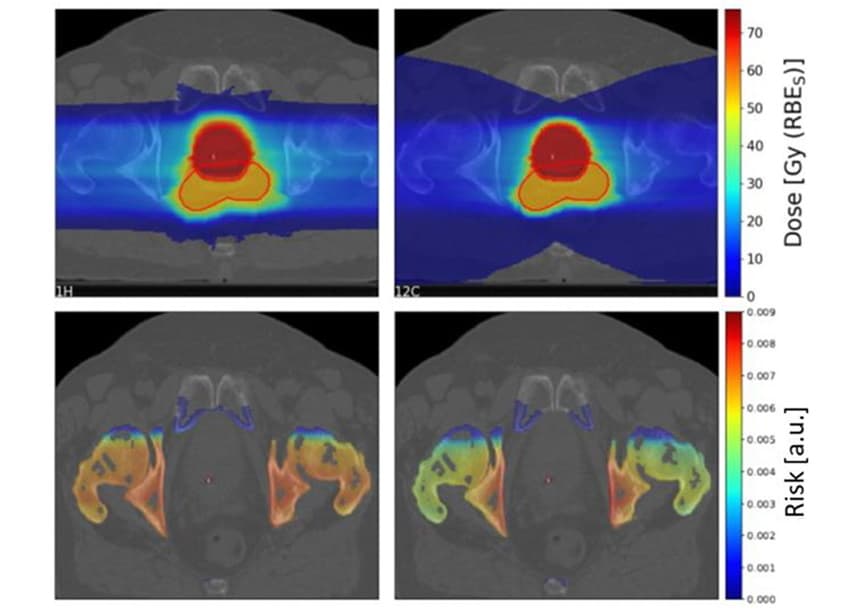
For disse idealiserte oppsettene viste ikke modellen en klar preferanse for verken protoner eller karbonioner, men avslørte en kompleks avhengighet av ulike parametere. Den reduserte laterale spredningen av karbonioner fører til lavere SC-risiko enn protoner i inngangskanalen. Imidlertid legger karbonioner en høyere dose bak målet på grunn av fragmenteringshalen, noe som øker SC-risikoen for OAR bak svulsten etter karbonionbestråling.
For enkeltstråleplaner var den totale SC-risikoen omtrent 1.5 ganger høyere for karbonioner enn for protoner. Med to motstående stråler var den totale SC-risikoen 1.16 ganger høyere for protoner, selv om denne varierte sterkt avhengig av den romlige plasseringen av det antatte sensitive volumet i forhold til målvolumet.
Radiosensitivitet i vev (for fotoner) hadde en stor innvirkning på SC-risikoforholdet, med radioresistente OAR-er som drar fordel av karbonionbehandling og sensitive OAR-er fra protonstråler. Derimot hadde fraksjoneringsordningen liten innvirkning på forventede risikoverdier.
Pasientgeometri
For å undersøke kliniske scenarier, estimerte Scholz og kolleger SC-risikoen for 10 prostatakreftpasienter tidligere behandlet med fotonstrålebehandling ved Karolinska Universitetssykehuset. De genererte behandlingsplaner for pasientene ved å bruke to sideveis motstående skannede proton- og karbonionfelt.
Som tidligere sett, resulterte fragmenteringshalen av karbonioner i et stort lavdoseområde bak målet. Imidlertid var høydosemålregionen mer konform for karbonionet enn protonplanene.
Teamet beregnet proton-til-karbonion SC risikoforhold for fire OARs (blære, rektum, bein og hud) for de 10 pasientene. For bein og hud ga protonplaner en litt høyere SC-risiko enn karbonionplaner, med median risikoforhold på henholdsvis 1.19 og 1.06 for bein og hud. For blære og rektum resulterte imidlertid protonplaner i betydelig lavere SC-risiko, med risikoforhold på henholdsvis 0.68 og 0.49 for blære og endetarm.
Forskerne konkluderer med at innsikten oppnådd med denne modellen kan bidra til å optimalisere fremtidige behandlinger. Foreløpig er relativ risikomodellering hovedsakelig egnet som et verktøy for å sammenligne ulike behandlingsscenarier for ulike pasientkohorter. Men Scholz bemerker at det vil være enkelt å inkludere slike modeller i behandlingsplanlegging for individuelle pasienter.

Karbonion-gitterterapi skåner sunt vev
"Det krever bare å kjøre planleggingen for en gitt dosefordeling med to forskjellige biologiske parametersett som representerer henholdsvis celledrap og celletransformasjonsprosessen," forklarer han. "Så er det bare noe etterbehandling av de resulterende 3D-effektfordelingene med standard matematiske verktøy som trengs for å utlede de tilsvarende risikoforholdsfordelingene."
Det neste trinnet, sier han, er å validere modellen via sammenligning med kliniske data. "Siden disse dataene for øyeblikket er knappe, vil utvidelse av tilnærmingen til også å inkludere fotonbehandlinger og å bestemme de tilsvarende risikoforholdene mellom protoner versus fotoner og karbonioner versus fotoner være et viktig neste skritt," forteller Scholz Fysikkens verden.