Cyberangrep på sykehus kan ha en ødeleggende innvirkning, spesielt for radiologi- og strålebehandlingsavdelinger som er spesielt avhengige av teknologi for å fungere. Et eksempel på dette er det landsomfattende cyberangrepet på Irlands offentlige helsetjenester i mai 2021, som avbrøt planlagte strålebehandlinger for enkelte kreftpasienter i opptil 12 dager.
Etter denne hendelsen har medisinske fysikere kl Universitetssykehuset Galway og National University of Ireland Galway begynte å utvikle et internt verktøy for å hjelpe med å lage reviderte strålebehandlingsplaner etter avbrudd. Verktøyet – kalt EQD2VH – beregner behandlingskompensasjonsplaner og muliggjør visuell sammenligning av alle planalternativer, samt individuell analyse av hver struktur i en pasients plan. Forskerne beskriver det nye programvareverktøyet i Journal of Applied Clinical Medical Physics.
Strålebehandling gis oftest over flere uker i en serie med små stråledoser (konvensjonelt 2 Gy) kalt fraksjoner. Uplanlagte behandlingshull – enten det skyldes cyberangrep, maskinhavari eller pasientsykdom – kan forårsake betydelige tilbakeslag. Under slike hull gjenpopuleres kreftceller raskt i tumorvev, noe som resulterer i en reduksjon i den radiobiologiske dosen til planleggingsmålvolumet (PTV).

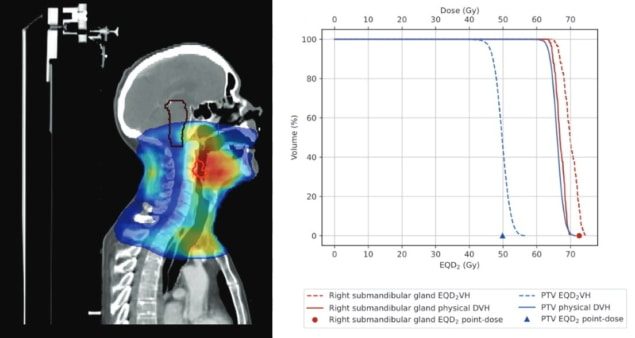
For å løse dette problemet, EQD2VH bruker dose-volum histogram (DVH) informasjon hentet fra opprinnelige pasientplaner for å utføre behandlingsgapberegninger. Hovedforfatter Katie O'Shea, fra National University of Ireland Galway, og kolleger forklarer at programvaren konverterer den fysiske dosen i hver dosebeholder (doseområdet mellom datapunkter i en DVH) til den biologisk effektive dosen (BED). Dette står for både repopulasjonseffekter i PTV og effektene av sub-letal skade på ureparert normalt vev i organer-at-risk (OARs).
Etter å ha modifisert BED-konverteringen for å ta hensyn til dosevariasjoner i hver struktur, ved bruk av en variabel dose-metode, konverterer verktøyet BED for hver struktur til ekvivalent dose i 2 Gy-fraksjoner (EQD2). Dette normaliserer hver behandling til konvensjonell fraksjonering og gjør det mulig å summere planer med ulike fraksjoneringsopplegg. Den resulterende EQD2 -basert DVH gir en 2D-representasjon av virkningen av behandlingsgap-kompensasjonsstrategier på både PTV- og OAR-dosefordelinger, sammenlignet med den foreskrevne behandlingsplanen.
For å evaluere EQD2VH som et klinisk beslutningsverktøy valgte forskerne fem høyt prioriterte pasienter med raskt voksende svulster hvis behandlingsgap ikke skulle overstige to dager. Dette inkluderte fire pasienter med hode- og nakkekreft som gjennomgikk intensitetsmodulert strålebehandling og en lungekreftpasient som gjennomgikk 3D konform strålebehandling, som hadde behandlingsgap på 12 eller 13 dager. Disse tilfellene gjorde det mulig for teamet å evaluere bruken av EQD2VH for pasienter med både konvensjonell (2 Gy) og ikke-konvensjonell (2.2 Gy) fraksjonering og ulike behandlingsgaptider (fra ni til 46 dager inn i behandlingen).
De reviderte behandlingsplanene for hver pasient var basert på deres opprinnelige planer med enten dose-per-fraksjon eller antall fraksjoner endret. O'Shea forklarer at hver pasients reviderte plan og tidsplan brukte en kombinasjon av fraksjonering to ganger daglig, helgebehandlinger og økt dose til målvolumet for å redusere effekten av celle-repopulasjon.
Planene begrenset behandlingen til seks fraksjoner per uke og utelukket fraksjonering to ganger daglig på påfølgende dager. Hvis den foreskrevne behandlingen ikke kunne fullføres innen den nødvendige tidsrammen, undersøkte forskerne planer ved bruk av hypofraksjonering (levering av økt dose per fraksjon). De var i stand til visuelt og kvantitativt å sammenligne ulike reviderte planer med pasientens opprinnelige plan for å finne ut hvilken som ville levere den beste dosen til PTV med minst dose til OARs.
Forskerne bemerker at 2D-representasjonen av hver enkelt struktur i EQD2VH gir en mer dyptgående analyse enn Royal College of Radiologists (RCR) anbefalte 1D punktdoseberegningsmetode som for tiden brukes til å håndtere strålebehandlingsgap. En 1D-representasjon av dosedistribusjon innenfor et volum tar ikke hensyn til OARs som vanligvis har en ujevn dosefordeling og kan overvurdere OAR-dosen. I tillegg har EQD2VH-verktøyet kan lage planer for en hvilken som helst lengde på behandlingsgapet, mens RCR-retningslinjene er basert på et standardgap på fire til fem dager.
Ytterligere fordeler med det nye verktøyet inkluderer muligheten til å overvåke hver OAR i pasientens plan for å minimere ytterligere doseøkninger som kan forårsake mer akutte toksisiteter. Brukere kan også beregne virkningen av ulike behandlingsgap-varigheter på en pasients behandling. Denne evnen kan bidra til å avgjøre om en pasient skal overføres til en annen klinikk hvis avstanden ved den planlagte klinikken er for lang eller om pasienten trygt kan vente på at behandlingen gjenopptas.

Hvordan har COVID-19 påvirket tilbudet av strålebehandling?
EQD2VH kan også forklare endringer i den totale behandlingstiden og subletal skade i normalt vev, noe et kommersielt system kanskje ikke kan gjøre. Det viktigste er at verktøyet ikke trenger å være koblet til sykehusnettverket for å fungere – det kan brukes selv om et sykehuss servere fortsatt er ødelagt av et cyberangrep.
"Vi evaluerer fortsatt EQD2VH som et beslutningsverktøy, sier hovedetterforsker Margaret Moore fra University Hospital Galway. "Det er en del av et pågående prosjekt som gjennomgår pasienter som får flere re-behandlinger for palliative regimer der dosen per fraksjon er ikke-standard og hvor det kan være et utvalg av fraksjoneringsskjemaer å vurdere. Konvertering av behandlingsdose fra en rekke behandlinger med ulike fraksjoneringer til EQD2 lar den radiobiologiske dosen til målvev og OAR akkumuleres for en samlet doseoversikt, noe som kan hjelpe med beslutningstaking for valg av videre behandling."