Kroppenes molekylære maskineri brytes ned med alderen.
DNA akkumulerer mutasjoner. De beskyttende endene deres eroderer bort. Mitokondrier, cellens energifabrikk, vakler og bryter ned. Immunforsvaret går løs. Reservebasen av stamceller minker, mens noen modne celler går inn i en zombie-lignende tilstand og spyr ut giftige kjemikalier i miljøet.
Bildet høres forferdelig ut, men det er ikke bare dårlige nyheter. Aldring er et komplisert puslespill. Ved å finne individuelle stykker, kan forskere sette sammen et fullstendig bilde av hvordan og hvorfor vi eldes – og utvikle nye måter å avverge aldersrelaterte symptomer.
Det har allerede vært en viss suksess. Senolytika – medisiner som dreper zombieceller –er allerede i kliniske studier. Delvis omprogrammering, som sletter en celles identitet og returnerer den tilbake til en stamcelle-lignende tilstand, får damp som en lovende alternativ behandling, og det er en av de hotteste levetidsinvesteringene i Silicon Valley.
En ny studie in Natur jaktet på en annen brikke til det aldrende puslespillet. I fem arter på tvers av den evolusjonære skalaen – ormer, fluer, mus, rotter og mennesker – satte teamet inn på en kritisk molekylær prosess som driver hver eneste celle inne i kroppen og degraderes med alderen.
Prosessen, kalt transkripsjon, er det første trinnet i å gjøre vårt genetiske materiale om til proteiner. Her blir DNA-bokstaver omarbeidet til en "budbringer" kalt RNA, som deretter sender informasjonen til andre deler av cellen for å lage proteiner.
Forskere har lenge mistenkt at transkripsjon kan gå galt med aldring, men den nye studien gir bevis på at den ikke gjør det - med en vri. I alle de fem artene som ble testet, gikk prosessen overraskende raskere etter hvert som organismen ble eldre. Men som å prøve å skrive raskere med bind for øynene, økte også feilraten.
Det er en løsning. Ved å bruke to intervensjoner kjent for å forlenge levetiden, var teamet i stand til å bremse transkripsjonen i flere arter, inkludert mus. Genetiske mutasjoner som reverserte den slurvete transkripsjonen forlenget også levetiden hos ormer og fruktfluer, og økte menneskelige cellers evne til å dele seg og vokse.
Det nye kjennetegnet for aldring er knapt klart for testing på mennesker. Men "det åpner opp et veldig grunnleggende nytt område for å forstå hvordan og hvorfor vi eldes," sa Dr. Lindsay Wu ved UNSW Sydney, som ikke var involvert i studien.
Den genetiske redaktøren
Å gjøre vår genetiske plan til proteiner er en to-trinns prosess.
Først blir DNAs fire bokstaver - A, T, C og G - transkribert til RNA. RNA, som også består av fire bokstaver, er i utgangspunktet molekylære notater som kan skli forbi DNAs begrensede plass for å levere meldinger til cellens proteinfremstillingsfabrikk. Der blir RNA oversatt til proteiners språk.
Det første trinnet - å gjøre DNA til RNA - er vanskeligere enn det høres ut. For å spare plass er DNA tett pakket rundt en gruppe proteiner kalt histoner, som bacon rundt åtte aspargesstilker. Dette "gjemmer" effektivt den genetiske informasjonen, noe som gjør det umulig for cellen å lese.
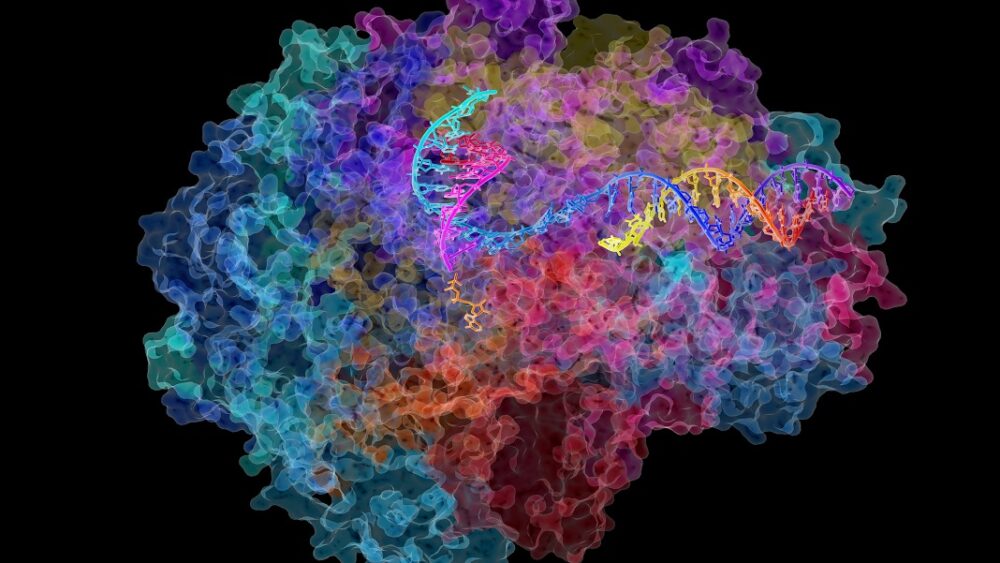
Det trengs en hel landsby med proteinhjelpere for å slappe av DNA og forberede det for transkripsjon. Men stjernen er Pol II (RNA-polymerase II), et gigantisk multikompleks som beveger seg langs en DNA-streng som hjelper den å transformere seg til en tidlig versjon av RNA, passende kalt pre-RNA.
Som en ordrik setning blir pre-RNA deretter kopiert til pithier-sekvenser for å bygge proteiner, en prosess som kalles spleising. Pol II overser hele prosessen, og sørger for at hundretusenvis av RNA er perfekt laget.
Men etter hvert som vi blir eldre, forringes prosessen. Ingen har funnet ut hvorfor.
Den nye studien spurte: hvorfor ikke finpusse stjernen i transkripsjonsshowet?
Spennende arter
Å tyde aldrende kjennetegn kommer med en snublestein: en potensiell bly kan bare være relevant for én art.
Den nye studien taklet problemet direkte ved å undersøke fem arter. Ved å bruke en teknikk kalt RNA-sekvensering fanget de Pol IIs hastighet da den rullet ned DNA fra orm, fruktflue, mus, rotte og menneskeceller i forskjellige aldre. Menneskelige prøver varierte fra 21 til 70 år, sammen med to "udødelige" dyrkede cellelinjer.
For en enda mer omfattende oversikt testet teamet prøver fra flere organer, inkludert hjernen, leveren, nyrene og blodet.
Resultatene kom tilbake som en overraskelse. Selv om hver art hadde sin egen Pol II "hastighetssignatur", var trenden den samme: Poll II økte på tvers av arter med alderen i hvert vev som ble undersøkt. Det eksakte genet eller vevet spilte ingen rolle. Den aldersrelaterte endringen dekket omtrent 200 forskjellige gener i flere arter. I stedet for en lokal endring, så Pol II-hastigheten ut til å være en universell aldringsmarkør.
Med farten kom imidlertid feilene. Skjøting - som redigerer pre-RNA - krever at Pol II-hastigheten er i en Goldilocks-sone. Å øke hastigheten øker risikoen for dårlige oversettelser, som i tidligere studier "har vært assosiert med høy alder og forkortet levetid," forklarte forfatterne.
"Økt hastighet på Pol II kan føre til flere transkripsjonsfeil fordi korrekturkapasiteten til Pol II er utfordret," sa de.
Skru tilbake klokken
Hvis Pol II i overdrive bidrar til aldring, kan vi bremse den – og i sin tur bekjempe aldring?
I en test benyttet teamet seg av to velkjente behandlinger for å forsinke aldring: hemme insulinsignalering og kaloribegrensning. Hos ormer, fluer og mus reduserte den genetiske forstyrrelsen av insulinfølingsbanen tempoet til Pol II. Å sette mus på diett i tidlig voksen alder og middelalder – men ikke høy alder – tråkket også bremsene på Pol II.
Nok en test finpusset på det ultimate spørsmålet: driver Pol II-akselerasjon aldring? Her sporet teamet en horde av genetisk konstruerte ormer og fruktfluer med mutasjoner som reduserer deres Pol II-hastighet. Sammenlignet med ikke-mutanter, forlenget begge konstruerte stammer levetiden med 10 til 20 prosent.
Da teamet brukte CRISPR-Cas9 for å reversere Pol II-mutasjonene i ormer, ble levetiden deres imidlertid forkortet og matchet villtype-fellene. Det virker som Pol II er en årsak til aldring, forklarte forfatterne.
Hvorfor?
Ved å grave dypere inn i transkripsjonsmaskineriet fant teamet ett svar. Husk: DNA er pakket inn i bacon-aspargesbunter, vitenskapelig kjent som nukleosomer. Ved å sammenligne menneskelige navleveneceller og lungeceller fant teamet at når cellene eldes, slapper buntene sakte av og faller fra hverandre. Dette gjør det mye lettere for Pol II å gli over en DNA-streng, og i sin tur utløse en transkripsjonshastighetsøkning.
Ytterligere testing av teorien deres, satte teamet genetisk inn to typer histonproteiner - aspargesdelen av nukleosombunten - for å danne flere nukleosomer i menneskelige celler i petriskåler. Dette skapte igjen flere fartshumper for Pol II og bremset farten.
Det funket. Celler med ekstra histonproteiner hadde mindre sjanse for å bli aldrende zombieceller. I fruktfluer, en populær modell for forskning på lang levetid, ga den genetiske tilpasningen dem en betydelig levetid.
Selv om det fortsatt er veldig tidlig, er resultatene gode nyheter for potensielt å forfølge en ny klasse av antialdringsmedisiner. Pol II har blitt grundig forsket på kreftbehandling, med flere medisiner som allerede er testet og godkjent, noe som gir muligheten til å gjenbruke medisinene for forskning på lang levetid.
"Til sammen avslører dataene som presenteres her en molekylær mekanisme som bidrar til aldring og tjener som et middel for å vurdere påliteligheten til cellemaskineriet under aldring og sykdom," sa teamet.
Bilde Credit: David Bushnell, Ken Westover og Roger Kornberg, Stanford University/NIH Image Gallery
- SEO-drevet innhold og PR-distribusjon. Bli forsterket i dag.
- Platoblokkkjede. Web3 Metaverse Intelligence. Kunnskap forsterket. Tilgang her.
- Minting the Future med Adryenn Ashley. Tilgang her.
- kilde: https://singularityhub.com/2023/04/18/this-longevity-study-across-5-species-found-a-new-pathway-to-reverse-aging/
- : har
- :er
- $OPP
- 10
- 70
- a
- evne
- I stand
- Akkumulere
- tvers
- Ytterligere
- avansert
- Ages
- Aldring
- Alle
- langs
- allerede
- alternativ
- Selv
- og
- En annen
- besvare
- hverandre
- godkjent
- ER
- AREA
- rundt
- AS
- vurdere
- assosiert
- At
- forfattere
- tilbake
- dårlig
- I utgangspunktet
- BE
- fordi
- bli
- vært
- Blokker
- blod
- kroppen
- øke
- styrket
- øker
- Brain
- Break
- pauser
- Bygning
- by
- som heter
- CAN
- Kreft
- kreftterapi
- Kapasitet
- Årsak
- Celler
- utfordret
- sjanse
- endring
- klasse
- Klinisk
- bekjempe
- sammenlignet
- sammenligne
- komplisert
- omfattende
- medvirkende
- dekket
- opprettet
- kreditt
- kritisk
- dato
- dypere
- leverer
- Kosthold
- forskjellig
- dire
- sykdom
- dna
- ned
- stasjonen
- Narkotika
- under
- Tidlig
- enklere
- effektivt
- slutter
- energi
- ingeniør
- Enter
- Hele
- Miljø
- feil
- feil
- Selv
- Hver
- undersøke
- forklarte
- utvide
- fabrikk
- Fall
- raskere
- fidelity
- tenkte
- finne
- Først
- Fix
- Til
- skjema
- funnet
- fire
- fra
- fullt
- fundamental
- få
- giganten
- Go
- Går
- flott
- Gruppe
- Grow
- Ha
- hjelpe
- her.
- hotteste
- Hvordan
- Men
- HTTPS
- menneskelig
- Hundrevis
- Identitet
- bilde
- Immunsystem
- umulig
- in
- Inkludert
- økende
- individuelt
- informasjon
- Investeringer
- involvert
- IT
- jpg
- Drepe
- kjent
- Språk
- føre
- levetid
- i likhet med
- linjer
- Liver
- lokal
- Lang
- levetid
- maskiner
- laget
- gjøre
- GJØR AT
- Making
- markør
- matchet
- materiale
- Saken
- moden
- Kan..
- midler
- mekanisme
- meldinger
- Middle
- mitokondrier
- modell
- molekyl~~POS=TRUNC
- mer
- trekk
- flere
- Natur
- Ny
- nyheter
- bemerkelsesverdig
- Merknader
- roman
- of
- Tilbud
- Gammel
- on
- ONE
- åpner
- Annen
- vår
- egen
- Fred
- del
- deler
- Past
- prosent
- bilde
- brikke
- stykker
- plato
- Platon Data Intelligence
- PlatonData
- avstemning
- basseng
- Populær
- potensiell
- potensielt
- krefter
- Forbered
- presentert
- forrige
- Problem
- prosess
- lovende
- bevis
- Beskyttende
- Protein
- Proteiner
- gi
- Sette
- puslespillet
- spørsmål
- ROTTE
- priser
- heller
- Lese
- klar
- redusere
- relevant
- husker
- forskning
- Reserve
- begrensning
- Resultater
- avsløre
- reversere
- Risiko
- RNA
- Valsede
- omtrent
- Sa
- samme
- forskere
- syntes
- synes
- dømme
- sekvense
- betjene
- Vis
- Silicon
- Silicon Valley
- enkelt
- Skyv
- langsom
- Sakte
- noen
- Rom
- fart
- hastigheter
- Stjerne
- Tilstand
- Damp
- stem
- Stamceller
- Trinn
- Still
- stammer
- studier
- Studer
- snuble
- suksess
- overraskelse
- sydney
- Symptomer
- system
- tar
- Tappet
- lag
- test
- Testing
- Det
- De
- informasjonen
- deres
- Dem
- tusener
- tett
- til
- Transform
- behandling
- Trend
- utløsende
- SVING
- Turning
- vri
- typer
- ultimate
- forståelse
- Universell
- koble av
- brukt
- Dal
- versjon
- Se
- Village
- måter
- velkjent
- hvilken
- mens
- HVEM
- hele
- med
- arbeidet
- orm
- orm
- Innpakket
- wu
- år
- zephyrnet