En ny type datamodell som kan avsløre stråleskader på cellenivå kan forbedre strålebehandlingsresultatene for lungekreftpasienter.
Roman Bauer, en beregningsnevroforsker ved University of Surrey i Storbritannia, i samarbeid med Marco Durante og Nicolò Cogno fra GSI Helmholtzzentrum für Schwerionenforschung i Tyskland, laget modellen, som simulerer hvordan stråling interagerer med lungene på celle-for-celle basis.
Over halvparten av alle pasienter med lungekreft behandles med strålebehandling. Selv om denne tilnærmingen er effektiv, etterlater den opptil 30 % av mottakerne strålingsinduserte skader. Disse kan utløse alvorlige tilstander som påvirker pusten, som fibrose – der slimhinnen i alveolene (luftsekkene) i lungene blir fortykket og stivnet – og lungebetennelse – når veggene i alveolene blir betent.
For å begrense stråleskader på sunt vev samtidig som det dreper kreftceller, leveres strålebehandling i flere separate "fraksjoner". Dette gjør at en høyere – og derfor mer effektiv – dose kan administreres totalt fordi noen av de skadede friske cellene kan reparere seg selv mellom hver fraksjon.
Foreløpig velges strålebehandlingsfraksjoneringsskjemaer basert på tidligere erfaringer og generaliserte statistiske modeller, så de er ikke optimalisert for individuelle pasienter. I motsetning til dette kan personlig tilpasset medisin oppnås takket være denne nye modellen som, som Durante, direktør for Biofysisk avdeling ved GSI forklarer, ser på "toksisitet i vev med utgangspunkt i de grunnleggende cellulære reaksjonene og [er] derfor i stand til å forutsi hva som skjer med enhver pasient" når forskjellige fraksjoneringsskjemaer er valgt.
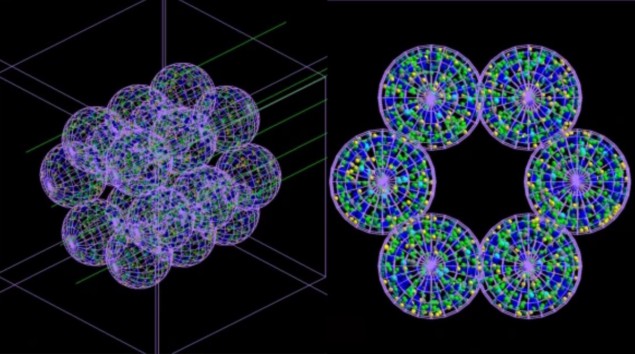
Teamet utviklet en "agent-basert" modell (ABM) bestående av separate interagerende enheter eller agenter - som i dette tilfellet etterligner lungeceller - kombinert med en Monte Carlo-simulator. ABM, beskrevet i Kommunikasjonsmedisin, bygger en representasjon av et alveolært segment bestående av 18 alveoler hver 260 µm i diameter. Deretter utføres Monte Carlo-simuleringer av bestråling av disse alveolene i mikroskopisk og nanoskopisk skala, og informasjon om strålingsdosen levert til hver celle og dens distribusjon blir matet tilbake til ABM.
ABM bruker denne informasjonen til å finne ut om hver celle vil leve eller dø, og sender ut de endelige resultatene i form av et 3D-bilde. Det er avgjørende at den koblede modellen kan simulere tidens gang og dermed vise alvorlighetsgraden av stråleskade – og progresjonen av de medisinske tilstandene den kan forårsake – timer, dager, måneder eller til og med år etter behandling.
"Det jeg syntes var veldig spennende er at disse beregningssimuleringene faktisk ga resultater som samsvarte med ulike eksperimentelle observasjoner fra forskjellige grupper, laboratorier og sykehus. Så vår beregningsmessige tilnærming kan i prinsippet brukes innenfor en klinisk setting, sier Bauer, talspersonen for det internasjonale BioDynaMo samarbeid, som har som mål å bringe nye beregningsmetoder inn i helsevesenet via programvarepakken som brukes til å bygge denne modellen.
Bauer begynte å jobbe med beregningsbaserte kreftmodeller etter at en nær venn døde av sykdommen bare 34 år gammel. "Hver kreft er forskjellig og hver person er forskjellig, med forskjellige formede organer, genetiske predisposisjoner og livsstil," forklarer han. Håpet hans er at informasjon fra skanninger, biopsier og andre tester kan mates inn i den nye modellen for å gi et bilde av hver enkelt. En AI-assistert behandlingsprotokoll kan deretter opprettes som vil produsere en tett skreddersydd behandlingsplan som forbedrer pasientens sjanser for å overleve.
Pasientspesifikk planlegging kan forbedre strålebehandlingsresultatene
Bauer søker for tiden samarbeidspartnere fra andre disipliner, inkludert fysikk, for å hjelpe til med å gå mot en klinisk studie etter lungekreftpasienter over flere år. I mellomtiden har teamet til hensikt å utvide modellens bruk til andre områder innen medisin.
Durante, for eksempel, håper å studere virusinfeksjon med denne lungemodellen, da den "kan forutsi lungebetennelse indusert av COVID-19-infeksjonen". I mellomtiden har Bauer begynt å simulere utviklingen av kretsløp i hjernen til premature babyer, med mål om å bedre forstå "på hvilket tidspunkt å gripe inn og hvordan".
- SEO-drevet innhold og PR-distribusjon. Bli forsterket i dag.
- PlatoData.Network Vertical Generative Ai. Styrk deg selv. Tilgang her.
- PlatoAiStream. Web3 Intelligence. Kunnskap forsterket. Tilgang her.
- PlatoESG. Karbon, CleanTech, Energi, Miljø, Solenergi, Avfallshåndtering. Tilgang her.
- PlatoHelse. Bioteknologisk og klinisk etterretning. Tilgang her.
- kilde: https://physicsworld.com/a/modelling-lung-cells-could-help-personalize-radiotherapy/
- : har
- :er
- :ikke
- $OPP
- 135
- 3d
- a
- I stand
- Om oss
- AC
- oppnådd
- faktisk
- administrert
- påvirke
- Etter
- alderen
- agenter
- mål
- AIR
- Alle
- tillater
- Selv
- an
- og
- noen
- tilnærming
- ER
- områder
- AS
- At
- tilbake
- basert
- grunnleggende
- basis
- BE
- fordi
- bli
- begynte
- begynt
- Bedre
- mellom
- puste
- bringe
- bygge
- bygger
- by
- CAN
- Kreft
- Kreftceller
- gjennomført
- saken
- Årsak
- celle
- Celler
- sjansene
- valgt ut
- Klinisk
- Lukke
- tett
- samarbeid
- samarbeidspartnere
- beregnings
- datamaskin
- forhold
- Består
- kontrast
- kunne
- kombinert
- Covid-19
- opprettet
- avgjørende
- I dag
- skade
- Dager
- levert
- Avdeling
- beskrevet
- utviklet
- Utvikling
- Die
- døde
- forskjellig
- Regissør
- disipliner
- sykdom
- distribusjon
- dose
- hver enkelt
- Effektiv
- Selv
- Hver
- spennende
- Expand
- erfaring
- eksperimentell
- forklarer
- Fed
- slutt~~POS=TRUNC
- etter
- Til
- skjema
- funnet
- brøkdel
- venn
- fra
- generalisert
- genetisk
- Tyskland
- mål
- Gruppens
- Halvparten
- skjer
- he
- helsetjenester
- sunt
- hjelpe
- høyere
- hans
- håp
- håper
- sykehus
- TIMER
- Hvordan
- HTTPS
- i
- forbedre
- forbedrer
- in
- Inkludert
- individuelt
- informasjon
- skader
- f.eks
- hensikt
- samhandler
- interaktiv
- internasjonalt
- gripe inn
- inn
- utstedelse
- IT
- DET ER
- jpg
- bare
- drepe
- Labs
- Nivå
- livsstil
- BEGRENSE
- fôr
- leve
- UTSEENDE
- matchet
- max bredde
- Kan..
- Mellomtiden
- medisinsk
- medisin
- metoder
- mikroskopisk
- modell
- modellering
- modeller
- måneder
- mer
- flytte
- Natur
- Ny
- neste
- of
- on
- optimalisert
- or
- rekkefølge
- Annen
- vår
- ut
- utfall
- produksjon
- utganger
- enn
- samlet
- passasje
- Past
- pasient
- pasienter
- person
- tilpasse
- Personlig
- Fysikk
- Fysikkens verden
- bilde
- fly
- planlegging
- plato
- Platon Data Intelligence
- PlatonData
- Point
- forutsi
- prematur
- prinsipp
- progresjon
- protokollen
- gi
- strålebehandling
- reaksjoner
- mottakere
- reparasjon
- representasjon
- Resultater
- avsløre
- sier
- Skala
- skanner
- ordninger
- søker
- segmentet
- separat
- alvorlig
- innstilling
- flere
- formet
- Vis
- simulere
- simuleringer
- simulator
- So
- Software
- noen
- talsperson
- Start
- statistisk
- Still
- Studer
- slik
- suite
- Surrey
- overlevelse
- skreddersydd
- lag
- tester
- Takk
- Det
- De
- Storbritannia
- seg
- deretter
- terapi
- derfor
- Disse
- denne
- thumbnail
- Dermed
- tid
- til
- mot
- behandlet
- behandling
- prøve
- utløse
- sant
- typen
- Uk
- forståelse
- lomper
- bruke
- brukt
- bruker
- ved hjelp av
- ulike
- veldig
- av
- viral
- Hva
- når
- om
- hvilken
- mens
- med
- innenfor
- Arbeid
- trene
- arbeid
- verden
- ville
- år
- zephyrnet