Behandling av kreftpasienter med romlig modulerte strålingsstråler kan ødelegge svulster samtidig som skade på nærliggende organer og sunt vev minimeres. Det er ideen bak proton ministråle stråleterapi (pMBRT), en fremvoksende behandlingsteknikk som bruker en rekke submillimeter store strålestråler for å levere terapeutisk dose.
Ministrålene består av alternerende høydosetopper og lavdosedaler, et mønster som er mindre skadelig for sunt vev på grunne dyp. På større dyp utvides disse strålene gradvis for å skape en homogen dosefordeling innenfor målvolumet. Studier på små dyr har vist at pMBRT kan dramatisk redusere normal vevstoksisitetmed ekvivalent eller overlegen tumorkontroll, sammenlignet med konvensjonell protonterapi.
"Proton ministrålestrålebehandling har allerede vist en bemerkelsesverdig gevinst i den terapeutiske indeksen i prekliniske studier," sier Ramon Ortiz fra Institut Curie. "Disse lovende resultatene oppmuntrer til oversettelse av denne teknikken til det kliniske domenet." Med dette målet evaluerte Ortiz (nå ved UC San Francisco) og kolleger ved Institut Curie fordelene med pMBRT for behandling av kreftmetastaser, rapporterte funnene sine i Medisinsk fysikk.
Simulering av pMBRT-scenarier
Metastatisk sykdom står for opptil 90 % av kreftrelaterte dødsfall. Metastaser behandles vanligvis med stereotaktisk strålebehandling (SRT), men dosen som kreves for lokal kontroll er ofte begrenset av risikoen for toksisitet til nærliggende normalt vev. For hjernemetastaser, for eksempel, rapporteres strålingsindusert hjernenekrose hos halvparten av pasientene behandlet med SRT.
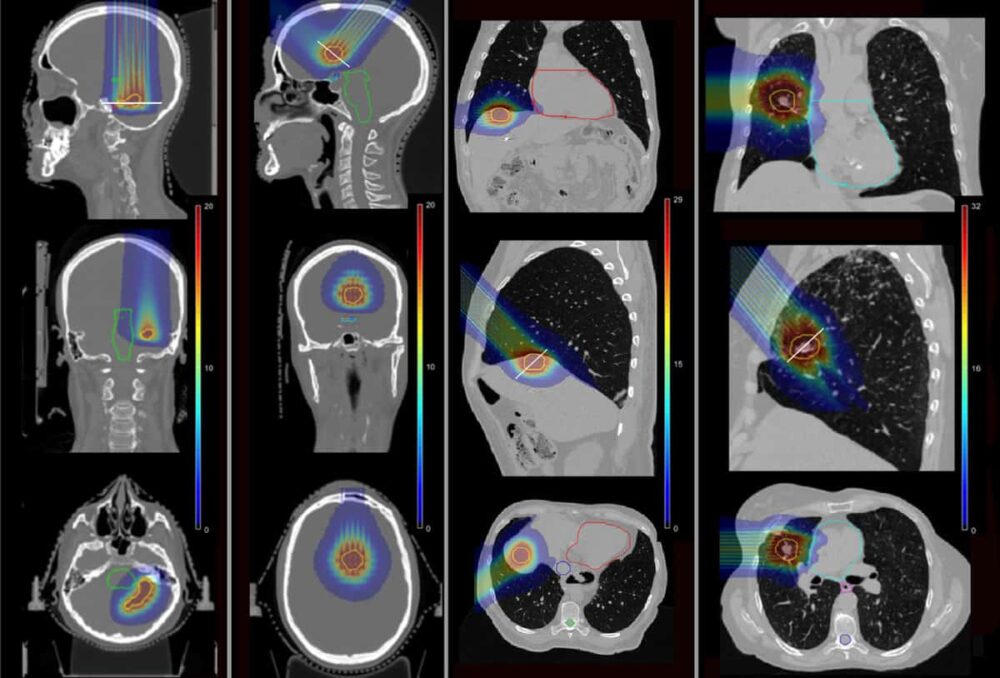
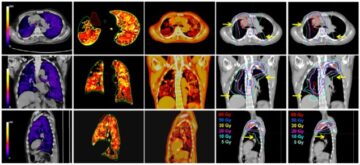
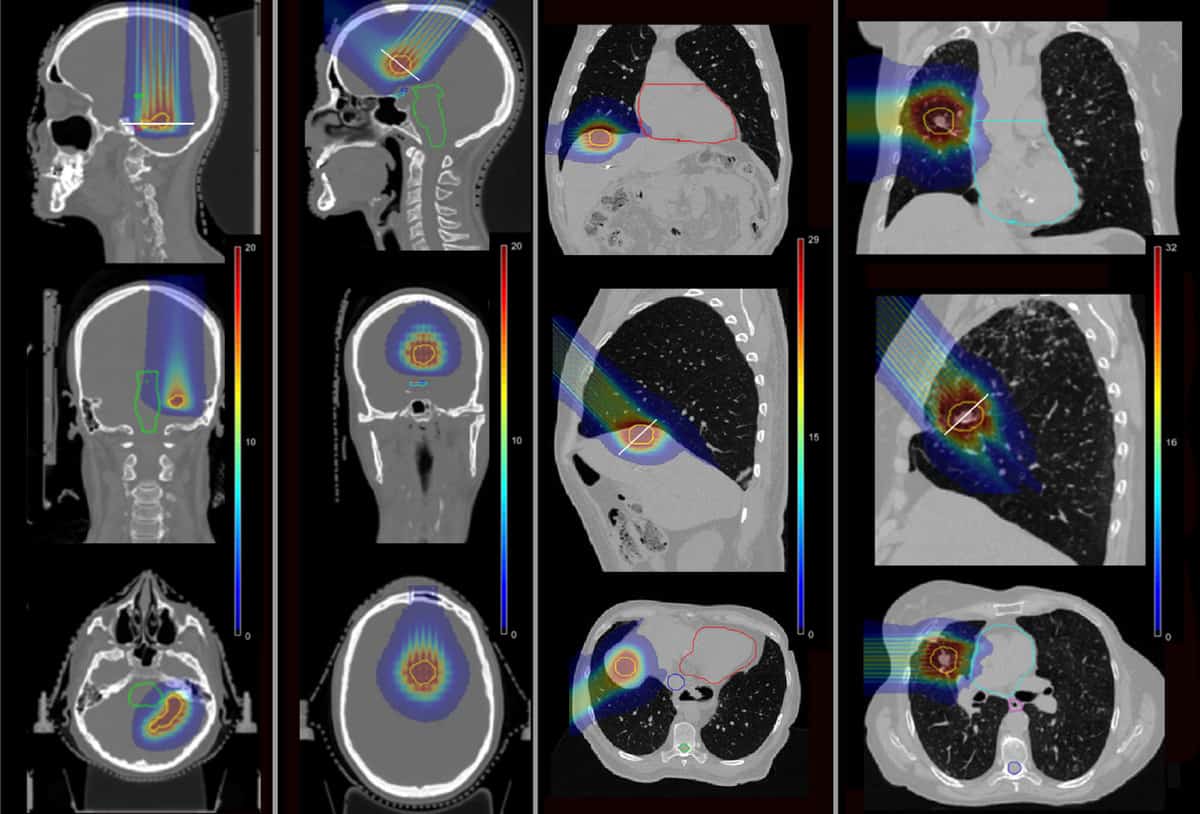
For å avgjøre om pMBRT kan redusere slike komplikasjoner, brukte teamet Monte Carlo-simuleringer for å beregne dosefordelinger for fire pasienter som tidligere mottok SRT ved Institut Curie. Pasientene hadde blitt behandlet for metastatiske lesjoner i hjernens tinninglapp, frontallapp, lever og lunge.
Forskerne simulerte enkeltfraksjons pMBRT-planer, ved å bruke ett eller to behandlingsfelt for å levere samme biologiske ekvivalentdose (BED) til tumormålet som foreskrevet for SRT. De modellerte en ministrålekollimator av messing som inneholdt 400 μm × 5.6 cm spalter ved forskjellige senter-til-senter-separasjoner, for å lage både smale og bredere avstandsplasserte ministråler. De beregnet deretter dosefordelinger for de fire pasienttilfellene, for pMBRT, SRT og konvensjonell protonterapi.
I pMBRT-planene med smal avstand, som skaper en jevn dosefordeling i målvolumet, var tumordekning lik eller litt bedre enn i SRT-planene. Planer som bruker pMBRT-stråler med bredere avstand, som leverer en kvasi-ensartet dosefordeling til målet, hadde en lavere tumordekning.
Viktigere, pMBRT reduserte dosen betydelig til kritiske strukturer sammenlignet med SRT. I det første hjernetilfellet reduserte pMBRT gjennomsnittlig BED til organer-at-risk (OARs) med mellom 44 % (høyre akustisk nerve) og 100 % (venstre akustisk nerve). I den andre hjernebehandlingen sparte pMBRT fullstendig OAR-ene, inkludert den optiske kanalen, hjernestammen og chiasmen.
I levertilfellet ble gjennomsnittlig BED til leveren og ribbeina redusert med henholdsvis 25 % og 75 %, samtidig som man unngikk bestråling av vena cava superior. Og for lungetilfellet ble dosen til OAR redusert med mellom 11 % (ribben) og 100 % (lungearterie og bronkier). Gjennomsnittlig BED til OARs var stort sett lik mellom pMBRT og konvensjonell protonterapi.
Forskerne undersøkte også mulige negative effekter av pMBRT på normalt vev. For de to tilfellene av hjernemetastaser, for eksempel, beregnet de dosen som ble levert til sunt hjernevev. De vurderte dosegrensene for standard fraksjonert bestråling, der en normalisert totaldose ved 2 Gy-fraksjoner (NTD)2.0) på 72 Gy fører til 5 % sannsynlighet for radionekrose innen fem år.
For alle pMBRT-planer, den maksimale dalen NTD2.0 til den friske hjernen (61 Gy(RBE) for tinninglappen og 47 Gy(RBE) for frontallappen) holdt seg under denne dosetoleranseterskelen, i motsetning til konvensjonell protonterapi. For pasientene med lunge- og levermetastaser var gjennomsnittsdosene til lunge- og levervev i pMBRT-planer også godt under de maksimalt tolerable gjennomsnittsdosene.
Kliniske fordeler
pMBRT-behandlingene som ble vurdert i denne studien ble levert ved bruk av bare én eller to ministråle-arrayer. Bruken av færre felt enn i SRT-behandlingene (tre eller fire buer) krever mindre reposisjonering av pasienten, reduserer fraksjonsbehandlingstiden, samt reduserer volumet av normalt vev som eksponeres for lave doser. I tillegg reduserer levering av pMBRT i én behandlingsfraksjon betraktelig den totale behandlingstiden sammenlignet med SRT-planene, som brukte tre til fem fraksjoner.

Ministrålebehandling: fra fotoner til ladede partikler
Forskerne påpeker at pMBRT-planene som er evaluert i dette arbeidet kan leveres klinisk ved å bruke oppsettet som allerede er implementert ved Orsay Proton Therapy Center for prekliniske studier, med mål- og organbevegelser under behandling kontrollert som i SRT og protonterapi.
Ortiz forteller Fysikkens verden at Institut Curie nå diskuterer muligheten for fase I/II kliniske studier. "Disse ville evaluere nevrotoksisiteten og svulstkontrollratene i behandlingen av tilbakevendende glioblastoma multiforme med protonministråler," forklarer han. "Denne studien har som mål å bidra til forberedelsen av disse kliniske undersøkelsene."
- SEO-drevet innhold og PR-distribusjon. Bli forsterket i dag.
- Platoblokkkjede. Web3 Metaverse Intelligence. Kunnskap forsterket. Tilgang her.
- kilde: https://physicsworld.com/a/proton-minibeams-could-improve-treatment-of-cancer-metastases/
- :er
- $OPP
- 10
- a
- kontoer
- tillegg
- uheldig
- mål
- AL
- Alle
- allerede
- og
- dyr
- ER
- Array
- AS
- At
- unngå
- BE
- bak
- under
- Fordeler
- Bedre
- mellom
- Brain
- messing
- by
- CAN
- Kreft
- saken
- saker
- sentrum
- ladet
- klikk
- Klinisk
- kliniske studier
- kollegaer
- kolonner
- vanligvis
- sammenlignet
- helt
- Beregn
- ansett
- kontrast
- bidra
- kontroll
- kontrolleres
- konvensjonell
- kunne
- dekning
- skape
- kritisk
- dødsfall
- leverer
- levert
- levere
- Dybder
- ødelegge
- Bestem
- diskutere
- sykdom
- distribusjon
- Distribusjoner
- domene
- dramatisk
- under
- effekter
- Emery
- oppmuntre
- Tilsvarende
- evaluere
- evaluert
- eksempel
- forklarer
- utsatt
- Felt
- Først
- Til
- brøkdel
- Francisco
- fra
- Gevinst
- gradvis
- større
- Halvparten
- skadelig
- Ha
- sunt
- HTTPS
- Tanken
- bilde
- implementert
- forbedre
- in
- I andre
- Inkludert
- indeks
- informasjon
- Undersøkelser
- utstedelse
- jpg
- bare én
- Fører
- Begrenset
- grenser
- Liver
- lokal
- Lav
- senking
- max bredde
- maksimal
- minimere
- bevegelse
- Natur
- normal
- of
- on
- ONE
- åpen
- Annen
- skissert
- pasient
- pasienter
- Mønster
- fase
- Fotoner
- planlegging
- planer
- plato
- Platon Data Intelligence
- PlatonData
- Point
- mulighet
- mulig
- tidligere
- lovende
- strålebehandling
- priser
- mottatt
- redusere
- Redusert
- reduserer
- redusere
- forble
- bemerkelsesverdig
- rapportert
- påkrevd
- Krever
- forskere
- Resultater
- Risiko
- samme
- San
- San Fransisco
- sier
- Sekund
- grunne
- vist
- betydelig
- lignende
- liten
- Standard
- studier
- Studer
- slik
- overlegen
- Target
- lag
- teknikker
- forteller
- Det
- De
- deres
- Disse
- tre
- terskel
- thumbnail
- tid
- til
- toleranse
- Totalt
- Oversettelse
- behandling
- behandling
- forsøk
- sant
- bruke
- Dal
- ulike
- volum
- volumer
- VI VIL
- om
- hvilken
- mens
- HVEM
- med
- innenfor
- Arbeid
- ville
- år
- zephyrnet