Zwyrodnienie plamki związane z wiekiem (AMD) jest główną przyczyną ślepoty. Rozpoczyna się w zewnętrznej barierze krew-siatkówka (oBRB) utworzonej przez nabłonek barwnikowy siatkówki (RPE), błonę Brucha i naczyniówkę. Mechanizmy inicjacji i progresji AMD nadal wymagają lepszego zrozumienia ze względu na brak fizjologicznie istotnych ludzkich modeli oBRB.
Zespół badawczy National Eye Institute (NEI), będący częścią National Institutes of Health, wykorzystał pacjenta komórki macierzyste oraz biodruk 3D w celu wytworzenia tkanki oka, która przyczyni się do lepszego zrozumienia mechanizmów chorób oślepiających. Naukowcy wydrukowali kombinację komórek tworzących zewnętrzną barierę krew-siatkówka.
Nabłonek barwnikowy siatkówki (RPE), oddzielony od bogatego w naczynia krwionośne choriocapillaris Błona Brucha, tworzy zewnętrzną barierę krew-siatkówka. Choriocapillaris i RPE wymieniają składniki odżywcze i odpady pod kontrolą błony Brucha. Druzy, które są nagromadzeniami lipoprotein, rozwijają się w AMD poza błoną Brucha i utrudniają jej funkcjonowanie. Degradacja RPE z biegiem czasu powoduje pogorszenie fotoreceptorów i utratę wzroku.
Naukowcy połączyli w hydrożelu trzy typy niedojrzałych komórek naczyniówki: perycyty, komórki śródbłonka i fibroblasty. Następnie wydrukowali żel na biodegradowalnym rusztowaniu. W ciągu kilku dni komórki zaczęły dojrzewać, tworząc gęstą sieć naczyń włosowatych.
Dziewiątego dnia naukowcy zaszczepili komórki nabłonka barwnikowego siatkówki na drugiej stronie rusztowania. Wydrukowana tkanka osiągnęła pełną dojrzałość w 42. dniu. Analizy tkanek oraz badania genetyczne i funkcjonalne wykazały, że wydrukowana tkanka wyglądała i zachowywała się podobnie do natywnej zewnętrznej bariery krew-siatkówka.
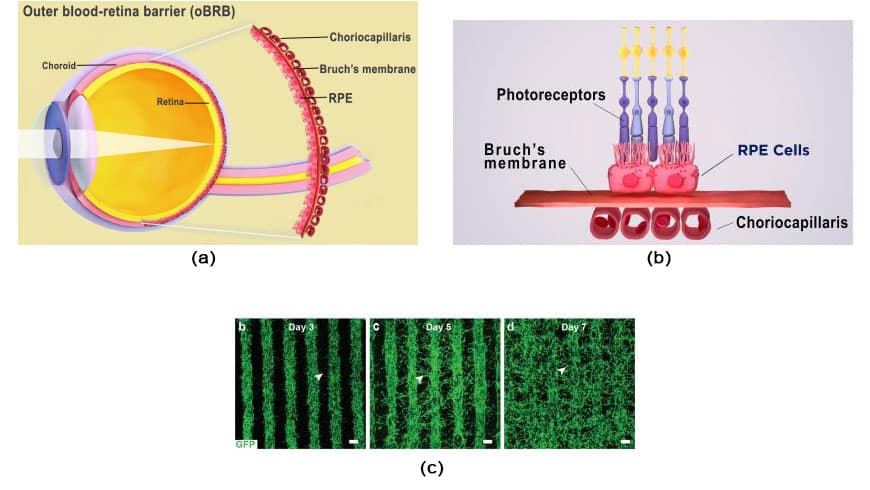
B. Zewnętrzna bariera krew-siatkówka oka składa się z nabłonka barwnikowego siatkówki, błony Brucha i naczyniówki. Źródło obrazu: Narodowy Instytut Oka.
C. Wzrost naczyń krwionośnych w drukowanych rzędach mieszaniny komórek śródbłonka, perycytów i fibroblastów. Do 7. dnia naczynia krwionośne wypełniają przestrzeń między rzędami, tworząc sieć naczyń włosowatych. Źródło obrazu: Kapil Bharti.
Poddana działaniu stresu zadrukowana tkanka wykazywała cechy AMD we wczesnym stadium, takie jak złogi druzów pod RPE, i przechodziła do późnego stadium AMD w fazie suchej, w którym obserwowano rozpad tkanki. Niski poziom tlenu powodował mokry wygląd przypominający AMD z hiperproliferacją naczyń naczyniówkowych, która przeniosła się do strefy poniżej RPE. Stosowane w leczeniu AMD leki anty-VEGF spowalniają tworzenie i migrację naczyń krwionośnych, jednocześnie poprawiając kształt tkanki.
Doktor Kapil Bharti, który kieruje sekcją NEI ds. badań nad translacją komórek ocznych i komórek macierzystych, powiedział: „Drukując komórki, ułatwiamy wymianę sygnałów komórkowych niezbędnych dla prawidłowej anatomii zewnętrznej bariery krew-siatkówka. Na przykład obecność komórek RPE indukuje ekspresja genów zmiany w fibroblastach, które przyczyniają się do tworzenia błony Brucha — coś, co sugerowano wiele lat temu, ale zostało udowodnione dopiero w naszym modelu”.
Naukowcy zajęli się dwoma kwestiami technologicznymi: stworzeniem odpowiedniego biodegradowalnego rusztowania i uzyskaniem spójnego wzoru nadruku. Opracowali wrażliwy na temperaturę hydrożel, który tworzył wyraźne rzędy, gdy żel był zimny, ale rozpuszczał się po ogrzaniu żelu. Bardziej dokładny system oceny architektury tkanki był możliwy dzięki dobrej spójności rzędów. Dodatkowo zoptymalizowali udział fibroblastów, komórek śródbłonka i perycytów w kombinacji komórek.
Współautor dr Marc Ferrer, dyrektor Laboratorium Biodruku Tkanek 3D w Narodowym Centrum Postępowych Nauk Translacyjnych NIH i jego zespół udostępnili wiedzę specjalistyczną w zakresie biofabrykacji zewnętrznych tkanek stanowiących barierę krew-siatkówka „w dołku, ” wraz z pomiarami analitycznymi umożliwiającymi badania przesiewowe leków.
[Osadzone treści]
„Nasze wspólne wysiłki zaowocowały bardzo odpowiednimi modelami tkanki siatkówki zwyrodnieniowych chorób oczu” – Ferrer powiedziany. „Takie modele tkanek mają wiele potencjalnych zastosowań w zastosowaniach translacyjnych, w tym w rozwoju terapii”.
Referencje czasopisma:
- Min Jae Song, Russ Quinn i in. Biodrukowana trójwymiarowa bariera zewnętrzna siatkówki odkrywa zależny od RPE fenotyp naczyniówki w zaawansowanym zwyrodnieniu plamki żółtej. Metody przyrodnicze, 2022; DOI: 10.1038/s41592-022-01701-1